三阴性乳腺癌(TNBC)是乳腺癌的一种侵袭性亚型,与高转移和高死亡率相关。由于三阴性乳腺癌患者的靶向治疗有限,迫切需要寻找有前景的靶点和治疗方案。
由于能量需求和营养微环境的不同,肿瘤在原发部位和转移部位的代谢重编程现象日益受到重视。侵袭性肿瘤在碳源利用方面表现出可塑性,以满足生物能量需求。尽管癌细胞的糖酵解水平升高,但它们也利用线粒体呼吸来产生大量的 ATP。
之前的研究表明,重编程为线粒体脂肪酸 β 氧化(FAO)是三阴性乳腺癌中占主导地位的代谢途径。而近期的研究发现,癌细胞中存在一种代谢混合状态,这种状态下癌细胞既能利用糖酵解途径,也能利用氧化磷酸化(OXPHOS)途径。这种癌细胞中的代谢混合状态对于肿瘤的进展以及对转移部位的适应至关重要。因此,在三阴性乳腺癌的治疗中,靶向线粒体代谢是一种颇具吸引力的治疗选择。
2025 年 2 月 10日,贝勒医学院的研究人员在 Cell 子刊 Cell Reports Medicine 上发表了题为:Biguanides antithetically regulate tumor properties by the dose-dependent mitochondrial reprogramming-driven c-Src pathway 的研究论文。
该研究发现了低剂量和高剂量的二甲 双胍对肿瘤有着完全相反的作用并揭示其机制,临床低剂量的二甲 双胍联合 Src 抑制剂(达沙替尼),能够抑制三阴性乳腺癌的进展和转移。

二甲 双胍等双胍类药物,作为 2 型糖尿病(T2DM)的一线治疗药物,最近已被用于抗癌治疗。二甲 双胍治疗的糖尿病患者癌症发病率降低,这促使了多项关于二甲 双胍在包括三阴性乳腺癌在内的多种癌症中的临床试验。
然而,二甲 双胍在肿瘤中未能达到有效浓度,在临床剂量下既不能抑制肿瘤增殖,也不能提供生存益处。因此,找到合适的治疗组合以应对双胍类药物因生物利用度差而效果有限的问题,是当务之急。
通过抑制线粒体电子传递链(ETC)复合物 I 的活性来抑制氧化磷酸化(OXPHOS),是双胍类药物抗癌活性的主要作用机制。近期有几项研究探讨了双胍类药物治疗癌症后的代谢调节情况。重要的是,一项临床研究发现,在接受二甲 双胍治疗的乳腺癌患者中,肿瘤存在两种不同的代谢亚组,其临床结局截然不同:一种是氧化磷酸化转录反应(OTR)组,其氧化磷酸化基因的转录增加;另一种是氟脱氧-D-葡萄糖(FDG)反应组,其 18-FDG 摄取增加。在二甲 双胍治疗后,OTR 组肿瘤表现出细胞增殖增加和耐药性增强。他们进一步的分析证实,以治疗剂量对原发性乳腺癌进行二甲 双胍治疗可增加 OTR 肿瘤中的脂肪酸 β 氧化(FAO),且 FAO 的激活与增殖增加相关。
因此,研究团队认为,在二甲 双胍治疗三阴性乳腺癌时,确定代谢重编程的伴随靶点对于开发有效的联合疗法至关重要。
该研究采用多种模型进行了全面分析,以揭示二甲 双胍在三阴性乳腺癌(TNBC)中诱导的线粒体与肿瘤通路之间的相互作用。
鉴于 FAO 可在侵袭性三阴性乳腺癌中激活 Src 激酶,研究团队推测低剂量双胍类药物驱动的 AMPK-ACC-FAO 信号通路可能在三阴性乳腺癌中激活 Src 通路。
在三阴性乳腺癌异种移植肿瘤中,二甲 双胍的低生物利用度类似于其体外低剂量效应。通过药物或基因手段抑制 FAO 能够显著增强了双胍类药物的抗肿瘤特性。较低剂量的双胍类药物可诱导 Src 信号传导,而较高剂量则会抑制。这些研究结果表明,低剂量二甲 双胍在体内可重编程三阴性乳腺癌的代谢,从而激活脂肪酸 β 氧化(FAO)-Src 激酶信号通路。
在上述发现的基础上,研究团队提出例如一种治疗新策略——临床剂量的二甲 双胍联合 Src 抑制剂达沙替尼,结果显示,联合治疗能够协同抑制三阴性乳腺癌患者来源的异种移植肿瘤的生长,但在高脂饮食喂养的小鼠中则无此作用,联合治疗还能抑制三阴性乳腺癌的转移。
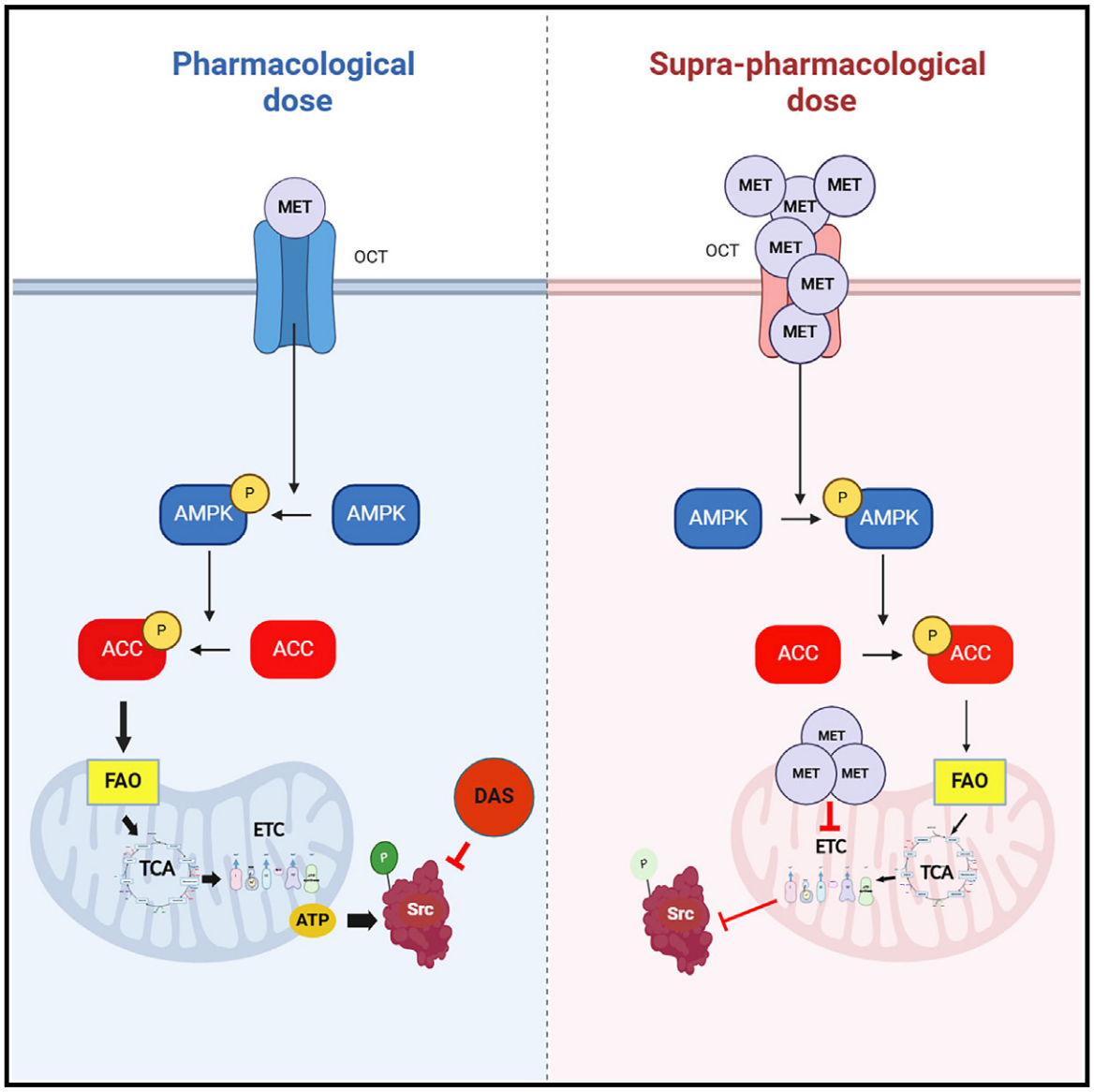
总的来说,该研究发现双胍类药物以剂量依赖性方式激活或抑制三阴性乳腺癌进展(低剂量促进,高剂量抑制),并揭示了低剂量的双胍类药物通过 AMPK-FAO 信号通路在三阴性乳腺癌中激活 Src 激酶。联合使用低剂量的二甲 双胍和 Src 抑制剂(达沙替尼)可抑制三阴性乳腺癌的进展和转移,从而为治疗选择有限的转移性三阴性乳腺癌提供潜在新疗法。
论文链接:
https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(25)00014-X



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57