
摘要:双抗药物,即双特异性抗体(BsAb),是一类能够同时识别并结合两种不同抗原或抗原表位的抗体分子。与传统单特异性抗体相比,双特异性抗体在肿瘤免疫治疗、自身免疫疾病、感染性疾病等领域具有独特的优势。本文将从作用机制、临床研究、应用进展等多个角度全面剖析双特异性抗体。0
双特异性抗体
双特异性抗体的概念起源于对传统单克隆抗体功能的拓展。单克隆抗体通常只能结合一个特定的抗原表位,而双特异性抗体(双抗)则是一种能够同时与两个不同抗原或同一抗原的两个表位结合的抗体。相较于单特异性抗体,双抗展现出更高的特异性,有效提升了治疗的效果和安全性,并显著降低了不良反应的发生。目前,市场上已有多种双抗药物获得批准上市,同时进入临床研究阶段的双抗药物数量正不断增长。因此,随着双抗药物形式的持续创新和应用范围的逐步扩大,其未来的应用前景也被广泛看好。
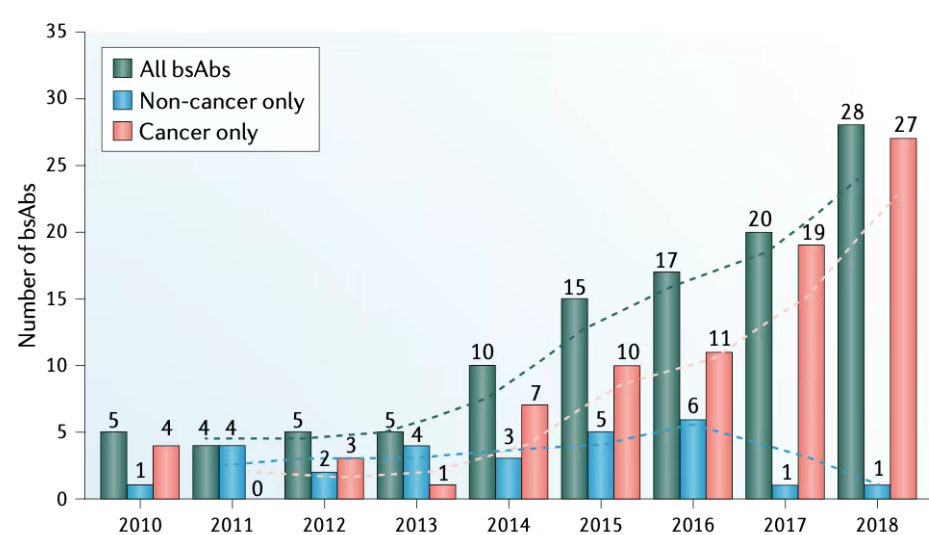
双特异性抗体数量变化情况(图源:免疫背包客)
双抗药物的作用机制
双抗药物的作用机制主要包括:细胞桥接、受体交联、辅助因子模拟和背负式运输等。细胞桥接机制通过同时结合肿瘤细胞和免疫细胞,促进两者相互作用,增强免疫细胞对肿瘤细胞的攻击能力。受体交联机制则通过结合并激活多个受体,引发多个信号通路,增强治疗效果。辅助因子模拟机制模拟并增强自然免疫系统中的辅助因子功能,增强免疫应答。背负式运输机制则将药物或细胞毒素运输到靶细胞,提高治疗的靶向性和效果。
由于双抗具备更强特异性、靶向性,可以降低脱靶毒性;相较单抗的组合疗法,也可有效降低治疗成本等。因此,在肿瘤治疗中具有广阔的应用前景。具体而言,双抗药物在肿瘤治疗领域的作用机制包括以下几点:
● 聚集/定位免疫细胞
双抗能够将免疫细胞聚集到特定的靶点位置,比如肿瘤细胞周围。通过与肿瘤细胞表面的抗原以及免疫细胞表面的相关受体结合,引导免疫细胞靠近肿瘤细胞,从而发挥免疫作用。
● 免疫细胞激活
双抗可以激活免疫细胞,例如T细胞等。当双抗与免疫细胞表面的受体结合后,能够启动免疫细胞内的信号传导通路,促使免疫细胞被激活,增强其对肿瘤细胞等异常细胞的杀伤能力。
● 阻断信号通路
很多肿瘤细胞的生长、增殖和转移依赖于一些特定的信号通路。双抗可以同时作用于这些信号通路中的多个靶点,阻断信号的传递,从而抑制肿瘤细胞的生长、增殖,诱导肿瘤细胞凋亡等。
双抗药物的作用机制(图源:Bicycle)
双抗药物临床研究应用进展
● 在肺癌治疗中的进展
● BL-B01D1
这是全球首个针对表皮生长因子受体(EGFR)×HER3的双特异性ADC药物。在针对62例EGFR野生型且曾接收含铂双药化疗并失败的NSCLC患者(其中93.5%的患者既往接受过免疫治疗)的研究中,客观缓解率(ORR)达到了30.6%,疾病控制率(DCR)达到了87.1%,而目前针对这类人群标准治疗药物有效率仅为16.6%。
● QL1706(艾帕洛利托沃瑞利单抗注射液)
由IgG4型PD-1抗体和IgG1型CTLA-4抗体按照特定比例组成。在60例EGFR野生型患者中,56例(93.3%)患者观察到病灶缩小,27例(45%)野生型EGFR患者实现部分缓解(PR),ORR达45%,DCR达88.3%;在31例携带突变EGFR的患者中,29例(93.5%)患者观察到病灶缩小,17例患者达到PR,ORR为54.8%,DCR为93.5%。
● Volrustomig(MEDI5752,PD-1×CTLA-4)
在2022年欧洲肿瘤内科学会(ESMO)上公布的一项探索Volrustomig一线治疗非鳞状(Nsq)NSCLC疗效及安全性的Ib/II期研究初步结果显示,与帕博利珠单抗联合化疗相比,Volrustomig(1500mgQ3W)联合化疗用于非鳞状NSCLC一线治疗时,可改善患者DoR、PFS和OS。在PD - L1 < 1%亚组中,Volrustomig(750 mg)+化疗的联合方案与对照组显示出相似的疗效,耐受性也得到改善。
卵巢癌治疗的创新进展
双抗药物在卵巢癌领域同样取得突破。PM8002(PD-L1×VEGF-A双抗)单药治疗铂耐药复发性卵巢癌(PROC)的Ib/II a期试验显示,ORR为20.6%,DCR达67.7%,中位PFS为8.3个月。另一项针对HER2的双抗ADC药物JSKN003在PROC患者中的合并分析表明其具有强效抗肿瘤活性与良好耐受性。其中,卡度尼利单抗(2022 年 6 月 29 日在中国获批上市,是全球首个获批上市的 PD-1/CTLA-4 双特异性抗体药物)联合化疗作为新辅助治疗用于晚期卵巢癌患者,R0切除率达73.7%,ORR高达95.8%,病理完全缓解(pCR)率为14.3%,显著改善预后。
其他方面的临床研究进展
● EGFR×MET双特异性抗体
其皮下制剂显示出不劣于静脉注射的药代动力学和抗肿瘤活性,在保证疗效的同时提高耐受性、减少给药时间及输液相关不良反应(IRR)、延长了患者OS。例如,CKD-702、EMB-01、MCLA-129等创新药物在早期临床研究中表现出临床治疗潜力。
● 依沃西单抗(PD-L1×VEGF)
HARMONi-A研究证实了依沃西单抗联合化疗能够显著延长EGFR-TKI经治NSCLC患者的PFS,同时初步显示出OS的获益趋势,且安全性可靠。对于可切除NSCLC患者,AK112-205研究证实了依沃西单抗无论是作为单药还是与化疗联合使用,在可切除NSCLC的围手术期治疗中均是安全且有效的。
双抗药物频频获批及其意义
● 塔奎妥单抗注射液的获批及其意义
● 药物概述
塔奎妥单抗注射液是由强生公司研发的首个靶向GPRC5D1的双特异性抗体药物,主要用于治疗既往接受过至少三线治疗的复发或难治性多发性骨髓瘤(RRMM)成人患者。
● 研究背景
该药物的获批基于一项单臂、开放标签、多中心研究MMY1001,显示出了较高且具有临床意义的ORR,尤其是在高风险亚组中,ORR与总体研究人群基本保持一致。
● 强生其他双抗药物的获批情况
● 埃万妥单抗
埃万妥单抗主要是用于一线治疗携带EGFR20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
● 格菲妥单抗
格菲妥单抗主要是用于治疗既往接受过至少两线系统性治疗的复发或难治性弥漫大B细胞淋巴瘤(DLBCL)成人患者,标志着中国淋巴瘤治疗进入双抗新时代。
结语
多项临床研究表明,双抗药物在提高缓解深度和持久疗效方面表现出色,尤其是在高风险患者群体中也显示出良好的治疗效果。随着更多双抗药物的获批,预计将为肿瘤患者提供更多治疗选择和希望,同时也为医药行业带来新的发展机遇和挑战。总而言之,双抗药物在我国的获批不仅为特定类型的患者带来了新的希望,同时也标志着中国肿瘤治疗领域进入了一个新的发展阶段。
参考文献:
1. Fang W, et al. Ivonescimab Plus Chemotherapy in Non-Small Cell Lung Cancer With EGFR Variant: A Randomized Clinical Trial. JAMA. 2024 May 31.
2. Cho BC, et al. Amivantamab plus Lazertinib in Previously Untreated EGFR-Mutated Advanced NSCLC. N Engl J Med. 2024 Jun 26.
3. Passaro A, et al. Amivantamab plus chemotherapy with and without lazertinib in EGFR-mutant advanced NSCLC after disease progression on osimertinib: primary results from the phase III MARIPOSA-2 study. Ann Oncol. 2024 Jan;35(1):77-90.
4. Ahn MJ, et al. Tarlatamab for Patients with Previously Treated Small-Cell Lung Cancer. N Engl J Med. 2023 Nov 30;389(22):2063-2075.
5. Lingying Wu, et al. Efficacy and safety of PM8002, a bispecific antibody targeting PD-L1 and VEGF-A, as a monotherapy in patients with solid tumors: Clinical data from advanced cervical cancer and platinum-resistant recurrent ovarian cancer cohorts.J Clin Oncol 42, 2024 (suppl 16; abstr 5524).
6. Wang C, et al. A Phase II Study of Perioperative Ivonescimab Alone or Combined with Chemotherapy in Resectable Non-Small Cell Lung Cancer.2024 WCLC Abtract OA01.06.
作者简介
凯文,从事药物临床评价与合理用药、药事管理相关研究。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57