2025年2月27日,Precigen宣布FDA受理其HPV治疗性疫苗PRGN-2012的上市申请并授予优先审评资格,用于治疗复发性呼吸道乳头状瘤病(RRP),PDUFA日期为2025年8月27日。如果顺利获批,PRGN-2012将成为首 款和唯一一款治疗RRP的药物。同时,PRGN-2012也将成为首 款HPV治疗性疫苗。

PRGN-2012为Precigen的首发管线,在其腺病毒载体技术平台AdenoVerse®的基础上开发,抗原为HPV6/11。

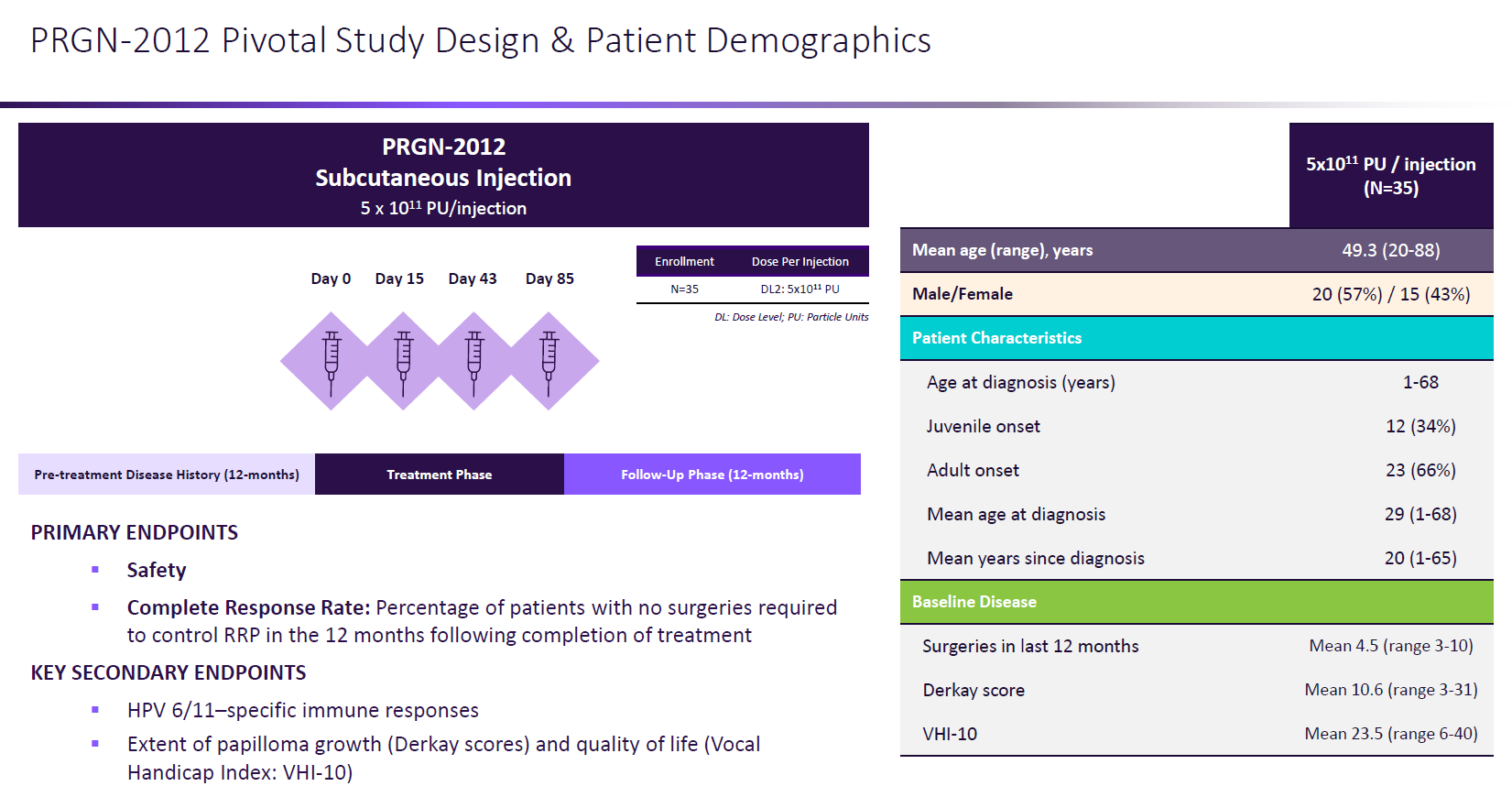
RRP由HPV感染引起,目前没有获批药物,临床上只能通过反复手术切除。
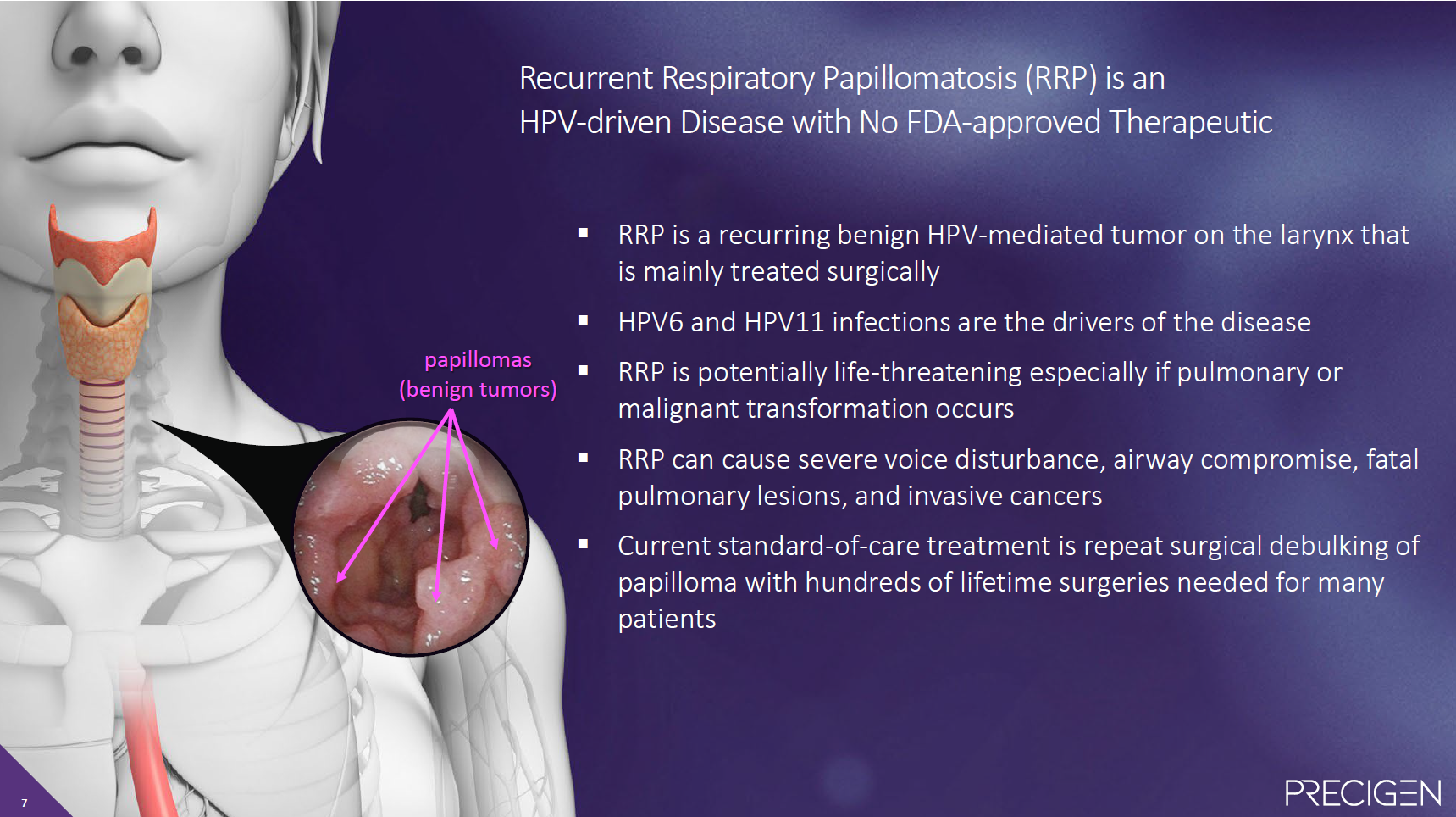
PRGN-2012从2021年开始进入人体临床试验,预计2025年获批上市,仅经过四年临床开发即将推进到商业化阶段。
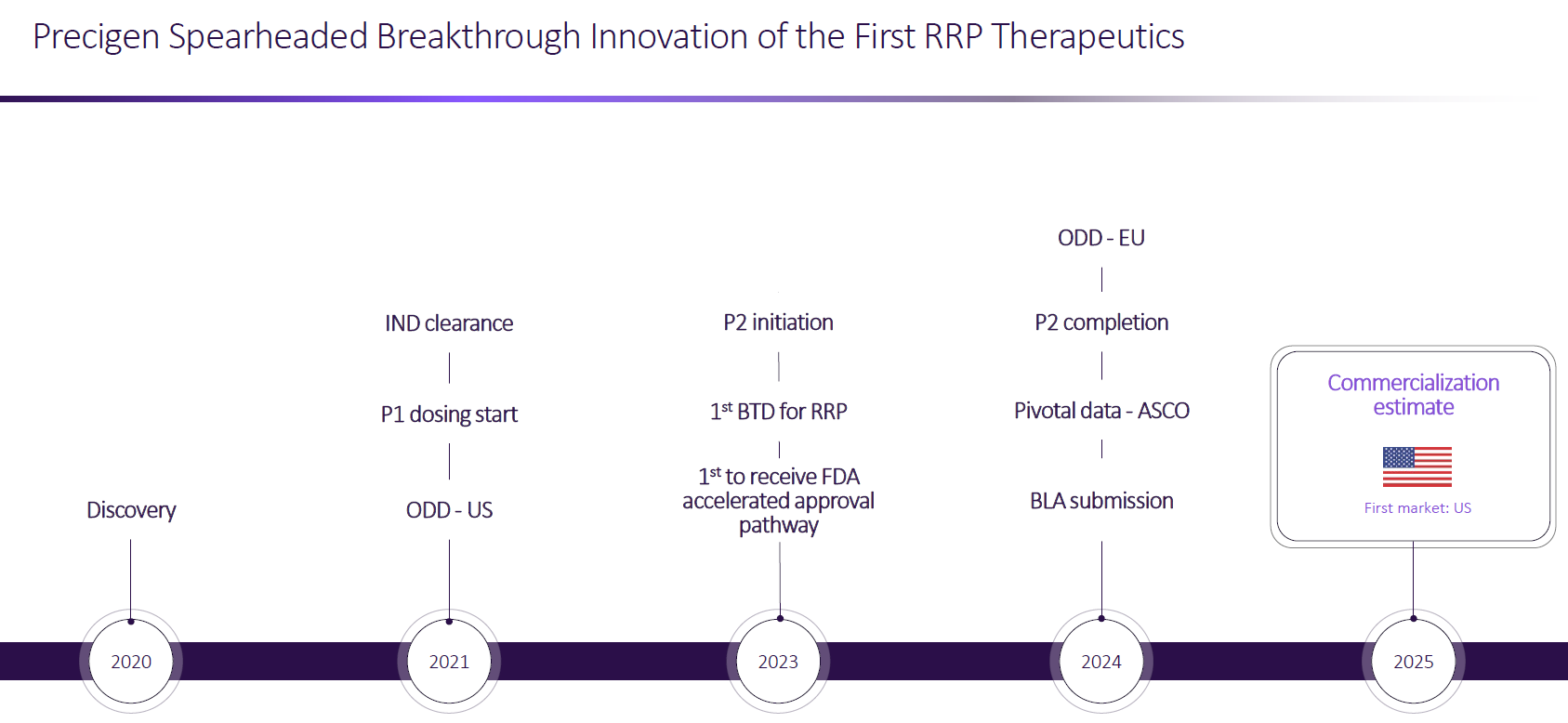
PRGN-2012的作用机制如下,本质上是一种HPV6/11治疗性疫苗。
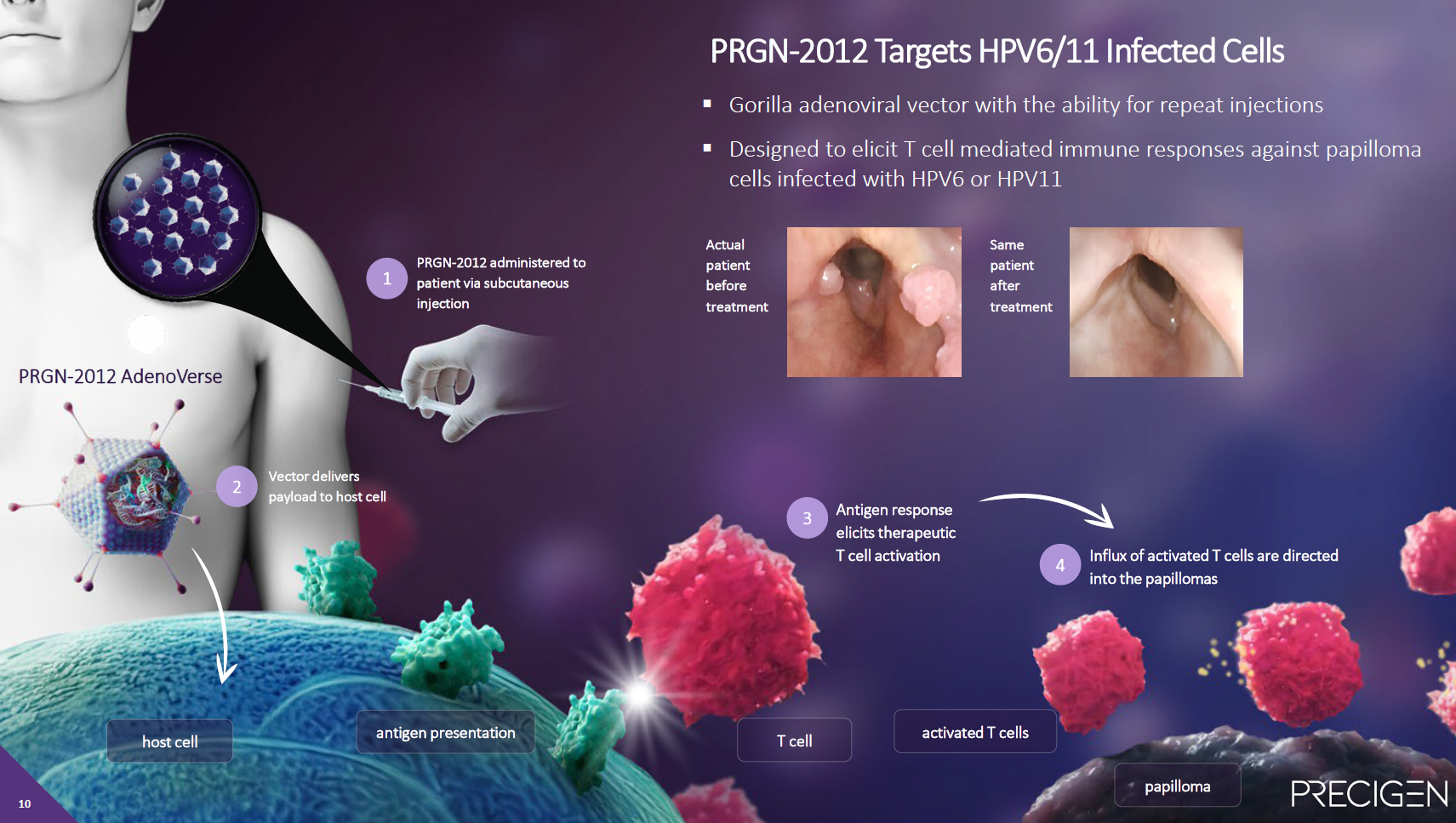
PRGN-2012的关键临床入组35例RRP患者,3个月内完成4次免疫接种。
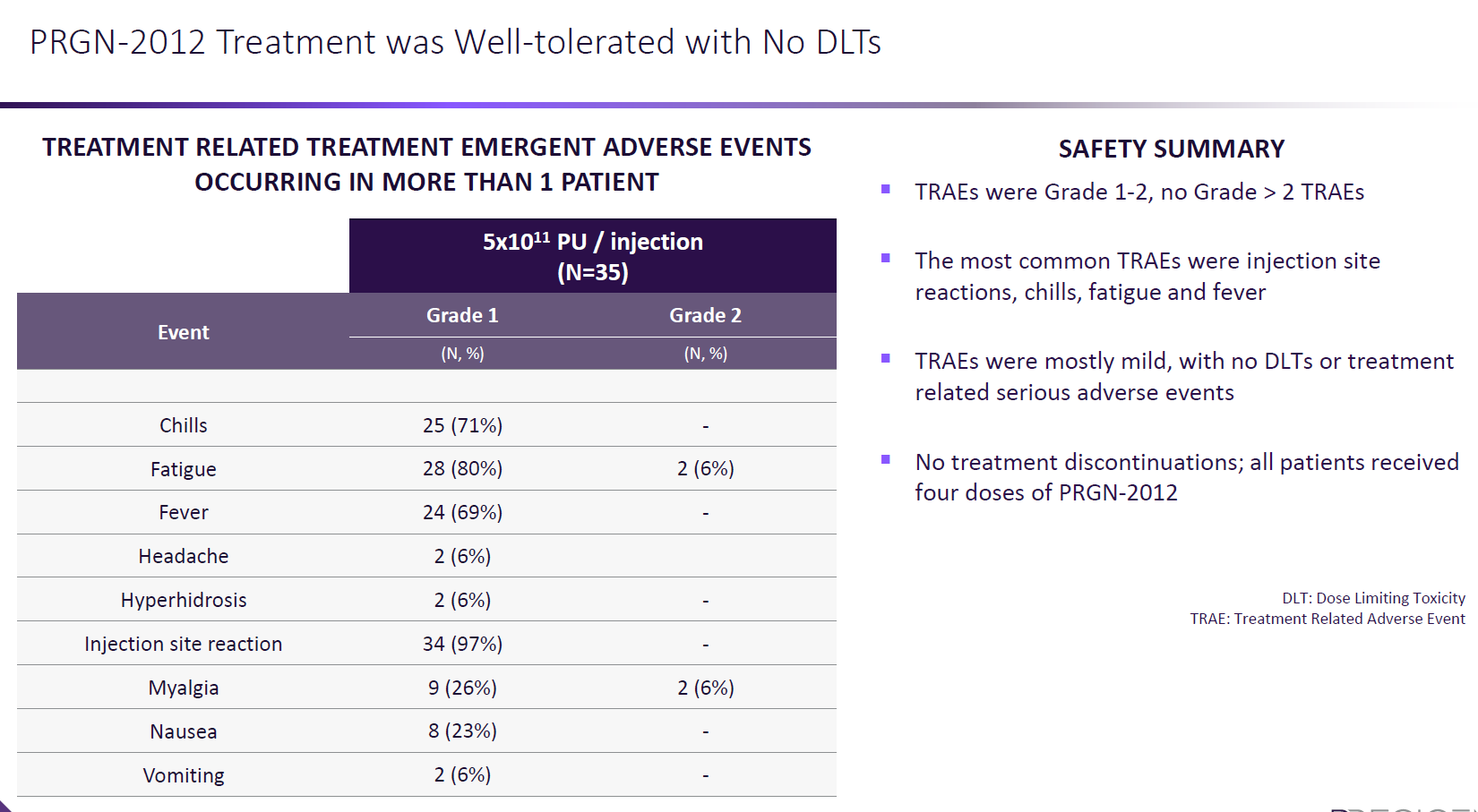
PRGN-2012的安全性良好,仅有1-2级副作用。
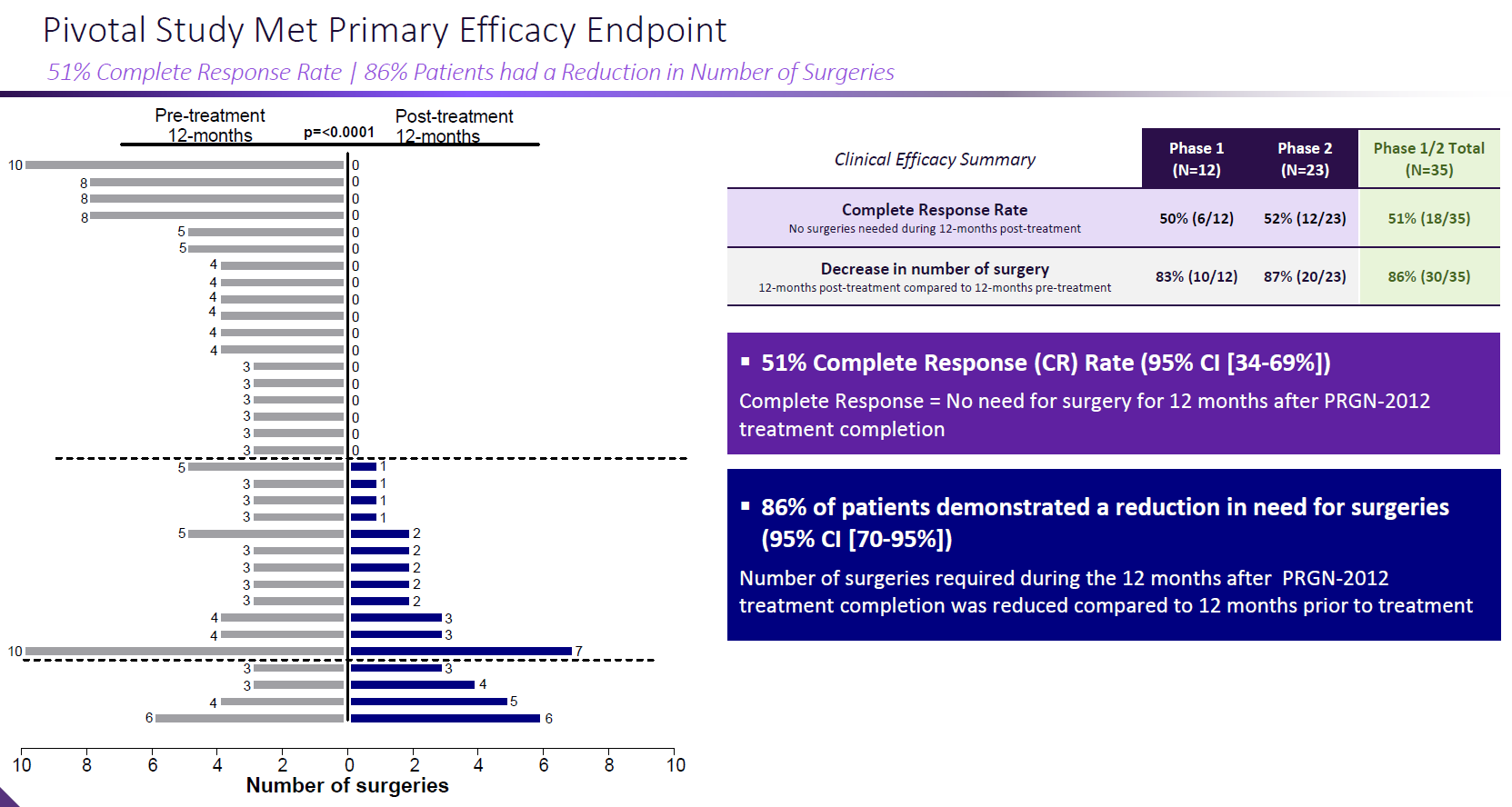
PRGN-2012治疗完全缓解率51%,手术次数下降了86%。
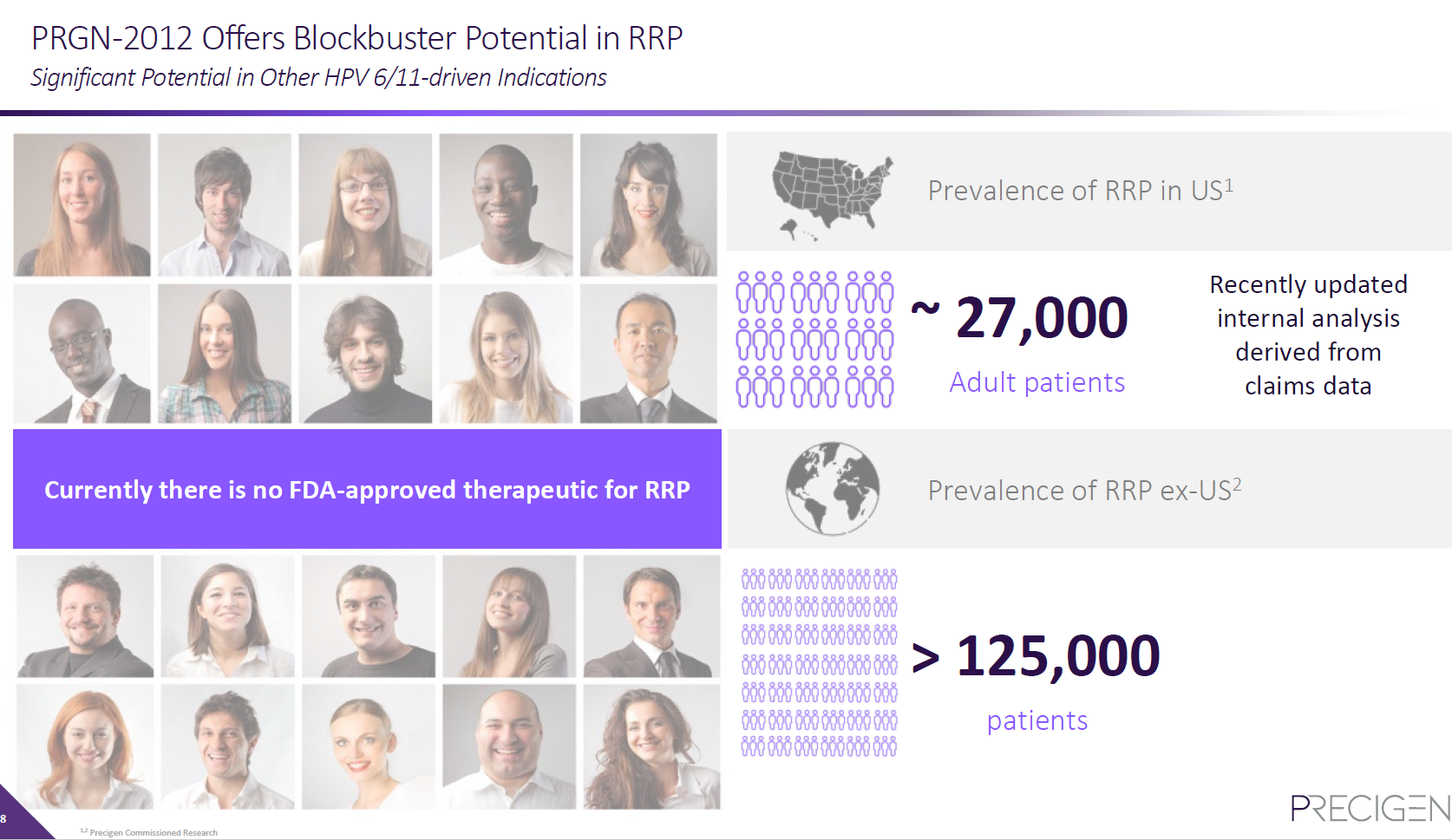
美国的RRP患者超过12.5万例,PRGN-2012有望成长为重磅炸弹药物。
总结
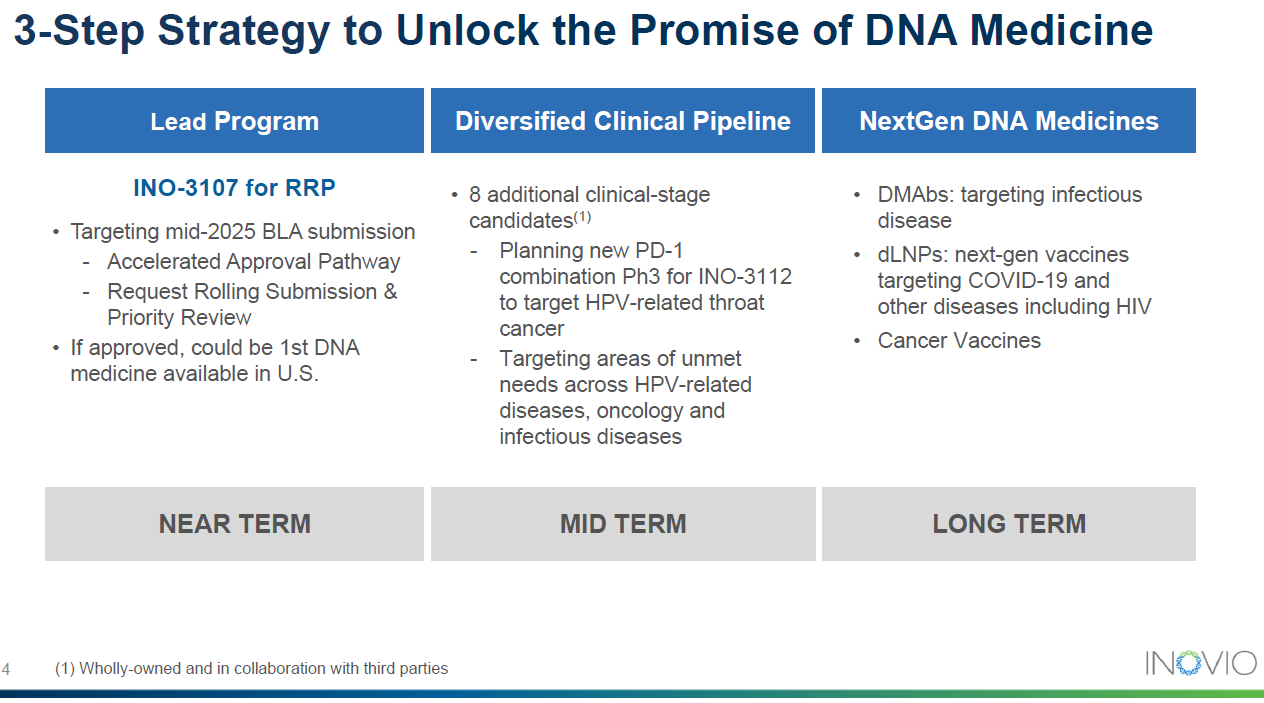
Inovio的HPV DNA疫苗也将在今年中递交RRP的上市申请,HPV治疗性疫苗将进入新时代。国内方面,多家企业布局HPV治疗性疫苗,东方略引进Inovio的VGX-3100,奥罗生物、诺未生物、石药集团、阿法纳生物、仁景生物等的HPV mRNA治疗性疫苗均已进入临床阶段。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57