近日,Beam Therapeutics宣布已经完成了首个体内碱基编辑疗法的概念验证。
此次的主角是BEAM-302,适应症针对的是α-1抗胰蛋白酶缺乏症(AATD),这种疾病通常由SERPINA1基因的G-to-A点突变(Z等位基因)引起,这种突变导致循环M-AAT蛋白水平不足,从而引发肺部疾病;同时,错误折叠的Z-AAT蛋白在肝细胞中聚集,导致肝脏疾病。BEAM-302则能通过CRISPR碱基编辑技术直接修复致病突变(PiZ突变),减少致病的Z-AAT蛋白。
虽然如此,市场反应却呈现出高开低走,消息宣布后,Beam股价一度上涨至36.82美元,但随后下跌14%。
尽管其中或许有大盘走弱的影响,但是其中也凸显出市场对于BEAM-302技术前景的不看好。
体内碱基编辑未必能胜过RNA编辑
在AATD适应症竞争中,目前来看BEAM-302的最大对手是Wave Life Sciences的RNA编辑疗法WVE-006。这是一款通过GalNAc偶联的寡核苷酸靶向mRNA,修复SERPINA1基因的突变的疗法。
与直接体内编辑一次给药不同,WVE-006需多次给药以维持疗效。理论上来说,在给药便捷性方面BEAM-302是存在优势的。
问题可能在于安全性和有效性方面。
去年10月,Wave Life Sciences公布了RNA编辑疗法WVE-006治疗AATD的Ib/IIa期RestorAATion-2研究的积极机制证明数据。
临床试验结果显示,患者血浆中的野生型M-AAT蛋白水平在第15天达到平均6.9µM,占总AAT蛋白的60%以上。重复给药后预计M-AAT水平可能进一步提升。试验第15天时,患者的平均总AAT蛋白水平达到10.8µM,达到了监管机构批准AAT增强疗法的标准。
而虽然此次BEAM-302公布了临床数据,但是没有公布关键的M-AAT蛋白水平数据和占比,没法和WVE-006直接对比,这可能是值得诟病的。
从目前信息来看,BEAM-302的数据更着重强调剂量对于患者体内功能性AAT蛋白水平提升程度。比如说15 mg剂量组提升1.6倍,30 mg组1.9倍,60 mg组2.8倍。
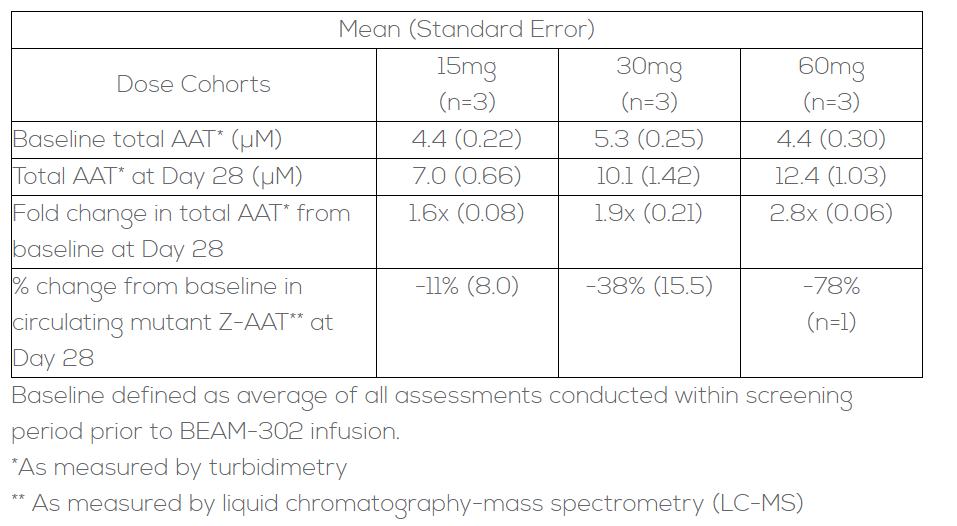
而60mg剂量组中,28天时,总AAT蛋白水平超过了11 µM保护阈值,这种情况下,两者似乎疗效相当,不过BEAM-302是一次性注射,且是高剂量组,而WVE-006可以反复注输,理论上WVE-006能够达到更高的阈值。
同样值得担忧的是安全性问题,随着剂量的攀升,BEAM-302可能迎来安全性困扰。因为这次安全性数据观察到轻度肝酶(ALT/AST)升高。而现在BEAM又打算在60mg剂量组的基础上招募第四个剂量群组,有可能是Beam认为60mg剂量组仍然不足够与WVE-006匹敌。因此需要额外加开剂量组解决问题。随着剂量的攀升,未来是可能出现剂量限制性毒性的。
另外一个问题则有关于适应症的不同分型。
而早先我们提到AATD分为肝和肺两种病症的表征,而这次临床中患者的数据都是来自于肺病患者的,纳入肝病患者的第二部分临床要等到今年之后再启动。届时BEAM-302对于肝功能问题的影响可能更加受到看重。
更多的不可知问题来自于脱靶。早先在临床前数据中,就有观察到BEAM-302存在脱靶问题。这一问题在I/II期临床中尚未解决。
总结
总的来说,BEAM-302的数据还是存在一些问题的。其商业化前景仍取决于更大规模试验的验证,以及与竞品的差异化优势。随着更多数据披露,AATD治疗领域或将迎来分水岭时刻。
参考来源
https://investors.beamtx.com/news-releases/news-release-details/beam-therapeutics-announces-positive-initial-data-beam-302-phase



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57