远端效应(Abscopal effect),是指在肿瘤学中,通过放射治疗对一个肿瘤病灶进行治疗时,未受辐射的远处肿瘤病灶也发生消退现象。这种现象激发了系统性的免疫反应,为放射治疗与免疫治疗的结合——放射免疫治疗,提供了理论基础。
放射免疫治疗具有良好的癌症治疗前景,但其带来的远端效应临床上却极为罕见,这背后的机制目前仍不清楚,阐明放射免疫治疗中远端效应受限的关键机制,有助于改进当前的放射免疫治疗。
2025年3月13日,南方医科大学南方医院董忠谊、吴德华、白雪、官键等人在 Cell 子刊Cancer Cell上发表了题为:PAI-1-driven SFRP2highcancer-associated fibroblasts hijack the abscopal effect of radioimmunotherapy的研究论文。
该研究阐明了放射免疫治疗中远端效应受限的机制,首次揭示了PAI-1 驱动高表达SFRP2的癌症相关成纤维细胞劫持放射免疫治疗的远端效应的机制,填补了放射免疫治疗中基质细胞作用机制的空白,为改善实体瘤免疫治疗效果提供了新靶点和新思路。

在这项最新研究中,研究团队通过全基因组 CRISPR 筛选,发现了SFRP2在癌症相关成纤维细胞(CAF)中高表达,且在放射免疫治疗后未辐射的肿瘤中显著上调。SFRP2 高表达的癌相关成纤维细胞(SFRP2highCAF)通过重塑血管周围免疫抑制微环境,抑制 CD8+T细胞浸润,从而阻碍远端效应。
基因敲除或药物阻断 SFRP2,可显著增强 CD8+T细胞招募,改善未辐射肿瘤的免疫微环境,促进远端效应。
接下来,研究团队通过血清蛋白质组学揭示,经辐射的肿瘤会分泌的PAI-1,通过血液循环到达远端肿瘤,进而通过 LRP1/p65 信号轴触发远处肿瘤周细胞向SFRP2highCAF 的细胞命运转变,形成免疫抑制性的血管周围微环境。
在这些发现的基础上,研究团队发现,使用SFRP2 中和抗体或 PAI-1 抑制剂(PAI-039)可逆转 CAF 的免疫抑制功能,显著增强放射免疫治疗的远端效应。在患者来源的异种移植(PDX)小鼠模型中,靶向 SFRP2 或 PAI-1,有效激活了未辐射肿瘤的免疫应答,验证了该发现的临床转化潜力。
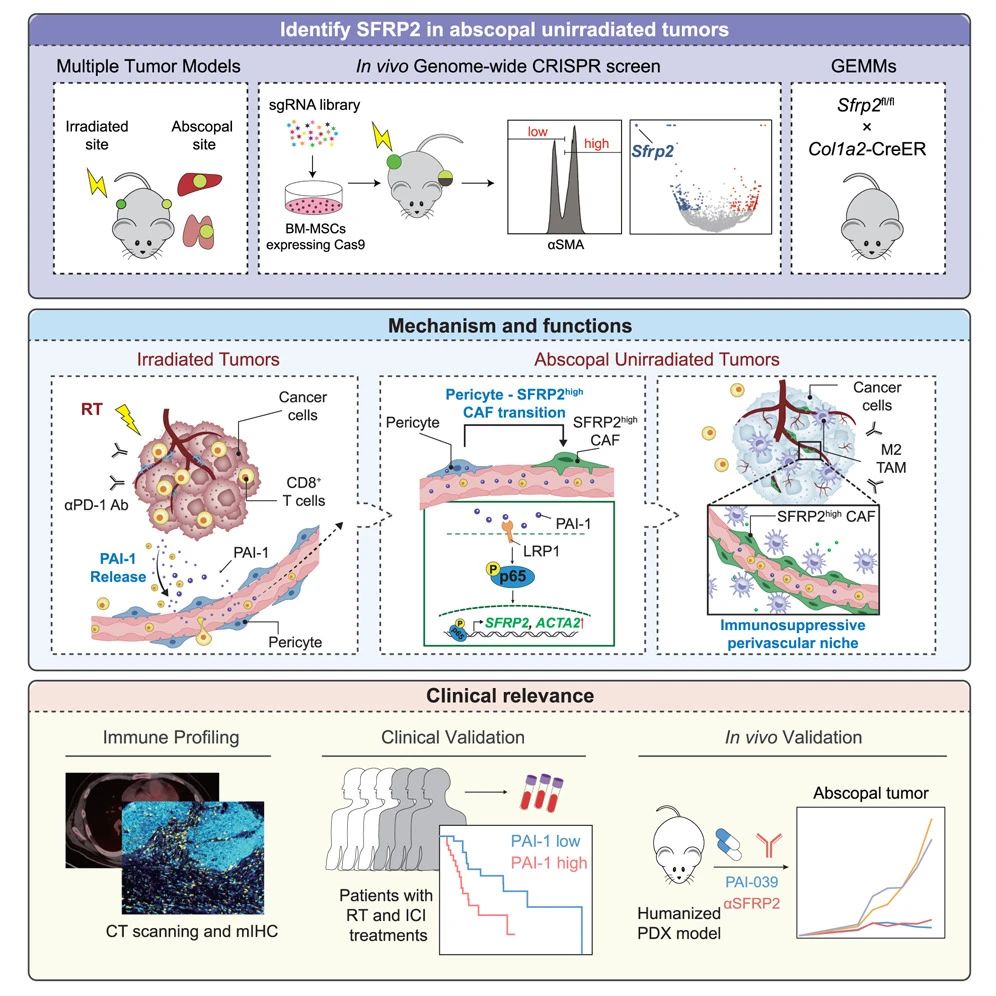
该研究阐明了放射免疫治疗中远端效应受限的机制,首次揭示 PAI-1/SFRP2 信号轴通过周细胞-CAF转化调控远端效应,填补了放射免疫治疗中基质细胞作用机制的空白。该研究还表明了基线 CD8+T细胞浸润水平和 PAI-1 表达可作为预测远端效应的潜在标志物,为改善实体瘤免疫治疗效果提供了新靶点和新思路。
论文链接:
https://www.cell.com/cancer-cell/abstract/S1535-6108(25)00076-5



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57