2025年3月21日,中国国家药监局(NMPA)官网最新公示,联邦制药以注册分类3.3类申报的利拉鲁肽生物类似药上市申请已获得批准。根据联邦生物早先新闻稿,该产品为一款胰高血糖素样肽-1(GLP-1)类似物,本次获批的适应症为糖尿病。
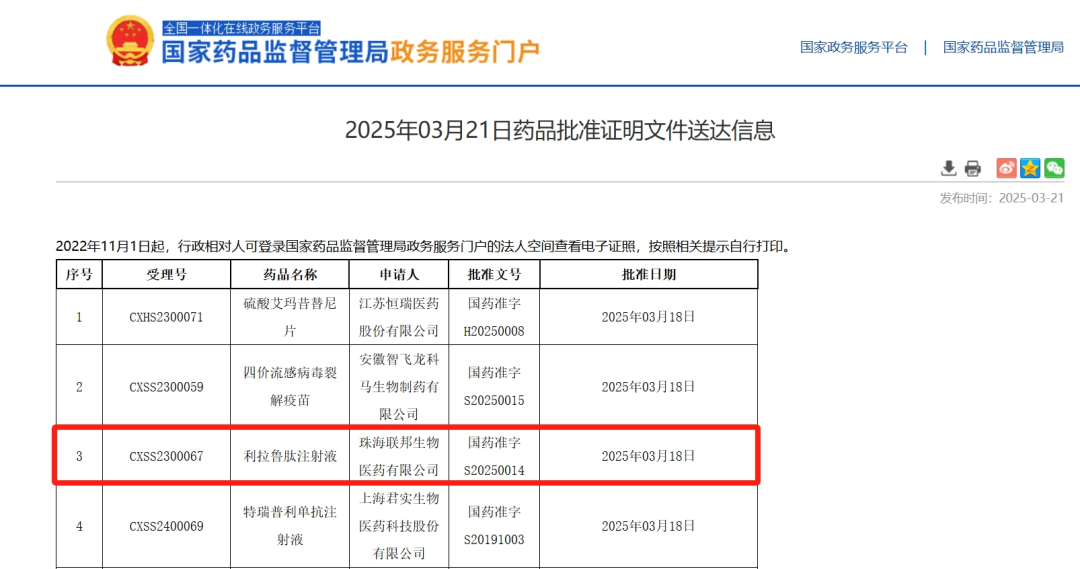
2024年12月,经国家药品监督管理局批复同意,珠海联邦生物医药有限公司及其申报的利拉鲁肽注射液、德谷胰岛素注射液和司美格鲁肽注射液三个品种,成为广东省第一批生物制品分段生产企业和试点品种。利拉鲁肽注射液作为获批分段生产后的首个上市产品,在满足市场需求、提高生产效率与产品质量等方面具有显著优势,也将为国内的生物制品分段生产积累宝贵的实践经验。
关于利拉鲁肽注射液
利拉鲁肽注射液是一种人胰高血糖素样肽-1(GLP-1)类似物,适用于成人2型糖尿病患者控制血糖;单用二甲 双胍或磺脲类药物最大可耐受剂量治疗后血糖仍控制不佳的患者,与二甲 双胍或磺脲类药物联合应用;降低伴有心血管疾病的2型糖尿病成人患者的主要心血管不良事件(心血管死亡、非致死性心肌梗死或非致死性卒中)风险。一天注射一次即可有效控制血糖。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57