三阴性乳腺癌(TNBC)有着转移率高、预后差、患者生存率低等特征,是最 具侵袭性和最致命的乳腺癌亚型,其缺乏雌激素受体(ER)和孕激素受体(PR),以及人表皮生长因子受体2(HER2)这几个乳腺癌治疗靶点,也因此得名。
免疫检查点抑制剂与化疗药物的联合疗法是三阴性乳腺癌(TNBC)的标准治疗方案。然而,许多患者对治疗产生抵抗,且起初对治疗有反应的患者仍有可能肿瘤复发,这表明存在获得性耐药机制,但我们对这些机制目前仍知之甚少。
2025年3月28日,贝勒医学院张翔团队在 Immunity 期刊发表了题为:Tumor-derived arachidonic acid reprograms neutrophils to promote immune suppression and therapy resistance in triple-negative breast cancer 的研究论文。
该研究揭示了一种癌细胞与中性粒细胞相互作用介导的癌症耐药新机制——肿瘤来源的细胞外囊泡通过其携带的花生四烯酸重编程中性粒细胞,从而促进三阴性乳腺癌的免疫抑制和治疗耐药。

在这项最新研究中,研究团队发现,三阴性乳腺癌(TNBC)细胞在抗 PD-1 疗法和化疗治疗后存活下来,会积累中性脂质。而干扰癌细胞中脂滴的形成可逆转耐药性并减轻免疫抑制微环境。单细胞 RNA 测序揭示了一部分中性粒细胞表现出与相邻肿瘤细胞相似的脂质丰富表型。
从机制上来说,肿瘤来源的携带花生四烯酸(arachidonic acid,AA)等脂质的细胞外囊泡(EV)介导了中性粒细胞的重编程。
阻断饮食中的 ω-6 脂肪酸的摄入或抑制花生四烯酸合成的脂肪酸延长反应,可恢复抗肿瘤免疫,并使耐药肿瘤重新对抗 PD-1 疗法和化疗敏感。此外,研究团队还发现,在人类患者中,花生四烯酸代谢相关通路与中性粒细胞富集相关。
该研究的核心发现:
● 免疫检查点阻断疗法(ICB)和化疗耐药的三阴性乳腺癌细胞表现出脂质积累增加;
● 脂质积累与花生四烯酸(AA)合成增加有关。
● 癌细胞来源的花生四烯酸使肿瘤中性粒细胞使更具免疫抑制性;
● 重编程的中性粒细胞通过增加前列腺素 E2(PGE2)和 PD-L1 来抑制 CD8+ T 细胞。
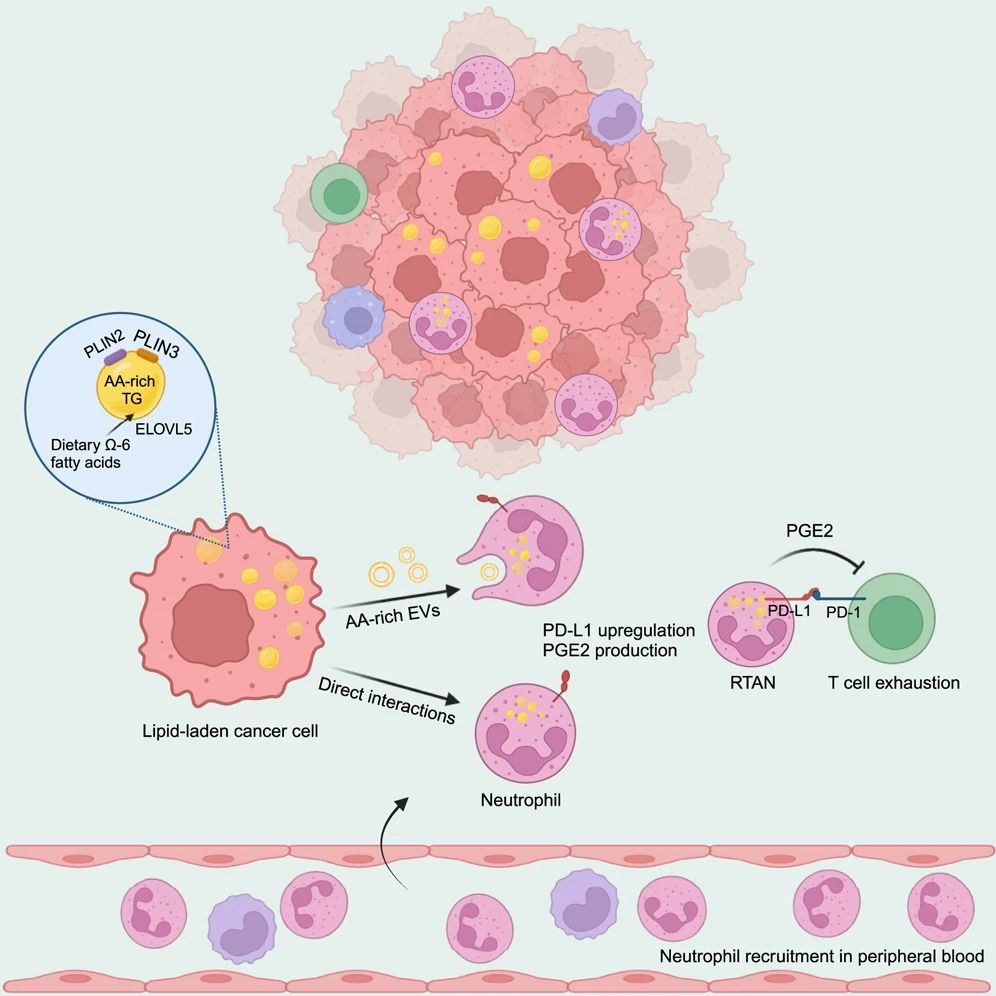
总的来说,这项研究揭示了三阴性乳腺癌(TNBC)细胞来源细胞外囊泡通过其中携带的花生四烯酸重编程中性粒细胞,从而促进了三阴性乳腺癌的免疫抑制和治疗耐药。
论文链接:
https://www.cell.com/immunity/abstract/S1074-7613(25)00096-2



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57