肥胖已成为全球范围内的重大公共卫生问题,尤其在中年人群(30-49岁)中,其发病率呈现显著上升趋势。更为严峻的是,中年肥胖患者的死亡风险显著高于其他年龄段的肥胖人群。尽管这些临床观察结果已引起广泛关注,但中年人群对肥胖的易感性及其背后的分子机制仍亟待探索。
近日,华中科技大学王从义教授、成都市第三人民医院刘雁军教授及山西白求恩医院刘师伟教授团队合作,在 Nature 子刊 Nature Communications 上发表了题为:Adipose progenitor cell-derived extracellular vesicles suppress macrophage M1 program to alleviate midlife obesity 的研究论文。
该研究发现,脂肪祖细胞(APC)来源的细胞外囊泡(EV)通过调控巨噬细胞 M1 极化,减轻中年肥胖。

该研究首先发现,中年小鼠在高脂饮食(HFD)诱导下更容易发生肥胖,且其白色脂肪组织(WAT)中的脂肪祖细胞功能显著下降。进一步联合 RNA-seq 和单细胞测序分析发现,中年脂肪祖细胞(APC)分泌的细胞外囊泡(EV)中 miR-145-5p 含量显著减少,导致这些 EV 无法有效抑制脂肪组织巨噬细胞(ATM)向 M1 型极化。M1 型巨噬细胞的增加进一步加剧了脂肪组织炎症反应及胰岛素抵抗,最终导致肥胖发生。
研究团队进一步探讨了 miR-145 调控巨噬细胞 M1 极化的机制。通过 RNA-seq 分析,团队发现 miR-145 能够显著抑制 L-选择素(SELL)的表达,而 SELL 是调控巨噬细胞 M1 极化的关键分子。SELL 通过激活 NF-κB 信号通路,促进 M1 巨噬细胞的极化和炎症因子的分泌。miR-145 通过抑制 SELL 的表达,阻断了 NF-κB 信号通路的激活,从而抑制了 M1 巨噬细胞的极化。
为了将上述发现转化为临床应用,研究团队设计了靶向递送 miR-145 的阳离子脂质体(miR-145@tar-lip),并将其注射到中年小鼠体内。结果显示,miR-145@tar-lip 能够显著抑制脂肪组织巨噬细胞(ATM)的 M1 极化,减轻脂肪组织炎症反应,并有效预防中年小鼠的肥胖。这一发现不仅揭示了 APC 来源的 EV 在中年肥胖中的关键作用,还为临床治疗中年肥胖提供了新的潜在靶点。
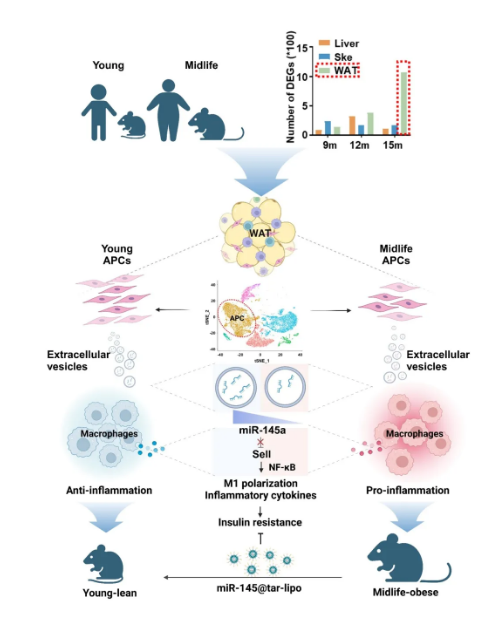
总的来说,这项研究不仅揭示了中年肥胖的新机制,还为临床治疗提供了新的思路。通过靶向递送 miR-145,可以有效抑制脂肪组织巨噬细胞(ATM)的 M1 极化,减轻脂肪组织的炎症反应,从而预防和治疗中年肥胖。此外,研究团队开发的 miR-145@tar-lip 脂质体具有高效靶向性和良好的生物相容性,为未来的临床应用奠定了基础。
华中科技大学王从义教授、成都市第三人民医院刘雁军教授、山西白求恩医院刘师伟教授为论文共同通讯作者,华中科技大学周庆博士、高佳博士、吴国娆博士及美国贝勒医学院王晨玮博士为论文共同第一作者。
论文链接:
https://www.nature.com/articles/s41467-025-57444-y



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57