
ACHIEVE-1研究结果将在第85届ADA科学会议上发布,并发表在同行评审的期刊上。预计今年年底前将发布ACHIEVE研究 3期临床试验项目的更多结果,以及orforglipron用于体重管理的ATTAIN 研究3期临床研究结果。礼来预计将在今年年底前向全球监管机构提交orforglipron用于体重管理的上市申请,预计于2026年提交其用于治疗2型糖尿病的上市申请。
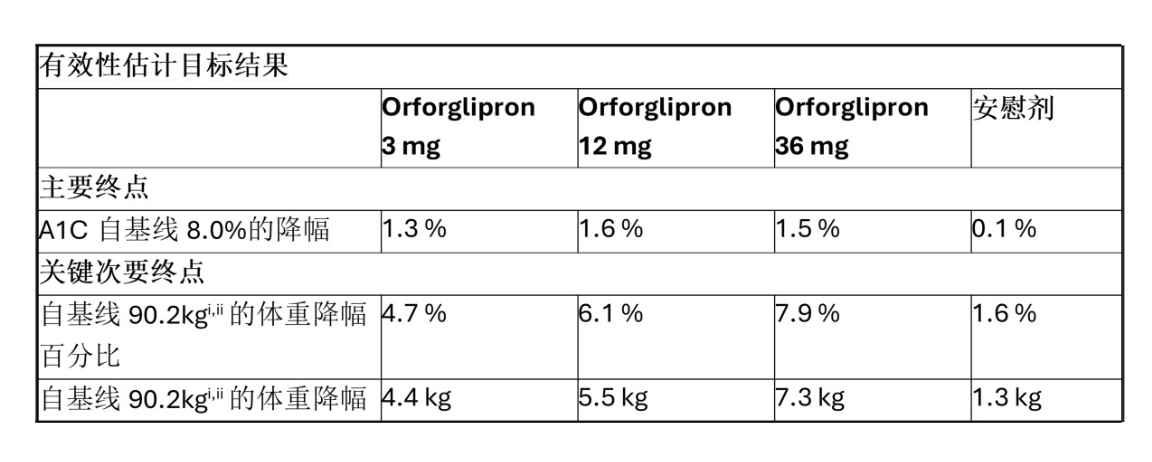
根据治疗方案估计量分析,所有剂量的orforglipron均显著降低患者的A1C水平。在体重变化的关键次要终点方面,12 mg和36 mg剂量也带来了统计学显著的减重效果。
A1C降低幅度:1.2%(3 mg)、1.5%(12 mg)、1.5%(36 mg)、0.4%(安慰剂)
体重减轻百分比:4.5%(3 mg)、5.8%(12 mg)、7.6%(36 mg)、1.7%(安慰剂)
体重减轻数值:4.2公斤(9.3磅;3 mg)、5.2公斤(11.5磅;12 mg)、7.2公斤(15.8磅;36 mg)、1.5公斤(3.4磅;安慰剂)
在ACHIEVE-1研究中,orforglipron的整体安全性特征与GLP-1类药物的既有安全性一致。最常见的不良事件与胃肠道相关,且大多为轻度至中度。Orforglipron组(3 mg、12 mg和36 mg)的常见不良事件包括:腹泻(19%、21%、26%,对比安慰剂9%)、恶心(13%、18%、16%,对比安慰剂2%)、消化不良(10%、20%、15%,对比安慰剂7%)、便秘(8%、17%、14%,对比安慰剂4%)和呕吐(5%、7%、14%,对比安慰剂1%)。因不良事件导致的治疗中断的比例分别为6%(3 mg)、4%(12 mg)、8%(36 mg),对比安慰剂为1%。未观察到肝脏安全性信号。
关于Orforglipron
Orforglipron是一种在研的、每日一次的口服小分子(非肽类)胰高血糖素样肽 – 1受体激动剂(GLP-1 RA)。该药物可在全天任何时间服用,对饮食或饮水不加以限制。5该药物由中外制药(Chugai Pharmaceutical Co., Ltd.)发现,并于2018年授权至礼来制药开发。中外制药与礼来共同发表了这一分子的临床前药理学数据。6目前,礼来正在进行orforglipron用于治疗2型糖尿病,以及用于肥胖或至少伴有一种体重相关合并症的超重成人进行体重管理的3期研究。此外,礼来还在研究orforglipron作为治疗肥胖成人的阻塞性睡眠呼吸暂停和高血压的潜在疗法。
关于礼来制药
礼来制药是一家致力于通过科学创新改善人类健康水平,惠及全球患者的医药公司。作为医疗健康行业的领军者,礼来制药拥有近150年的历史。今天,我们的药物已帮助全球数千万人。运用生物技术、化学和基因医学的力量,我们的科学家正在积极推动新的医学进展,以应对严峻的全球健康挑战。重新定义糖尿病与肥胖疗法,减少肥胖对人体的长期影响;助力阿尔茨海默病的防治行动;为一系列威胁人类健康的免疫性疾病提供解决方案;以及将难以治愈的癌症转变为可控的疾病。礼来制药迈向健康世界的每一步,都源自于我们“致力于让数百万患者生活得更美好”的信念。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57