2017年02月23日,来那度胺原研厂家celgene宣布,FDA已扩大批准Revlimid(来那度胺)10mg胶囊的新适应症,用于多发性骨髓瘤患者接受自体同源干细胞移植(auto-HSCT)后的维持治疗,这也使得来那度胺成为FDA批准的唯一一个自体同源干细胞移植后的维持控制药物,事实上,2017年01月,欧盟下属的人用医药产品委员会(CHMP)同样给出积极建议,推荐批准来那度胺作为auto-HSCT术后的维持用药,这对于来那度胺市场地位的巩固具有重要意义,文章关注超级重磅炸 弹来那度胺的逆袭成长之路,并对此次适应症扩展背后的核心数据予以了适当的解读。
一."度胺"药物的洗白:从臭名昭著的沙利度胺到"重磅炸 弹"来那度胺
说到"度胺",也许很多人第一个想到的并不是来那度胺而是臭名昭著的沙利度胺,这个世界上10000多个家庭的噩梦。1954年,沙利度胺(又称反应停)曾被广泛应用于孕期孕吐的治疗,然而事实证明药物具有非常严重的致畸作用,能够导致婴儿短指崎形(海豹儿),因此该药物于1961年被全面禁售,世界范围内10000名海豹儿也成为受害者和家庭的一大负担,事件成为医药界一个臭名昭著的负面典型,自此之后,药物不良反应,尤其是特殊**受到前所未有的关注,药物安全性的评价体系得到极大的完善。

研究发现,虽然沙利度胺具有非常严重的致畸型倾向(这里的致畸是针对孕妇),然而药物在某些疾病的控制中显示出非常惊喜结果,例如,沙利度胺在麻风性结节性红斑、多发性骨髓瘤治疗中疗效显著,此文来那度胺便是沙利度胺经过结构改造而得到的(如下图),有效降低了药物的不良反应,来那度胺自2005年12月批准用于多发性骨髓瘤以来,已经完成完美逆袭,华丽转身为响当当的重磅炸 弹级药物,市场表现令人惊叹。
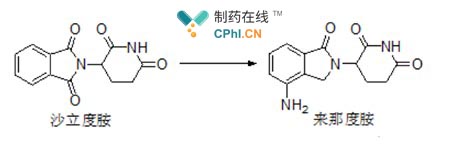
截至目前,Celgene公司研发的来那度胺已经有数个适应症获批临床(总结如下表)
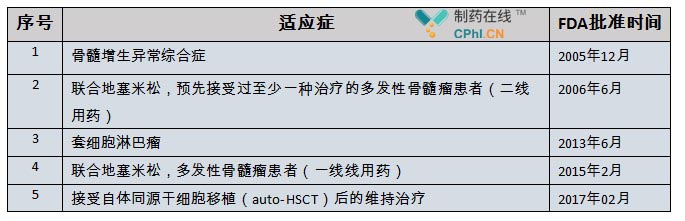
来那度胺上市以来,销售业绩逐步攀升,已经成长为一款重磅炸 弹级药物,并逐步成为多发性骨髓瘤领域内的绝对霸主。笔者也曾撰文《强生多发性骨髓瘤新药升级之旅正式开启Darzalex三联疗法获EMA积极建议》分析了来那度胺在多发性骨髓瘤市场中的优势地位,来那度胺销售数据也是一路飘升,fiercepharma,evaluatepharma对该药物的的未来销售预期给予相当积极的评价。
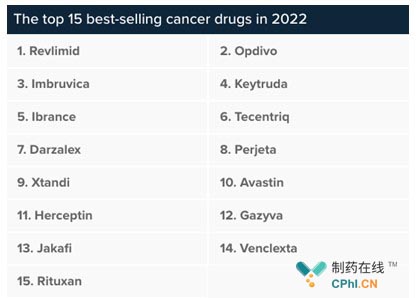
二.来那度胺新适应症获批 重磅炸 弹药物继续发力
《2016年最火爆药物top50 修美乐一骑绝尘 获5冠王》文章中曾经对比分析了全球 top50的畅销药,来那度胺成为top10中为数不多的一款小分子药物,而此次来那度胺新适应症获批将会进一步巩固其市场地位。事实上,来那度胺的新适应症获批是基于两项针对接受自体同源干细胞移植的患者(autologous stem cell transplant,ASCT)III期临床试验的核心数据,笔者总结如下:
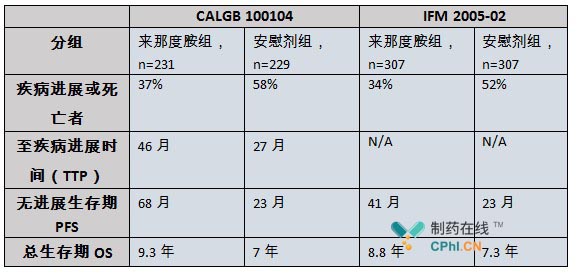
来那度胺在接受自体同源干细胞移植的患者控制中显示出优势,极有可能成为标准疗法,来那度胺的一步步升级同时也必将造福患者。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57