目前,中国是一个仿制药大国,中国本土企业生产的药品中约有97%为仿制药。而在临床实践中,不可避免的,国产仿制药和原研药在疗效等方面存在较大差异。
因此,就出现了一致性评价,意在提高仿制药审评标准,减少低质量供给。
一致性评价就等效原研,有争议
由于专利药的制剂工艺都是保密的,仿制药只能根据处方组成和给药途径来自行进行工艺研究,这会导致仿制药和原研药疗效和安全性的差异。
比如,以某个治疗勃起功能障碍的西药为例,其原研药和国产仿制药之间,就存在着一些差异。
药物崩解度,药物崩解度就是溶解度,会直接影响药物被人体吸收的程度。在实验中,人体胃液正常条件下,国产仿制药的崩解远远慢于原研药。
药物溶出度。这是药物溶出进入人体的过程,这个指标受生产流程的操作、辅料质量与含量的差异,压片过程中的设计和包衣的影响。国产仿制药溶出速度比原研药慢三到四倍。
药物活性成分的纯度。国产仿制药所含杂质较多,这有可能导致药物的活性以及药物功能降低,也许会产生副作用和潜在的“**”。
为了提高质量,对杂乱的仿制药市场进行规范,一致性评价出现了。
而业界有一种观点:通过一致性评价,也许仍然无法达到完全和原研药一致。
对此,北大第一医院的张志超教授在辉瑞的“西地那非原研与仿制研讨会”上提出:“就像生活中有人住五星级酒店,有人住三星级酒店,有人住快捷酒店一样,仿制药也有高仿,中仿和低仿。”
但在评价的相关指标中,就像奥迪和奥拓一样,可能在跑80迈的时候,你是看不出什么区别。因此,应该以更细分的标准,让药在临床评价中表现出差异,这样会鼓励更多的人做高仿。
张志超教授认为,就药监局而言,一致性评价的指标是合格的,但它可能只能限制某些主要指标,无法细分到更具体的领域——有些东西是无法量化的。
比如评价一个钉子,你只能评价这个钉子的“压强”,“能穿透多少东西”,但这个东西“好使不好使”,只有你自己知道。
在赛柏蓝之前的文章《过了一致性就能替代原研?!呵呵呵呵呵呵呵》中,张勇也表示过:我国的一致性评价主要指标是生物等效性,而实际上生物等效性并不等于临床等效性,甚至可以说其和临床有效性是有差距的。
据张志超教授所言,大型的三甲医院的医生更倾向于开进口原研药,因为疗效更有保证。
通过评价仿制药就能替代原研,不见得
那么,即使通过一致性评价的药品,也无法和原研比肩吗?
另一种观点认为:不见得。
事实上,如今的创新药大国美国也同样经历了这个阶段。1984年,美国颁 布《药品价格竞争和专利期恢复法》(Hatch-Waxman 修正案),创造了仿制药现代审批体系,规定了仿制药无需重复原研药的一系列临床试验,仅需证明仿制药与参照药品的生物等效性。此法案是现代仿制药工业的里程碑。
温州医科大学药学院药理学教授朱新波曾对《光明网》表示:在大多数常规情况下,通过一致性评价的仿制药是可以替代原研药使用的。只有在“病情危急的患者用药,血液病、心脑血管疾病中病情不易控制的患者,老年人、儿童、孕妇等高危患者群体”的情况下,需要谨慎的用仿制药来替代原研药。
无独有偶,一位教授7月7日在珠江论坛上谈到一致性评价,提到这样一个观点:一致性评价要做到:药效等效性+生物等效性=治疗等效性,此时的治疗等效性可以与临床等效性对等。
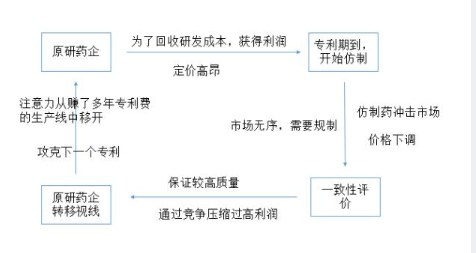
赛柏蓝的读者也提出了这样一个逻辑:一致性评价有助于营造一个通过竞争压缩高利润,促进创新的良性循环。
况且,从标准和政策支持上,一致性评价也一直在进步。
从企业的角度,为了通过一致性评价,企业需要大量的人力、时间和资金成本,来进行质量攻关、工艺改进和技术提升。为此,地方政府通过发布补助政策来支持本地区的企业通过仿制药一致性评价,主要是有现金补偿、销售额补偿等形式:给予企业50~600万不等的的现金,的是安徽亳州,补助600万;通过一致性评价后按照销售额大小设定补助金额,比如阜阳,销售额达到1000万给予30万补助。
从评价指标的角度,一致性评价涉及到大量的工作程序和技术性细节,其中有参比制剂的确定、整体工作程序、临床试验的要求等指标,CFDA也在不断提高效率,提供更为标准的技术规范和操作,制定评价标准和评价方法。据秦脉咨询统计,自仿制药一致性评价启动以来,CFDA先后发布了近30个技术指导原则和相关技术标准文件,对于企业开展研究起到了较好的技术支撑作用。
做好仿制药,要有匠人**
据慧博资讯,目前,共有65个品规正式通过一致性评价,其中,有57个品种通过补充申请完成一致性评价,有8个品规通过其他路径完成一致性评价。一致性评价申请和审批端进入加速期,支持政策陆续执行,其业绩兑现也即将到来。
通过一致性评价的品种将不断享受着利好时点:立刻在各省挂网采购;招标中和原研一组,具有绝对的价格优势,通过一致性评价的药品更有可能凭借低价抢占原研的市场份额。
如今,通过一致性评价的药品正在慢慢蚕食着原研的市场份额。而它是否能真正替代原研,还需要仿制药企的相关动作以及国家监管的不断完善。
正如张志超教授所言:中国是完全有能力制造出优质仿制药的,只是需要我们有匠人**,态度认真一点,工艺做的更精细一点。
与此同时,到了后仿制药一致性评价时代——即使通过了一致性评价,但生产过程中原辅料和包材等因素均可能对质量产生较坏的影响,使产品质量波动;此时,加强监管,积极修订和补充相关标准就显得格外重要。另外,还要保持一致的审评尺度,不能因为一致性评价的期限将至而前松后紧
这样,只有仿制药在疗效上实现一致,又不会因为其他指标的不合格而带来副作用,减少风险,才有可能真正实现对原研的替代。
原标题:仿制药无法替换原研,谁说的?



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57