2018年10月10-12日,德国柏林召开多发性硬化症2018 ECTRIMS年会,会议上公布多项备受关注的多发性硬化症临床研究进展,主要包括:1. Teva公布Copaxone® -25年长期安全性数据;2. 诺华公布Gilenya® VS Copaxone®头对头临床数据;3. Celgene公布ozanimod最新临床分析数据;4. 罗氏公布OCREVUS最新临床进展等。笔者将在这篇文章中汇总重要的临床数据。
一. 多发性硬化症与疾病修正治疗(DMT)
笔者在前文(接力芬戈莫德 诺华多发性硬化症药物siponimod上市申请获受理)中提到,多发性硬化症(multiple sclerosis, MS)是一种罕见的自身免疫性疾病,分为复发缓解型(RRMS,85%)、原发进展型(PPMS 10%)和进展复发性(PRMS, 罕见型5%),其中,80% RRMS可进展为申请适应症为继发进展型多发性硬化症(SPMS)。
#多发性硬化症:分型

数据来源:ALTAS OF MS 2013
#流行病学:全球患者230万,发病率0.5-3‰
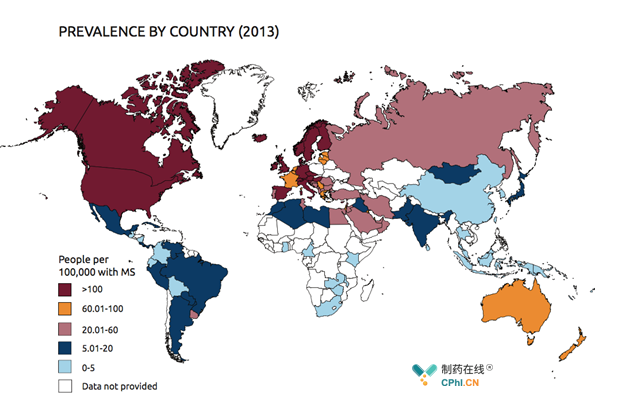
数据来源:ALTAS OF MS 2013
#疾病修正治疗(DMT)
多发性硬化症尚无有效的根治疗法,临床上仍旧以疾病修正治疗(Disease-modifying treatments ,DMT)为主,下图为目前临床上已上市的主要DMT治疗药物。本文暂不对比各治疗药物的用药方案和适应症。
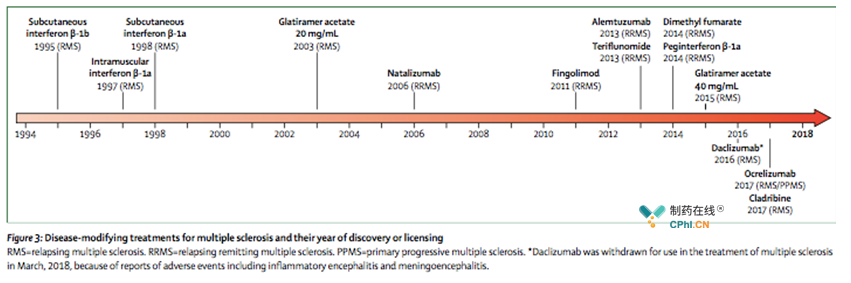
数据来源:Multiple sclerosis
#患者可用的多发性硬化症资源
1. 多发性硬化症国际联合会
https://www.msif.org/#
2. 多发性硬化症社区
https://www.mssociety.org.uk
3. 中国多发性硬化症权威科普性网站
暂无,笔者尚未查到
二.2018 ECTRIMS: 多发性硬化症开发进展汇总
1. Teva重磅产品COPAXONE® 发布25年长期安全性数据
Teva重磅产品COPAXONE®长期占据多发性硬化症市场销售冠军,是公司一款非常重要的资产,Teva日前公布COPAXONE® 发布25年长期安全性数据。
关于开放标签extension study
该临床试验为COPAXONE注册临床试验的扩展试验,患者完成36月、随机、安慰剂对照注册临床试验后,COPAXONE组和安慰剂组患者均开始服用开放标签的COPAXONE,目前,Teva已发布该扩展临床的2年,3年,6年,8年,10年,15年和20年安全性和有效性数据。
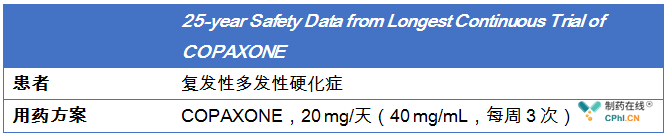
2. 诺华Gilenya® vs Copaxone®头对头临床数据:Gilenya®显示出优效性
Copaxone®和Gilenya®均是多发性硬化症市场中的重磅产品,2017年销售额位列第2,3。诺华该项头对头临床试验 ASSESS study (NCT01633112)旨在对比Copaxone®和Gilenya®在RRMS患者中的安全性和有效性。
#ASSESS study (NCT01633112)
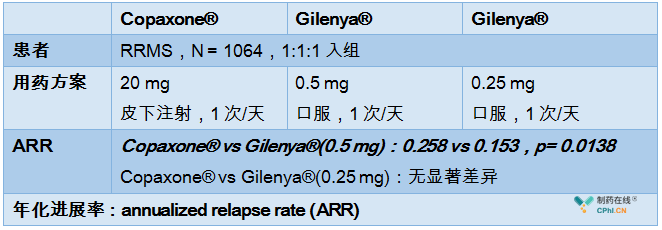
Gilenya 0.5mg可使患者1年复发进展率降低40.7%,同时,Copaxone® vs Gilenya®(0.5 mg),ARR 分别为0.258 vs 0.153,p= 0.0138,显示出优效性。
ASSESS study对于Gilenya具有重要的意义,这是首个Copaxone® vs Gilenya®头对头临床试验数据,Gilenya® 0.5 mg显示出优效性。
3. S1P受体调节剂临床进展
Ozanimod
# SUNBEAM™- NCT02294058
SUNBEAM™是一项多中心、随机、双盲、安慰剂/标准疗法对照的关键3期临床,,评估1 mg/0.5 mg ozanimod HCI 在RMS患者中的安全性和有效性。
# RADIANCE™ Part B- NCT02047734
RADIANCE Part B is一项多中心、随机、双盲、 标准疗法对照的关键3期临床,评估1 mg/0.5 mg ozanimod HCI 在RMS患者中的安全性和有效性。
SUNBEAM™-post hoc analysis of 12-month data
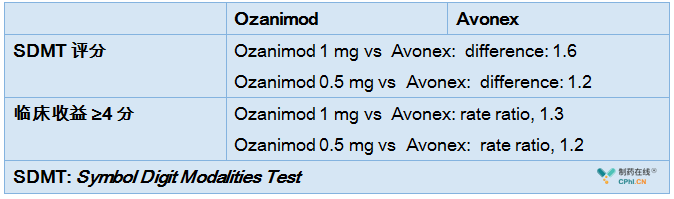
A second post hoc analysis on annualized relapse rates (ARR) and MRI lesions
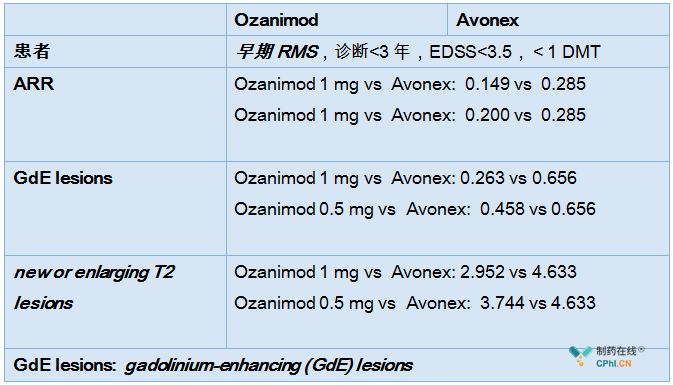
Celgene的S1P受体调节剂Ozanimod同样是另一款值得关注的多发性硬化症药物,是诺华两款S1P受体调节剂的一个强力竞争者,但是由于药物上市进程遭遇挫折,药物的市场预期大打折扣。
Siponimod临床数据详见(接力芬戈莫德 诺华多发性硬化症药物siponimod上市申请获受理)
4. 罗氏多发性硬化症新星OCREVUS (Ocrelizumab)
获批用于PPMS和RRMS,1年用药两次,罗氏这款OCREVUS (Ocrelizumab)是一颗冉冉升起的新星,这款"准重磅炸 弹药物"OCREVUS™正在开启多发性硬化症治疗的一个新时代。
该结果源自OPERA I, OPERA II扩展临床5年数据
该结果显示,相比早期使用INF beta-1α或安慰剂,早期OCREVUS可延缓患者致残进展,并具有优效性。
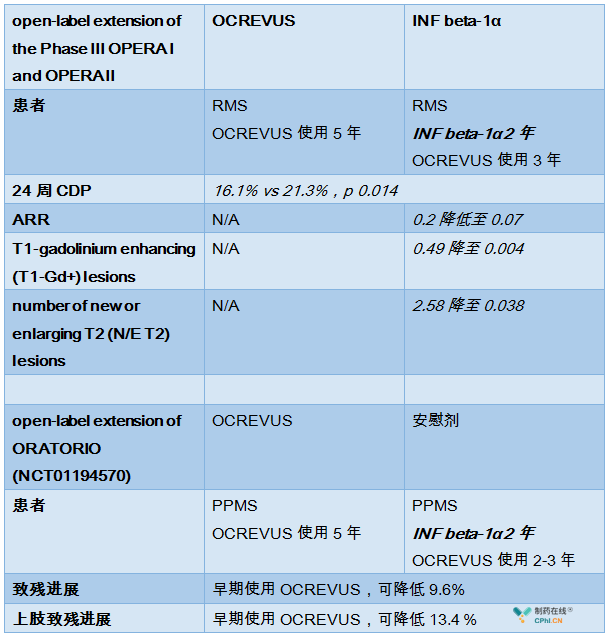
数据能够表明PPMS和RRMS患者尽早开始使用OCREVUS具有确证性的临床收益,罗氏同时还公布Phase IIIb CHORDS数据以及ORATORIO的 post-hoc analysis 数据,这里不再展示,post-hoc analysis详情可参考https://onlinelibrary.wiley.com/doi/10.1002/ana.25313
2018 ECTRIMS中,除了上述进展外,TG Therapeutics公布ublituximab进展,默克公布Evobrutinib研究进展等。以上多发性硬化症临床进展中,COPAXONE®,Gilenya,Ocrevus的数据相当吸引人,这其中,单克隆抗体药物Ocrevus更是备受关注,该药物是一颗冉冉升起的明星药物。笔者希望在下一篇文章中,分析多发性硬化症市场中各产品的市场份额,并对各款药物的适应症和用药方案。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57