2019年05月04日-10日,美国神经学(American Academy of Neurology, AAN) 年会正在美国费城召开,SMA,多发性硬化症、偏头痛等领域,均有多个产品开发进展有更新,本文关注口服偏头痛药物rimegepant。 Biohaven称将于2019Q2递交该药物上市申请,并使用优先审评券,预计领先ubrogepant成为全球首款获批上市的口服CGRP受体拮抗剂。本文主要介绍其BHV3000-303和BHV3000-201临床进展,同时,简单总结2019年偏头痛领域内最为值得关注的产品开发进展!
一.Biohaven:rimegepant更新BHV3000-303和BHV3000-201数据
rimegepant是Biohaven一项重磅资产,主要开发2种剂型,即常释片剂和速释片剂,拟开发用于偏头痛治疗和预防。
2019 AAN,rimegepant主要有两项更新,分别为:BHV3000-303临床数据和BHV3000-201 长期安全性数据。这两项数据均是支持rimegepant上市申请的重要数据基础。
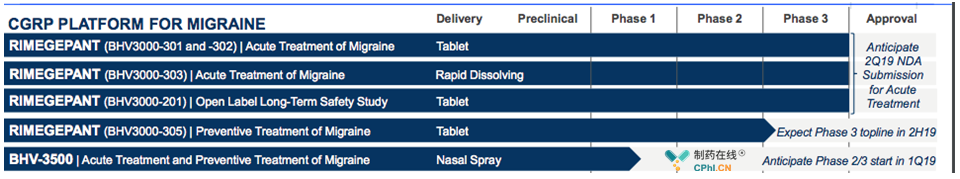
Biohaven官网
Study 303 (BHV3000-303):
BHV3000-303: Phase 3, Double-Blind, Randomized, Placebo Controlled, Safety and Efficacy Trial of BHV-3000 (Rimegepant) Orally Disintegrating Tablet (ODT) for the Acute Treatment of Migraine
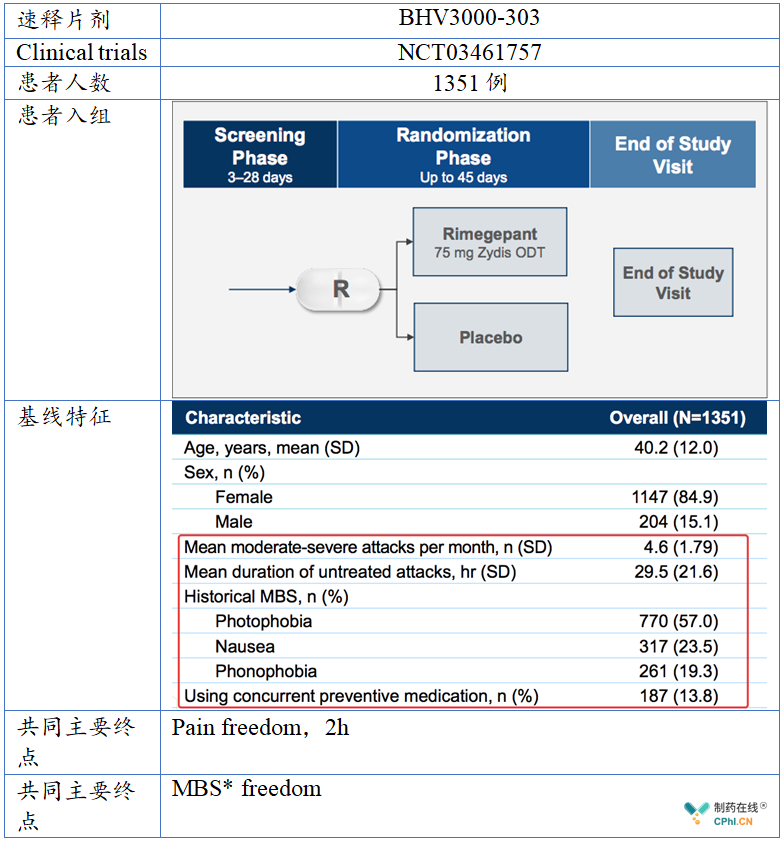
*most bothersome symptom, 如Photophobia, Phonophobia or Nausea.
Rimegepant 75 mg, Zydis ODT达到主要临床终点:
临床数据显示:
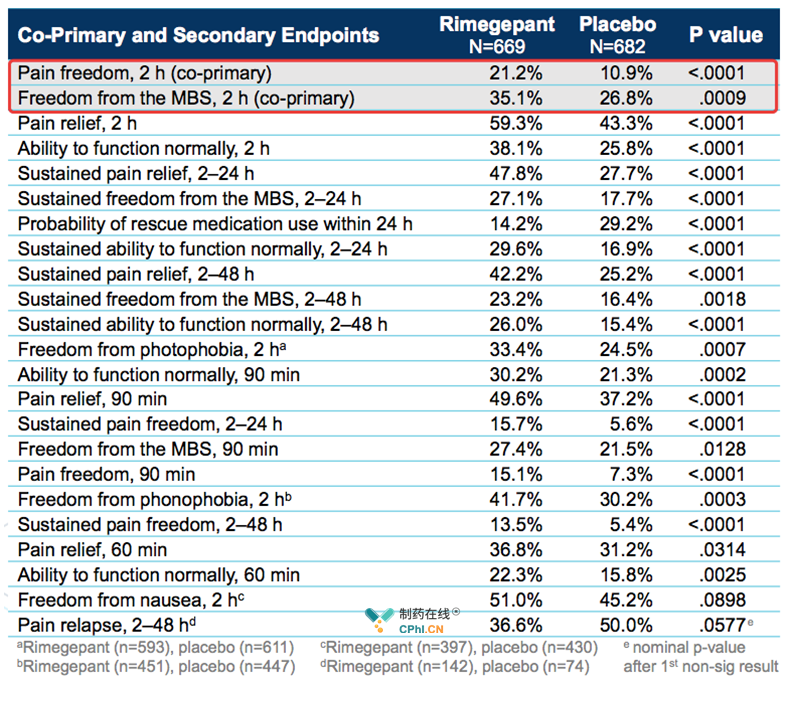
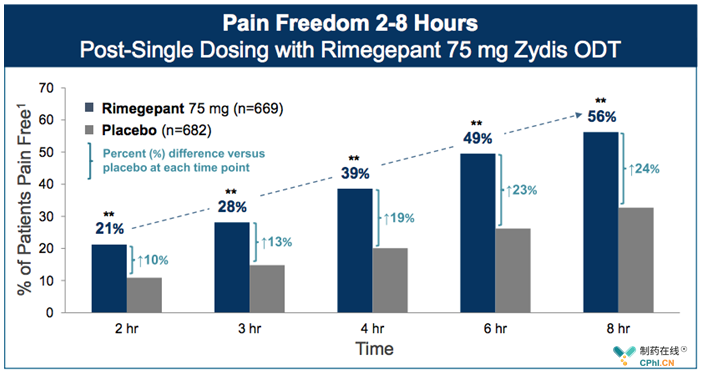
rimegepant 75 mg, Zydis ODT能够有效给偏头痛患者带来持续的临床收益,药物服用15min开始起效,同时能够给患者带来持续的症状缓解。
BHV3000-201长期安全性的初步临床数据
Evaluate the long-term safety of rimegepant 75 mg with up to daily dosing for 1 year
AS-NEEDED (PRN only): Patients with 2 to 14 moderate to severe migraine attacks per month prior to screening were assigned to rimegepant 75 mg PRN for up to 52 weeks FIXED-DOSING (QOD+PRN): A cohort with 4 to 14 moderate to severe migraine attacks per month were assigned to rimegepant 75 mg QOD for up to 12 weeks supplemented by PRN dosing on nonscheduled dosing days
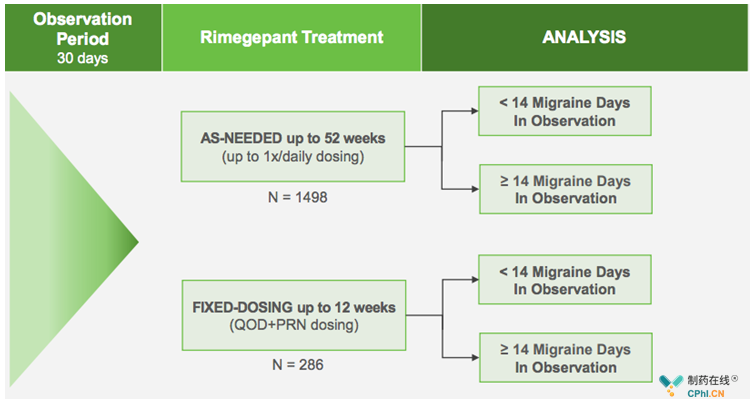
PRN: 必要时
QOD: 隔日一次
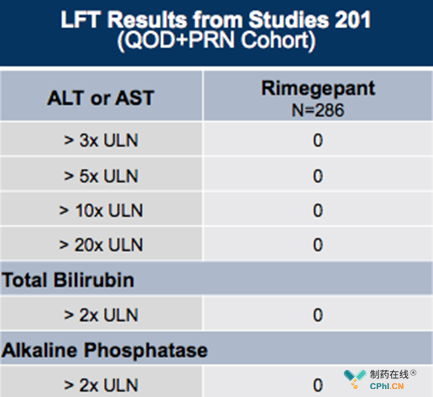
结果显示,rimegepant具有良好的安全性和耐受性
QOD+PRN 亚组中:因不良反应终止患者比例仅为3.1%,ALT/AST水平3*ULN 患者比例为0.
二.全球偏头痛重要产品管线开发进展
2018年全球首款CGRP单抗获批上市以来,偏头痛治疗迎来里程碑式突破,截至目前,全球已有3款CGRP单抗获批上市。其中,2018年09月14日,fremanezumab获批用于偏头痛预防性治疗,药物成为全球第2款获批上市的CGRP单抗,2018年全球销售额为490万美元,2019年销售额预计可达到1.5 亿美元。
2019年04月23日,Teva官方更新CGRP单抗项目Ajovy (fremanezumab) 开发进展,3期临床ENFORCE数据分析显示,试验大概率无法达到临床终点,Teva决定放弃fremanezumab丛集性头痛的开发。Teva对外宣布,fremanezumab将会继续开发创伤后头痛适应症,目前该临床试验(NCT03347188)处于2期,后续值得持续关注!
最近,Allergan 已经向FDA递交全球首款口服CGRP受体拮抗剂Ubrogepant上市申请;另外,FDA已经受理Alder BioPharmaceuticals的CGRP单抗eptinezumab上市申请;Biohaven更是花费1.05亿美元从GW Pharmaceuticals购买一张优先审评券,力保rimegepant成为全球首个口服偏头痛药物。
2019年以来,偏头痛领域内多款产品开发又有新的进展,总结如下表:
偏头痛重要产品开发进展汇总:
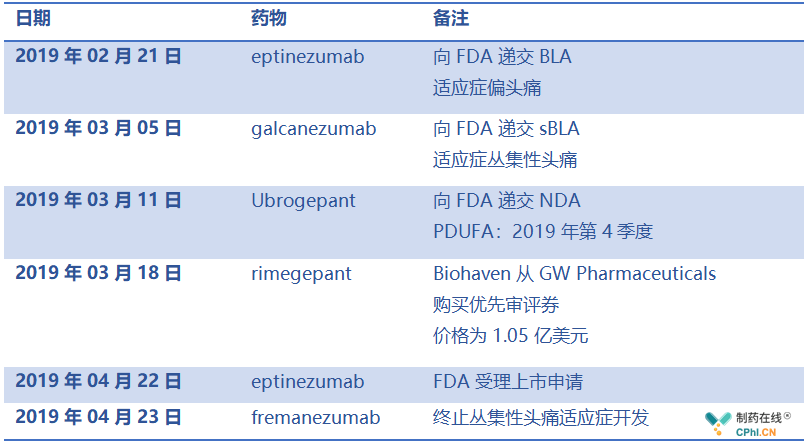
2019年,依然可期,例如,全球第4款CGRP单抗将会获批上市;2019年09月,礼来Emgality将会完成首个适应症拓展,获批用于丛集性头痛;2019年第4季度,全球首款口服CGRP受体拮抗剂将会获批上市,但是到底是Rimegepant,还是Ubrogepant ?敬请期待。
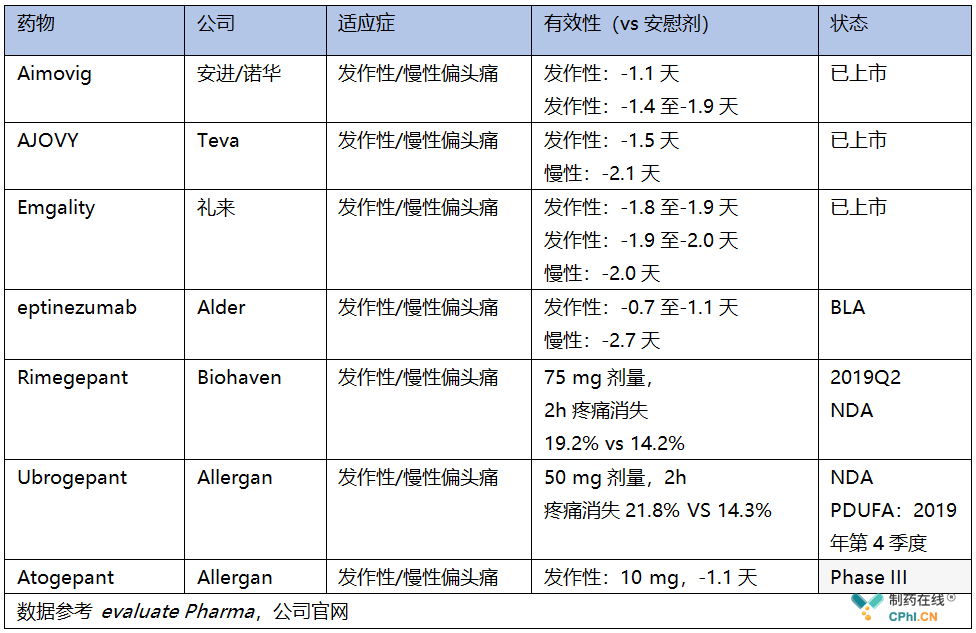
CGRP单抗或受体拮抗剂的开发和获批上市给偏头痛患者带来突破性创新疗法,笔者根据公开信息,整理出下表,口服小分子药物或是单抗药物均给患者带来临床获益,笔者同样和大家一样期待更多创新疗法的获批。
偏头痛重要产品关键临床试验数据总结:
参考资料:
各公司官方网站
点击下图,观众预登记成功送20元话费



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57