
9月26日,FDA将对Darzalex(daratumumab)联合标准护理(硼替佐米+来那度胺+低剂量地塞米松,VTd)一线治疗适合自体干细胞移植(ASCT)的多发性骨髓瘤(MM)患者的补充生物制品许可申请(sBLA)作出审查决定。若顺利通过,Darzalex将再次斩获MM治疗领域又一个一线疗法适应症,并给强生带来新的增长动力。
相关阅读:《 正大天晴PK扬子江!谁能拿下年销$20.4亿的多发性骨髓瘤重磅药泊马度胺首仿》
Darzalex是全球获批的首个针对肿瘤浆细胞表面的CD38分子、人源化免疫球蛋白IgG1单克隆抗体,具有广谱杀伤活性,通过多种免疫介导的作用机制诱导肿瘤细胞的快速死亡,包括互补依赖性细胞毒作用(CDC)、抗体依赖性细胞介导的细胞毒作用(ADCC)和抗体依赖性细胞吞噬作用(ADCP)以及通过细胞凋亡(apoptosis)。而且,Darzalex也被证明能够靶向肿瘤微环境中的免疫抑制细胞而表现出免疫调节活性。
Darzalex最初由丹麦药企Genmab研发的,2012年强生通过签署11亿美元的协议从Genmab获得其全球独家权利,作为强生大力开发的一款产品,除了MM,Darzalex也有潜力治疗高表达CD38分子的其他类型肿瘤,包括弥漫性大B细胞淋巴癌(DLBCL)、慢性淋巴细胞白血病(CLL)、急性淋巴细胞白血病(ALL)、浆细胞性白血病(PCL)、急性髓性白血病(AML)、滤泡性淋巴瘤(FL)和套细胞淋巴瘤(MCL)等。在今年1月份,百时美施贵宝(BMS)与强生达成战略合作,调查PD-1免疫疗法Opdivo联合Darzalex治疗血液学恶性肿瘤和多种实体瘤,包括多发性骨髓瘤(MM)、非小细胞肺癌(NSCLC)、胰 腺癌、结直肠癌(CRC)、三阴乳腺癌(TNBC)和头颈部癌。
Darzalex自2015年上市以来,已经在MM治疗领域斩获了多项适应症,从最初的四线疗法扩大到一线疗法,详见下文:
2013/05 FDA授予daratumumab治疗MM的突破性药物资格。
2015/11 作为一种单药疗法,用于既往已接受至少3种疗法治疗的MM患者(四线疗法)。
2016/11 Darzalex联合来那度胺和地塞米松,或硼替佐米和地塞米松,用于既往接受过至少一种疗法的MM患者(二线治疗)。
2017/06 Darzalex联合泊马度胺和地塞米松,用于既往已接受2种疗法(包括来那度胺和蛋白酶体抑制剂)治疗的MM患者(三线疗法)。
2017/11 Darzalex强生旗下的杨森制药向FDA提交Darzalex联合硼替佐米(bortezomib)、马法兰(melphalan)及泼尼松(prednisone),用于治疗不适合自体干细胞移植(ASCT)的新诊MM患者的补充生物制品许可(sBLA)。
2018/05 Darzalex联合硼替佐米(bortezomib)、马法兰(melphalan)及泼尼松(prednisone),用于不适合进行自体干细胞移植(ASCT)的新诊MM成人患者(一线疗法)。
2019/03 强生向FDA提交Darzalex联合硼替佐米(bortezomib)、沙利度胺(thalidomide)及地塞米松一线治疗符合自体干细胞移植(ASCT)条件的新诊多发性骨髓瘤(MM)患者的补充生物制品许可(sBLA)。
强生向FDA提交Darzalex联合来那度胺和地塞米松一线治疗不符合ASCT条件的新诊MM患者的补充生物制品许可(sBLA)。
Darzalex自上市以来,2016年到2018年的销售额就逐年递增(详见下表),但2018年增长速率已明显低于2017年。不过随着在MM领域一线疗法的获批,预计Darzalex在2019年的表现也将不俗,目前上半年的销售额就已达到14.03亿美元。而且今年7月份NMPA也已有条件批准daratumumab注射液的进口注册申请,用于单药治疗复发和难治性多发性骨髓瘤成年患者(包括既往接受过一种蛋白酶体抑制剂和一种免疫调节剂且最后一次治疗时出现疾病进展的患者),而且在欧洲市场上也在拓展适应症,估计2019年Darzalex全球销售额可以轻轻松松突破30亿美元。著名EvaluatePharma曾预测Darzalex2024年全球销售额有望达到60.33亿美元,且有分析师指预测Darzalex有机会突破100亿美元。

关于多发性骨髓瘤及其治疗药物
多发性骨髓瘤(MM)是以骨髓中浆细胞异常增殖为特征的血液恶性肿瘤,仅有25%的患者接受化疗后生存期在5年以上,其发病率仅次于非霍奇金淋巴瘤,是第三大常见血液肿瘤,全世界每年新增病例约114,000例。MM治疗方法包括化疗、放疗、骨髓移植和支持治疗等。
近年来,随着诊疗技术及药物研发的迅猛发展,治疗MM的药物也有了很大的变化,目前FDA已经批准了多款新型治疗MM的药物,主要包括4大类,分别是蛋白酶抑制剂(如硼替佐米、卡非佐米、伊沙佐米)、免疫调节剂(如来那度胺、沙利度胺、泊马度胺)、单抗类药物(如Daratumumab 、Elotuzumab)和组蛋白脱乙酰酶抑制剂(如帕比司他),详见下表:
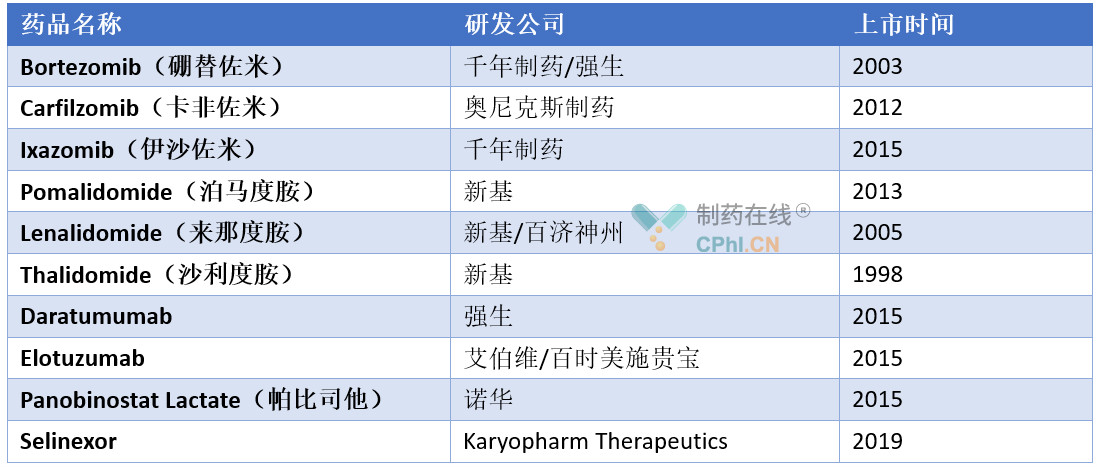
上述药物中,来那度胺、泊马度胺和Daratumumab可谓是MM治疗领域的重磅炸 弹,2018年的全球销售额分别为96.85亿美元、20.4亿美元和20.25亿美元,顺利进入2018年全球药品销售额TOP100。相信随着对各个药物研究的深入,MM领域的市场竞争将会更加激烈。
参考资料:
[1]Janssen Seeks Expanded Use of DARZALEX (daratumumab) Combination Therapy for Newly Diagnosed, Transplant Eligible Patients with Multiple Myeloma
[2] Janssen Submits Application to U.S. FDA to Expand Indication for DARZALEX®(daratumumab) Combination Therapy for Patients with Newly Diagnosed Multiple Myeloma who are Transplant Ineligible



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57