2019年11月14日,百济神州创新药泽布替尼(商品名BRUKINSA)获得FDA批准,适应症复发/难治性套细胞淋巴瘤(Mantle Cell Lymphoma),CTR20160888是支持泽布替尼获批上市的注册临床试验。
泽布替尼创造多个纪录,快速通道、突破性疗法、优先审评,3个月便加速批准,泽布替尼美国获批上市具有里程碑意义,同时开启泽布替尼全球化一个新的起点!
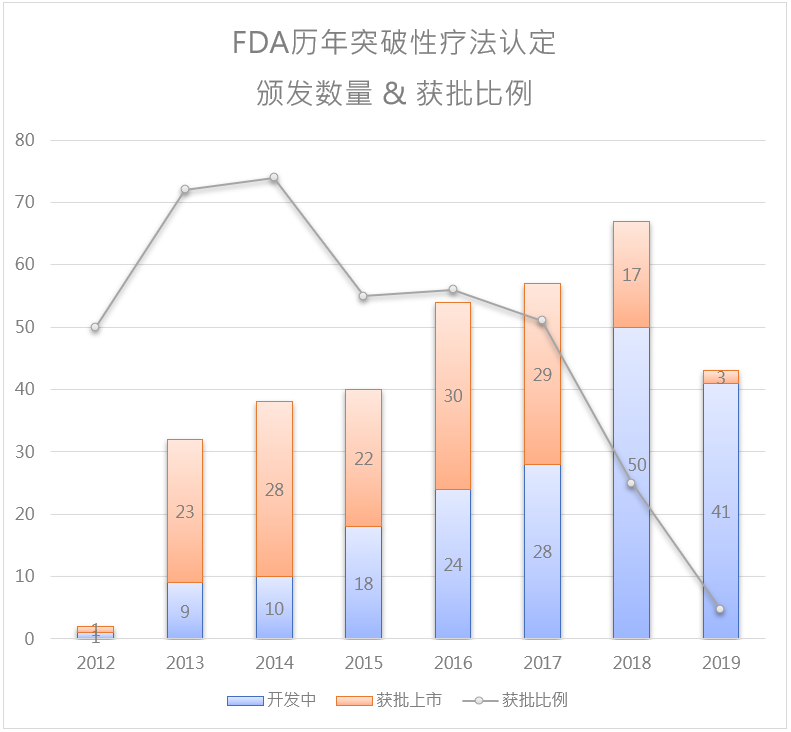
有一项统计数据,创新药开发平均耗费10亿美元,平均耗时10年,平均成功率< 10%。根据美国FDA的Breakthrough Therapy Approvals [1],friends of cancer research以及笔者平时的积累,FDA颁发了333项突破性疗法认定,其中151项获批,药物获批的概率从<10% 飙升至45%!毫无疑问,突破性疗法认定药物完全打破了这一规则,泽布替尼再次印证突破性疗法是药物获批上市方向标!
泽布替尼(赞布替尼,BGB-3111)是一款BTK抑制剂,首个获FDA突破性疗法认定的中国自主研发抗癌新药,药物对BTK靶点抑制持久、专一,可带来深度的缓解和良好的安全性!
本文关注泽布替尼复发/难治性套细胞淋巴瘤注册临床试验数据,同时简述泽布替尼全球开发布局。
一. ORR 84%:泽布替尼给套细胞淋巴瘤患者带来深度缓解
Best-in-class:泽布替尼对BTK靶点抑制更为专一、持久
泽布替尼,潜在的Best-in-class,泽布替尼 vs 伊布替尼 vs acalabrutinib,泽布替尼对BTK具有更为专一、持久的选择性抑制,血浆暴露量更高。
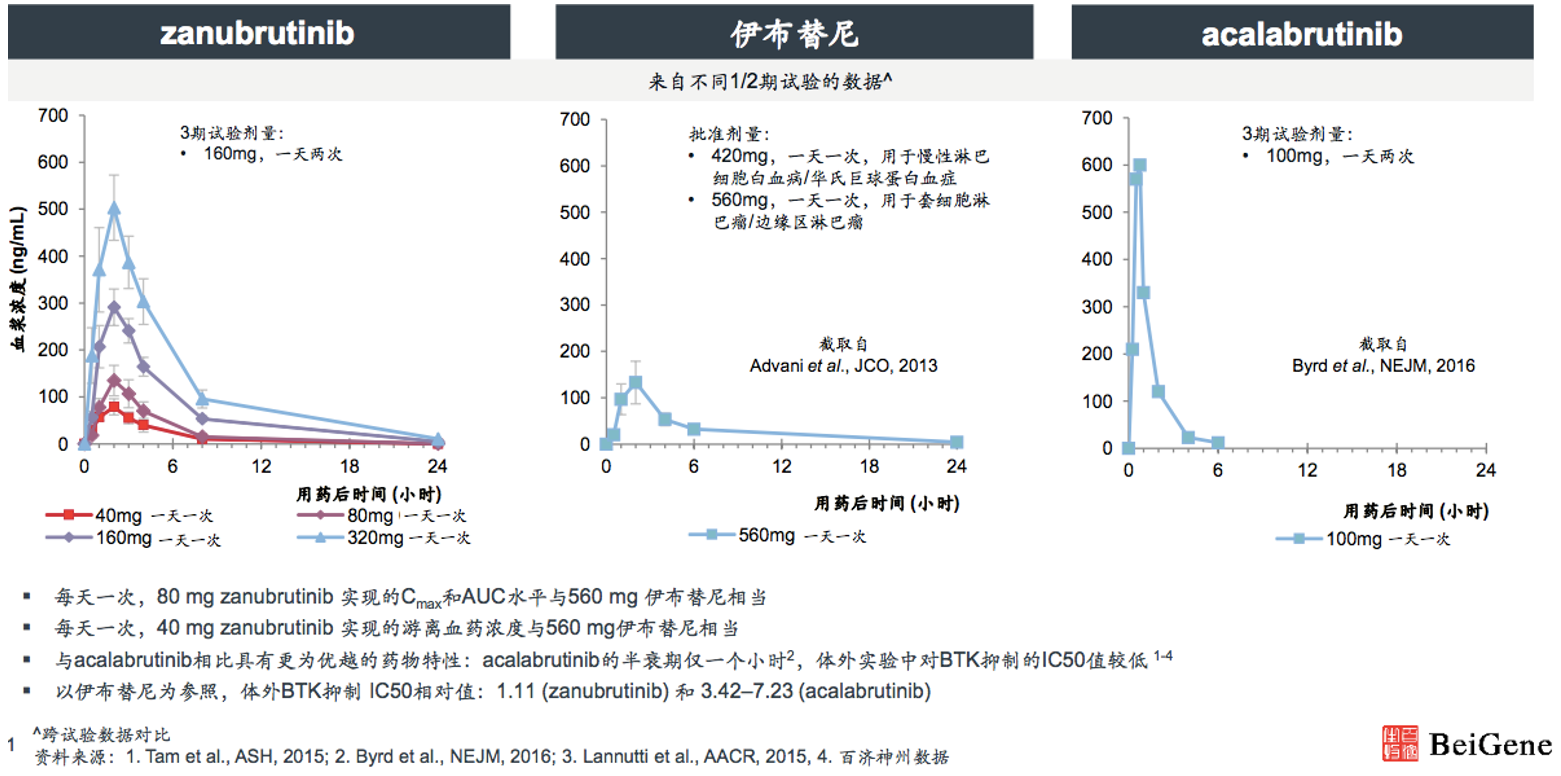
来源:百济神州
ORR 84%:泽布替尼给套细胞淋巴瘤患者带来深度缓解
注册临床:CTR20160888 (NCT03206970, BGB-3111-206)
专业题目:Bruton酪氨酸激酶(BTK)抑制剂BGB-3111治疗复发或难治性套细胞淋巴瘤(MCL)有效性和安全性的研究
泽布替尼关键临床数据:
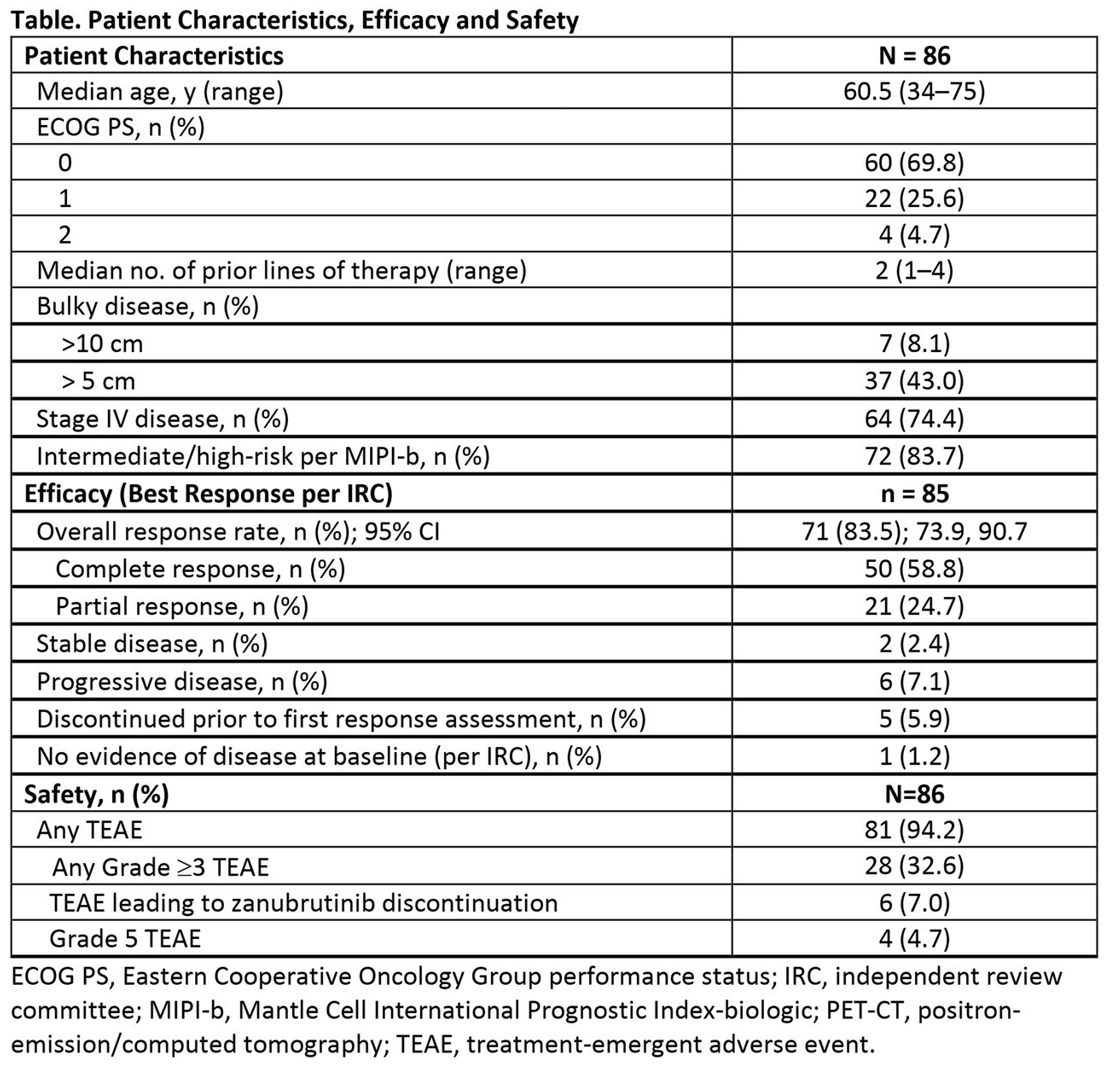
详见Safety and Activity of the Investigational Bruton Tyrosine Kinase Inhibitor Zanubrutinib (BGB-3111) in Patients with Mantle Cell Lymphoma from a Phase 2 Trial
二. 泽布替尼:立足中国,走向全球
BTK抑制剂泽布替尼的开发无疑是中国医药创新的一个突出代表,2019年,泽布替尼将会迎来多个里程碑事件,主要包括:
♦ 预计2020年初,中国获批用R/R-CLL/SLL;
♦ 公布华氏巨球蛋白血症中国患者中的关键2期临床(CTR20170208)数据,并递交sNDA;
♦ 完成临床试验NCT03734016的患者招募;
♦ ME-401联合泽布替尼,完成首例患者给药;
♦ 华氏巨球蛋白血症3期临床MYD88WT亚组数据公布
♦ 公布泽布替尼vs伊布替尼,华氏巨球蛋白血症主要数据;
♦ 华氏巨球蛋白血症和套细胞淋巴瘤全球1期数据更新,R/R MCL和CLL/SLL 关键2期临床数据更新等等;
FDA已经授予泽布替尼突破性疗法认定和快速通道资格,这将明显加速泽布替尼的美国注册进程!同时,泽布替尼立足中国,走向全球。
泽布替尼关键临床试验:

WM: Waldenstrom's Macroglobulinemia; R/R: Relapsed / Refractory; CLL/SLL: Chronic Lymphocytic Leukemia/Small Lymphocytic Lymphoma; MCL: Mantle Cell Lymphoma; FL: Follicular Lymphoma; MZL: Marginal Zone Lymphoma; DLBCL: Diffuse Large B-Cell Lymphoma; PCNSL: Primary Central Nervous System Lymphoma; RT: Richter's Transformation. 1. Cohort 2 of 17p del patients completed enrollment. 2. global trial and potentially registration-enabling in certain countries
截至目前,泽布替尼有多项注册临床试验正在开展中,其中全球开发布局中,值得关注的点主要包括:
1. vs伊布替尼,华氏巨球蛋白血症,招募完成,2019-2020美国递交NDA;
2. vs苯达莫司汀+利妥昔单抗,CLL/SLL一线治疗;
3. vs伊布替尼,r/r-CLL/SLL;
4. 滤泡性淋巴瘤,预计为全球首个获批该适应症的BTK抑制剂;
5. r/r- MZL,关键2期临床试验中
泽布替尼临床开发进展顺利,泽布替尼在多种B细胞恶性肿瘤患者中显示出令人激动的临床效果,泽布替尼与伊布替尼的头对头也在顺利开展,该头对头数据备受期待,2019年预计会公布主要数据!
伊布替尼的成功商业化是有目共睹的,泽布替尼作为一个潜在的best-in-class产品,具有十分光明的商业化前景,伊布替尼已在美国率先获批上市,中国获批上市将会随之而来,中国有着巨大临床需求,泽布替尼的上市将会极大改善中国患者药物可及性,给B细胞恶性肿瘤患者带来质优价廉的创新疗法,进一步改善患者的用药,惠及中国和全球癌症患者!
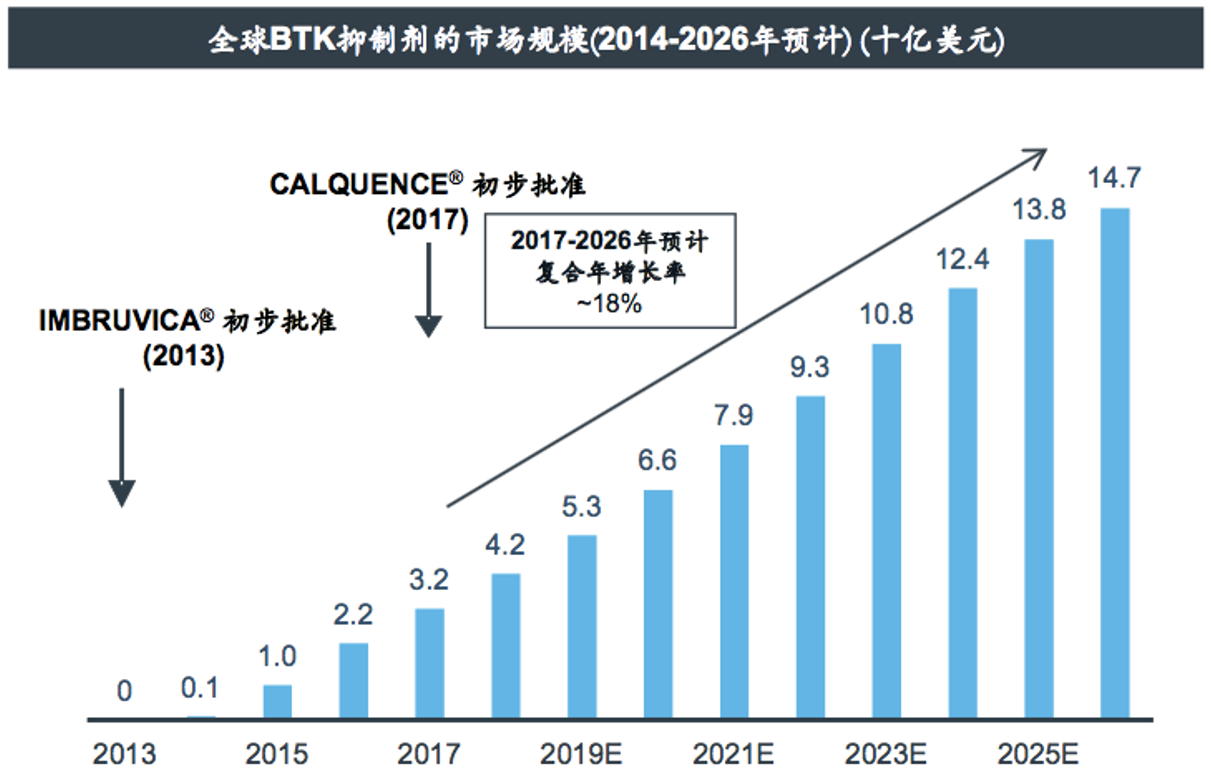
百济神州官方资料
参考来源: [1] https://www.fda.gov/drugs/nda-and-bla-approvals/breakthrough-therapy-approvals
作者简介:1°C,医药行业从业人员,希望自己的专业文字会越来越有温度,医药知识能够服务更多人,打破信息知识的壁垒!



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57