2019年12月16日,百济神州公布头对头临床试验ASPEN (BGB-3111-302) 关键进展,这就是备受关注的泽布替尼 vs. 依布替尼在华氏巨球蛋白血症中的一个重磅临床,数据显示泽布替尼 vs. 依布替尼,ORR, 28.9% vs. 19.8%,并未显示优效 (p=0.116)。
泽布替尼能够给B细胞淋巴瘤带来深度缓解,泽布替尼代表着中国企业医药创新的新高度,敢于和一线疗法开展头对头临床,泽布替尼 PK 依布替尼:虽败犹荣。
除了ASPEN外,另外的头对头临床试验,在复发/难治-CLL/SLL中,ALPINE (BGB-3111-305) 依旧值得期待。
本文关注泽布替尼中国审评审批进展,关注泽布替尼关键临床试验。
一.ASPEN虽败犹荣:泽布替尼 PK 依布替尼
ASPEN: A Phase 3 Study of Zanubrutinib vs Ibrutinib in Waldenström's Macroglobulinemia
临床设计
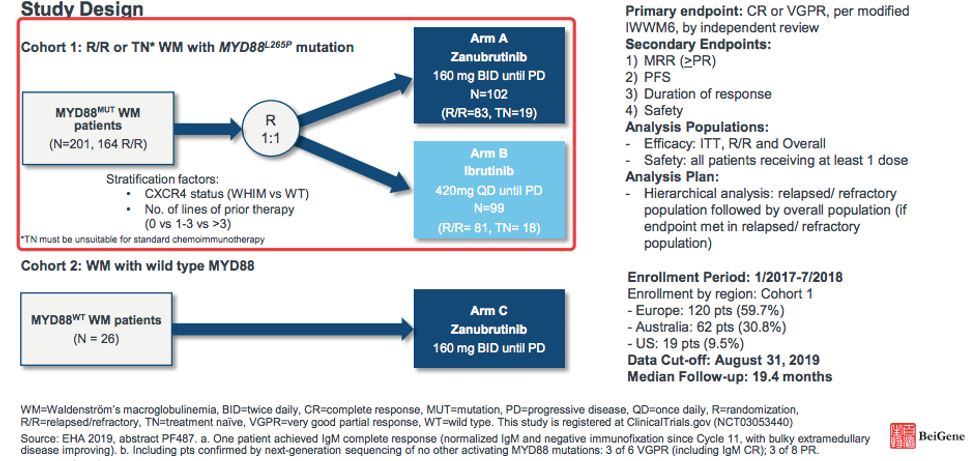
百济神州[1]
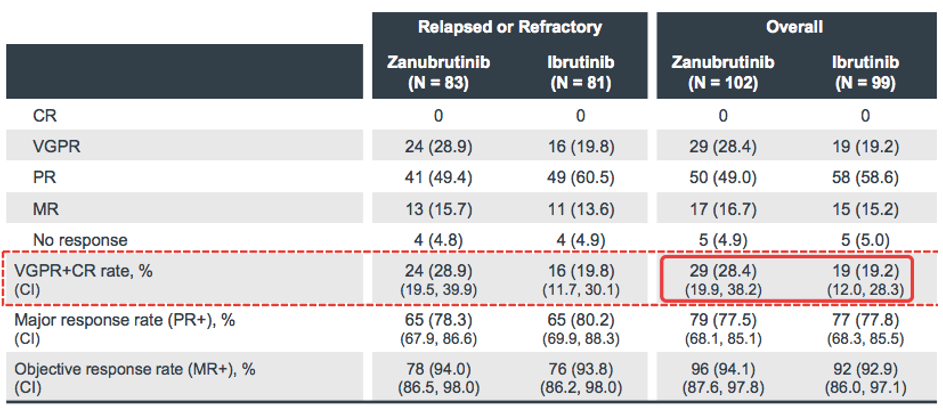
百济神州[1]
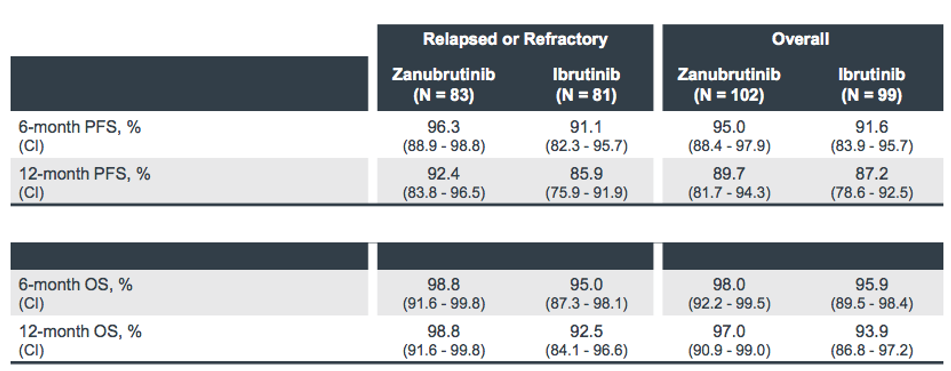
百济神州[1]
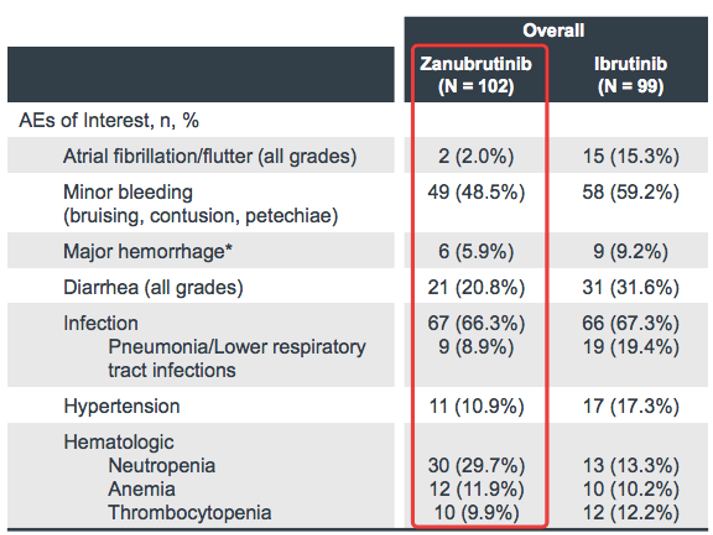
安全性:
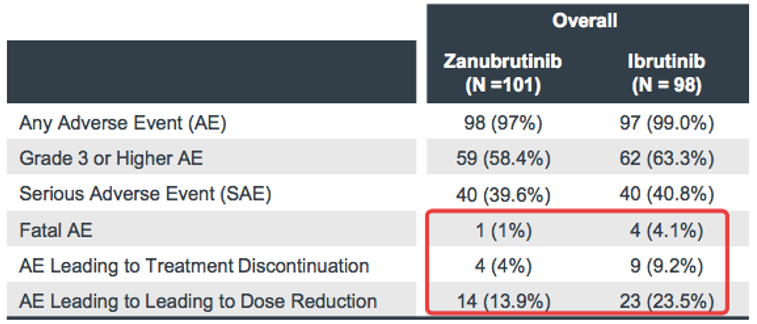
百济神州[1]
百济神州[1]
总结:
泽布替尼 vs. 依布替尼
华氏巨球蛋白血症中,ORR, 28.9% vs. 19.8%,并未显示出优效 (p=0.116);
但是,仍能够看出,泽布替尼 vs. 依布替尼安全性、耐受性有改善,1. 3级以上不良事件泽布替尼 vs. 依布替尼,58.4% vs. 63.3%;2. 在房扑房颤、出血、腹泻比例降低;3. 中性粒细胞减少症,泽布替尼组比例增加。
二.泽布替尼预计2020年1季度中国获批
泽布替尼两个上市申请受理号CXHS1800024,CXHS1800030,适应症分别为r/r-CLL/SLL, r/r-MCL,目前仍在技术审评阶段,预计先后在2020年1季度中国获批上市。
三.泽布替尼值得期待的里程碑事件
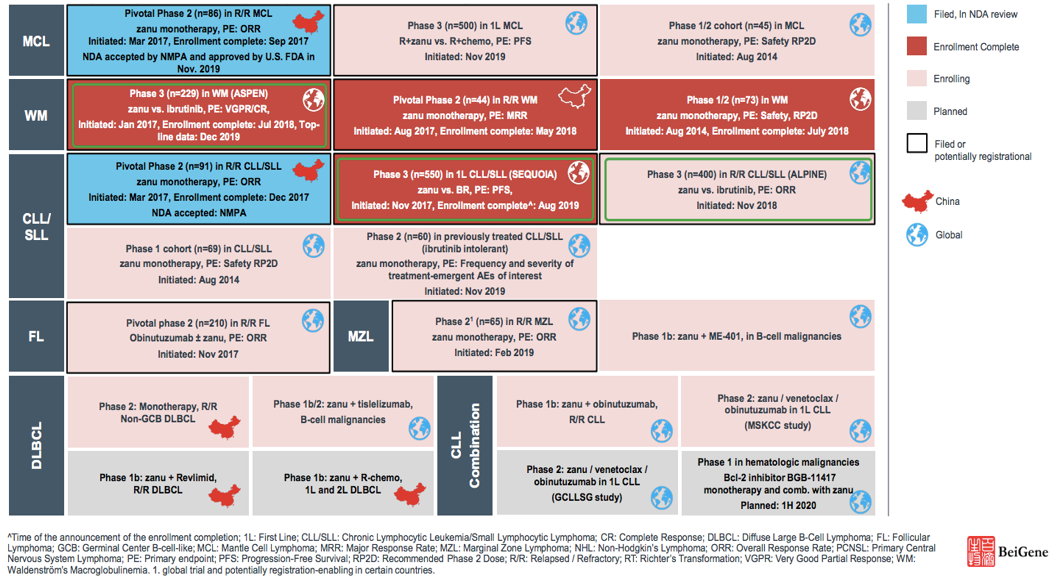
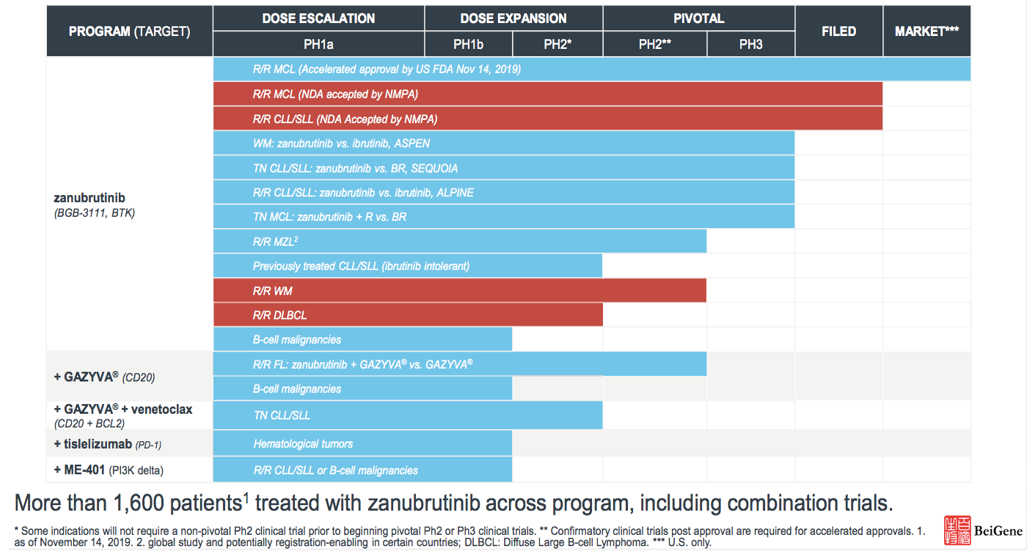
泽布替尼临床开发总结:
百济神州[1]
百济神州
2020年,泽布替尼值得关注的里程碑事件:

百济神州
目前,全球已有3款BTK抑制剂获批上市,Imbruvica为代表的BTK抑制剂销售额前景十分积极,2019年销售额预计在50-55亿美元,未来5年,BTK抑制剂市场预计突破100亿美元。
礼来[2]
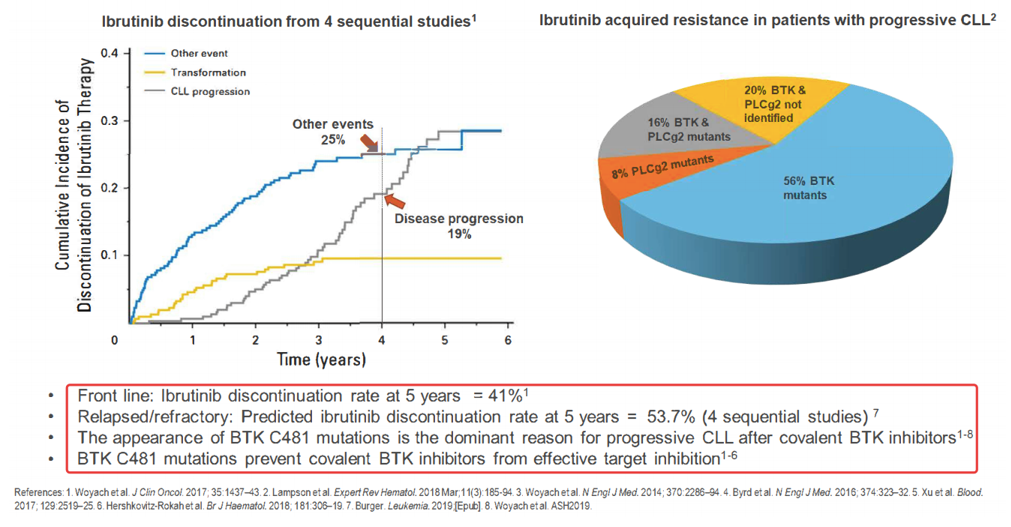
然而,无论如何优效,第一代BTK抑制剂仍有局限性,数据显示:
1. 依布替尼一线治疗患者中,患者5年停用比例41%
2. 依布替尼复发患者中,患者5年-停用比例过半;
3. BTK C481 突变是CLL患者进展的主要原因。
依布替尼、泽布替尼后,值得关注的是新一代的BTK抑制剂。
参考来源:
[1] http://ir.beigene.com/static-files/59795eef-4f0e-46a7-871f-9fcdda0c7925
[2] https://www.loxooncology.com/docs/presentations/LOXO-305-ASH2019-Phase1-8DEC2019-Final-V3.pdf
作者简介:1°C,医药行业从业人员,希望自己的专业文字会越来越有温度,医药知识能够服务更多人,打破信息知识的壁垒!



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57