KRAS
KRAS (Kirsten Rat Sarcoma Viral Oncogene Homolog)基因属于RAS家族,是人类癌症中最常见的基因突变之一,其编码的蛋白是一种小GTP酶(small GTPase)。KRAS基因参与了控制基因转录的激酶信号传导路径,从而调节细胞的生长和分化。KRAS可被上游的生长因子或酪氨酸激酶(如EGFR)短暂活化,活化后的KRAS可以激活下游通路,常见的有控制细胞生成的PI3K-AKT-mTOR信号通路,以及控制细胞增殖的 RAS-RAF-MEK-ERK信号通路,这条通路属于众多信号通路中的一条,这也给众多靶点联用奠定了生物学基础。
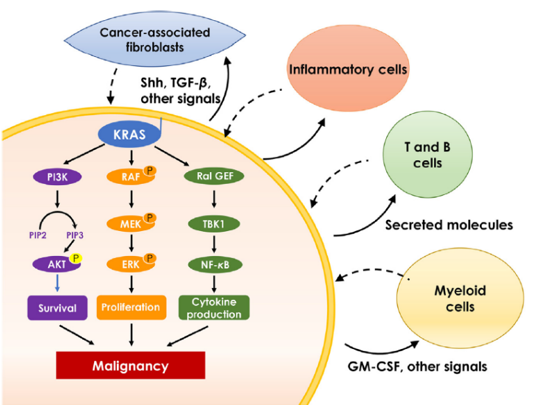
大多数KRAS错义突变发生在12号密码子中,导致甘氨酸变为其他氨基酸。如KRAS G12D和KRAS G12V突变,二者在90%的胰 腺癌中均有发现。其中,KRAS G12D也是结肠癌中最常见的KRAS突变。但令人遗憾的是,由于突变位点氨基酸残基难以通过化学方式结合,因此KRAS G12D和KRAS G12V目前仍然不可成药。
KRAS G12C是另一种主要的癌症驱动基因,约13%的肺癌和3%的结肠癌中存在该突变。对于存在KRAS突变的NSCLC患者而言,由于KRAS突变状态不受上游EGFR基因的影响,只有野生型KRAS基因受到上游EGFR基因的影响,因此EGFR靶向药物对他们的治疗并无效果。
目前,针对KRAS信号通路的抑制剂研发主要有三种策略,包括直接靶向KRAS G12C的策略;靶向KRAS上下游靶点的策略;以及间接靶向KRAS的策略等。
直接靶向KRAS G12C的抑制剂
AMG 510
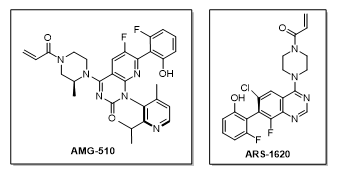
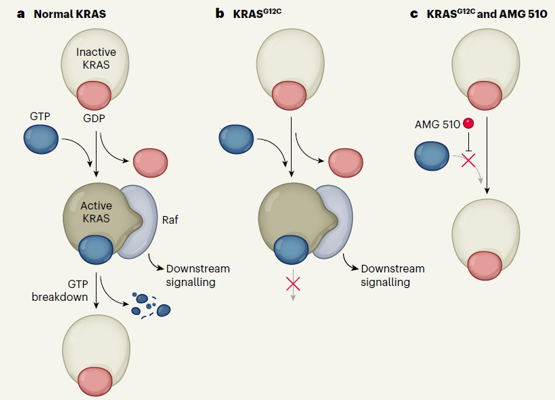
AMG 510是Amgen开发的一种小分子抑制剂,通过将KRAS锁定在非活性的GDP结合状态来特异性且不可逆地抑制KRASG12C。研究人员发现,KRAS G12C蛋白 His95翻转而形成的表面凹槽可以被AMG 510芳香环占据,这增强了其与KRASG12C蛋白的相互作用,此为抑制剂设计的关键突破。虽然AMG 510和ARS-1620(Araxes开发)在结构上具有一定的重叠,但由于AMG 510与His95凹槽的结合,使其效力为ARS-1620的10倍。另外,这种结合方式也提高了小分子与蛋白的结合特异性。在AMG 510结构中,由于空间位阻作用,甲基,异丙基取代吡啶环被锁定在两种构象中的一种,从而产生旋转异构现象,成为一种旋转异构体(rotamer)。
AMG 510的临床实验(NCT 03600883)结果令人满意。在23例NSCLC患者中有11例具有部分缓解,有效率达到48%。获得部分缓解的患者的中位缓解持续时间(DOR)达到15.1周,疾病稳定患者的中位接受治疗时间也达到了10周。最高剂量960mg的有效率最高,为54%(7/13),疾病控制率为100%。与AMG 510相关的最常见不良事件是胃肠道副作用,如腹泻和恶心。与NSCLC相比,结肠癌的数据没有那么亮眼,迄今为止只有一名结肠癌患者接受了960mg剂量治疗,在这么小的样本量中解释数据需要谨慎。
2020年3月9日,Amgen提交的AMG 510临床申请获得CDE受理。

MRTX 849
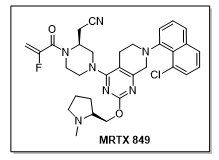
MRTX 849是由美国Mirati Therapeutics公司开发的针对KRAS G12C突变的口服小分子抑制剂。它不可逆地与KRAS G12C的可诱导Switch II口袋中的半胱氨酸12结合,并将其锁定在非活性GDP结合状态,从而抑制RAS / MAP激酶途径。其KRAS G12C的选择性是野生型KRAS和其它蛋白上胱氨酸的1000倍以上。MRTX 849口服生物利用度达到30%,并具有广泛的组织分布以及线性药代动力学,单次给药后半衰期长达25小时。
MRTX849第一个多中心Phase I/Pahse II临床实验于2019年1月开始,目前正在进行中(NCT 03785249)。根据Mirati Therapeutics公司在第31届EORTC-NCI-AACR会议中披露的临床实验结果,MRTX849临床试验目前招募了17名患者,其中包括10名NSCLC患者,4名CRC患者,3名其它癌症类型患者。他们接受不同剂量MRTX849的治疗,最低剂量为150 mg每天一次,最高剂量为600 mg每天两次。在接受所有剂量(All Doses)治疗的患者中,3/6能被评估的NSCLC患者,和1/4能被评估的CRC患者达到部分缓解;在接受最高剂量(600mgBID)治疗的患者中,3/5能被评估的NSCLC患者,和1/2能被评估的CRC患者达到部分缓解,其它患者病情稳定。
由于入组人数较少,目前MRTX849与AMG 510的优越性尚不具可比性。
JNJ-74699157 (ARS-3248)
Araxes 公司(wellspring公司的子公司)是最早涉足KRAS新突变位点的公司之一。近年来先后报道出ARS-853和ARS-1620等新型小分子抑制剂。化合物ARS-853虽表现出较好的细胞活性,但药代动力学性质较差,不适于进行动物体内模型的药效评估。ARS-1620对KRAS G12C具有高效性和选择性,可实现快速和持续的体内靶标占据以诱导肿瘤消退。
ARS-3248是在ARS-1620基础上研发的新一代KRAS G12C抑制剂。2019年5月份, Wellspring公司宣布FDA已批准ARS-3248的IND申请。Janssen对该化合物的临床开发负全部责任,且于7月26日在clinical trials登记JNJ-74699157(ARS-3248)开展临床I期试验(NCT04006301),选择KRAS G12C阳性晚期实体瘤患者入组,研究期限为4年。
JAB-3312
2019年9月29日,由国内公司加科思自主研发、具有全球知识产权的小分子口服抗肿瘤药JAB-3312在中国获得临床许可,目前已于中国(NCT04121286)、美国(NCT04045496)同步开展临床试验。
JAB-3312将用于治疗携带KRAS G12突变、BRAF Class3、NF1LoF、以及RTK突变、扩增或重排等基因型异常的实体瘤患者,包括但不限于非小细胞肺癌、结直肠癌、胰 腺癌、食管鳞癌、头颈部鳞癌。同时JAB-3312单药或JAB-3312联合PD-1抗体,也可用于经PD-1/PD-L1抗体治疗失败或耐药的非小细胞肺癌、结直肠癌、膀胱癌、三阴性乳腺癌患者等。
LY3499446以及其他新化合物
目前,正在开发的新型KRAS G12C抑制剂还包括Eli Lilly公司的LY3499446,Pfizer四氢喹唑啉衍生物(US 20190248767A1)和AstraZeneca的四环化合物(WO 2019110751 A1)等等。三者中进展最快的是LY3499446,其临床一期实验(NCT 04165031)目前已在澳洲和美国展开。在这项研究中,LY3499446将作为单一疗法并与其他药物如西妥昔单抗联用对晚期实体瘤(包括NSCLC和CRC)的治疗进行评估。
最近,Revolution Medicine在2020年1月的AACR-IASLC会议中披露了一种新型三复合物抑制剂对GTP-结合模式的KRAS G12C进行抑制。它克服了rtk介导的逃逸机制,并在NSCLC的临床前模型中推动了肿瘤的消退,现在可以将其归为第二代KRASG12C抑制剂。
针对KRAS的新尝试,包括抗KRAS的TCR-T治疗(NCT 03745326)以及与上游通路SHP2抑制剂的联合治疗(NCT 03989115, NCT 03114319),目前正在进行中。
KRAS G12C抑制剂的联合用药
研究者将AMG 510与HER,EGFR, SHP2, PI3K, AKT和MEK抑制剂分别组合,于KRASG12C细胞系中进行体外实验。MEK抑制剂与AMG510的组合在多种情况下具有协同作用。此外,MAPK抑制剂与AMG 510联用能够消除可能限制疗效或诱发耐药性的残留信号通路,因此有必要进行进一步研究。
MRTX 849同样与大约70个化合物在对MRTX849敏感和部分耐药的非临床模型中进行了体外联合筛选,以探索可能增强MRTX 849反应并克服潜在耐药性的联用方式。目前发现, MRTX849和HER2家族抑制剂阿法替尼、CD4/6抑制剂palbociclib、SHP2抑制剂RMC-4450以及mTOR通路抑制剂等小分子抑制剂的组合具有良好的前景。
当前AMG 510和MRTX 849的临床数据均缺乏对CNS渗透性的评估。AMG 510研究未招募有活动性脑转移的患者,接受MRTX 849治疗的受试者均未记录脑转移。由于CNS是KRAS突变癌症(尤其是NSCLC)中常见的转移部位,因此需要进一步评估这些化合物的CNS活性。
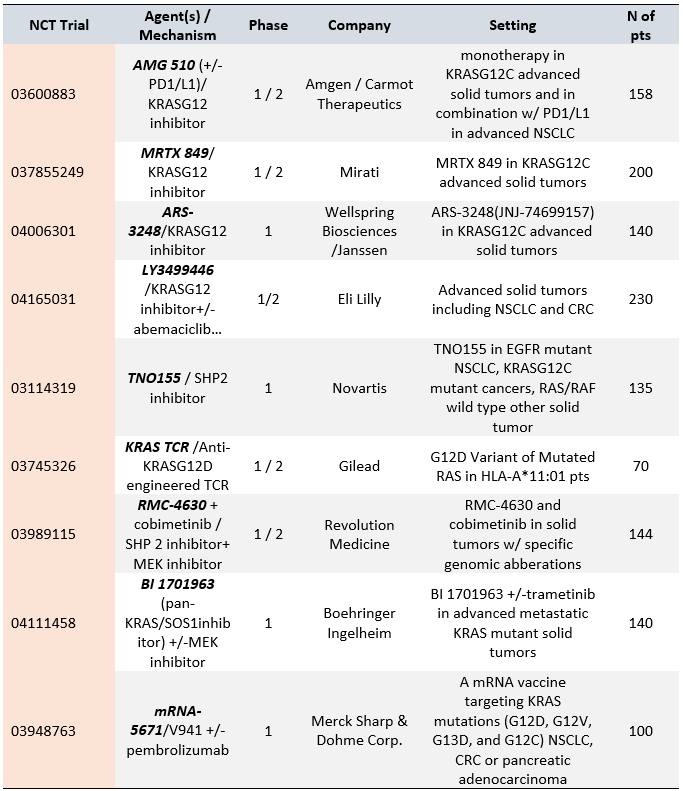
表1 处于临床阶段的KRAS G12C抑制剂
靶向KRAS上下游靶点的抑制剂
由于KRAS蛋白的"不可成药"性,靶向KRAS信号通路的上游与下游调控蛋白成为抑制KRAS通路的一个研究方向。目前处于在研阶段的抑制剂如表2中所示。
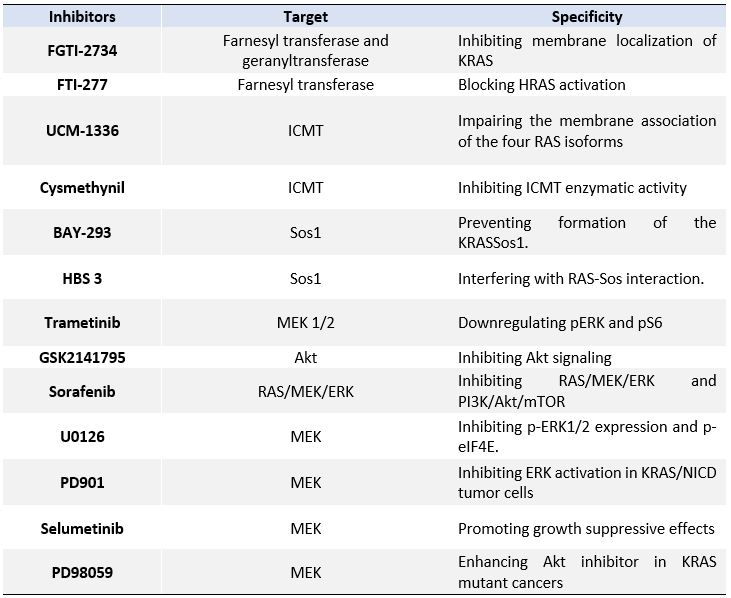
表2 处于在研阶段的KRAS上下游靶点抑制剂
总结
风雨三十载,曾经被认为"不可成药"的KRAS靶点,如今屡屡有新的突破,为全球肺癌以及其他种类癌症患者带来福音。截至目前,国内外诸多医药研发企业纷纷布局KRAS抑制剂研发管线,曾空旷寂寥的赛道如今百舸争流。虽然AMG 510暂时领先,但以MRTX 849为代表的诸多竞争者不甘示弱,各显神通。各公司以解决临床需求为出发点,从临床前研发至临床开发阶段,通过差异化布局寻求竞争优势。桃红李白竞争妍,绿野尽春色。相信不久的未来KRAS抑制剂能在临床取得更大突破。
参考文献:
1. Cancer Treatment Reviews 2020, 84, 101974.
2. Cancer Cell 2020, 37, 5-7.
3. Nature 2019,575, 294-295.
点击下图进行CPhI & P-MEC China 2020观众预登记抽奖,奖品多多!



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57