距2018年11月CDE发布《第一批临床急需境外新药名单的通知》,目前已有66个药品被列为临床急需境外药品。而临床急需境外新药主要是指近年来已在美国、欧盟或日本批准上市而我国尚未上市的,用于罕见病治疗的新药以及用于防治严重危及生命或严重影响生活质量的疾病,且尚无有效治疗手段或具有明显临床优势的新药。为加速这些药品在国内获批上市,国家药品监督管理局、国家卫生健康委员会制定《临床急需境外新药审评审批工作程序》。
根据《临床急需境外新药审评审批工作程序》,列入临床急需境外新药名单的品种,企业可在提交相关资料后,直接提出上市申请。而且CDE已建立专门通道开展审评,对罕见病治疗药品,在受理后3个月内完成技术审评;对其他境外新药,在受理后6个月内完成技术审评。尚未申报的品种,可随时提出与CDE进行沟通交流,尽快提出上市申请。
时隔一年多,随着国家药审政策的利好,已有多款药品在国内获批,接下来笔者将根据这66款药品在国内的审批进度将其分为已批准、上市申请中、申请临床/批准临床/临床试验申请中以及未申报四类,其中将着重分析已批准和处于上市申请阶段的药品。
目前,已有25款临床急需境外药品在国内获批,其中有4款已被批准治疗肺动脉高压,3款被批准治疗丙肝,2款被批准治疗克罗恩病。从适应症上来看,这24款药品大部分用于治疗罕见病,如肺动脉高压、IVA型黏多糖贮积症、多发性硬化症、法布雷病等,其中依洛硫酸酯酶α和阿加糖酶β是目前国内治疗相应疾病的首款且唯一一款药物。从药品成分上来看,有6款单抗,1款**,4款复方制剂。不在这其中有个别药品如辉瑞的西地那非、田边三菱的依达拉奉和艾伯维的阿达木单抗早已在国内获批,但治疗罕见病适应症的都是近年来才被批准的。值得一提的是,艾伯维的阿达木单抗截至目前在国内共获批6个适应症,分别是类风湿性关节炎(2010)、强直性脊柱炎(2013)、中重度斑块型银屑病(2017)、多关节型幼年特发性关节炎(2019)、克罗恩病(2020.01)和葡萄膜炎(2020.03)。
已批准的临床急需境外药品
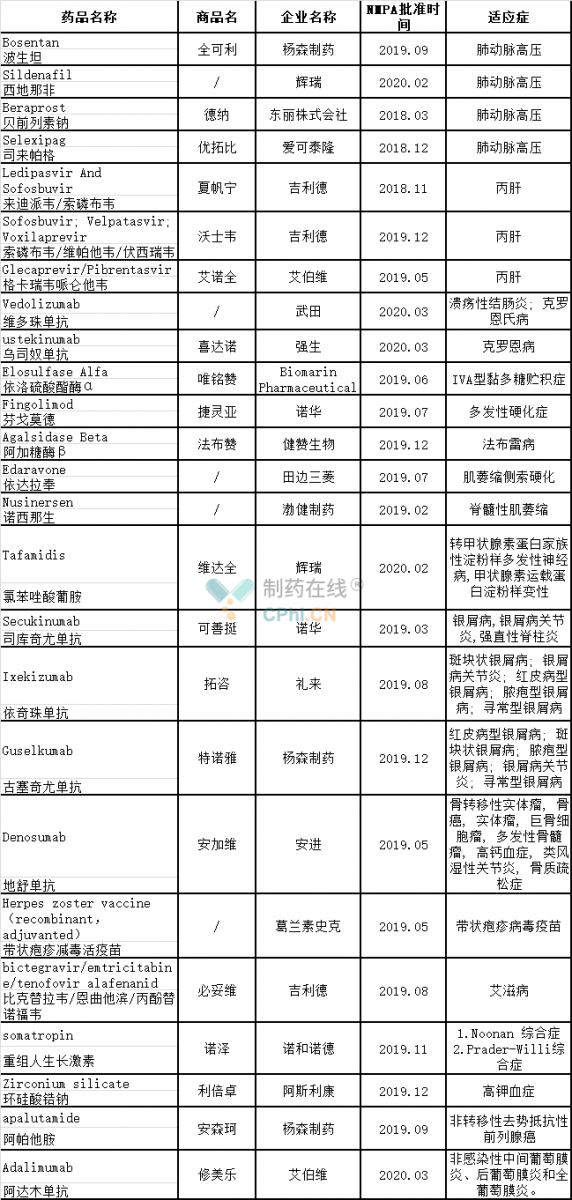
除了上述已获批的25款药物,目前还有10款临床急需境外药品处于上市申请阶段,这10款药品大部分针对罕见病,如戈谢病,亨廷顿氏舞蹈症等,其中I型黏多糖贮积症在国内还没有任何一款有效治疗药物,而戈谢病在国内获批的药物仅有伊米苷酶。Dompe farmaceutici的重组人神经生长因子滴眼液于2017年被EMA批准用于中重度神经营养性角膜炎的治疗,目前在国内处于上市申请阶段,不过国内已经批准四款注射用重组生长因子,即丽珠集团的丽康乐、武汉海特生物制药的金路捷、舒泰神(北京)生物制药的苏肽生和未名生物的恩经复,其中丽康乐、苏肽生批准用于治疗视神经损伤,而另外两款被批准用于治疗正已烷中**周围神经病。最值得一提的是,氘代丁苯那嗪是FDA批准的首个氘代药物,已于2019年12月在国内提交治疗亨廷顿舞蹈症的新药申请。
已提交上市申请的临床急需境外药品
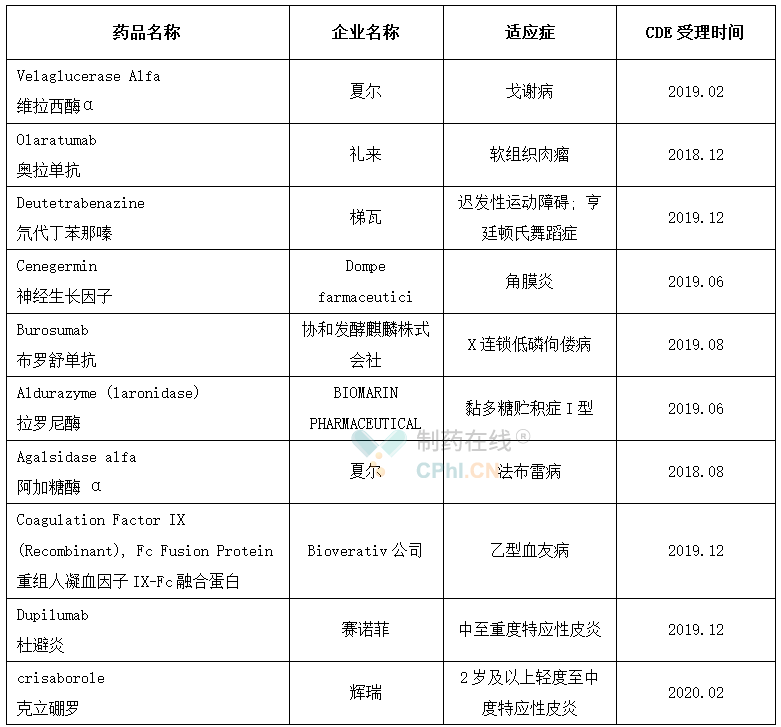
此外,还有9款药物在国内申请临床试验或处于临床试验阶段,其中伊那尼布、卡那奴单抗进展最快,处于III临床阶段,而健赞依鲁司他在国内已被批准临床,但协和药业已经提交了其仿制药上市申请。
申请临床/批准临床/临床试验中的临床急需境外药品
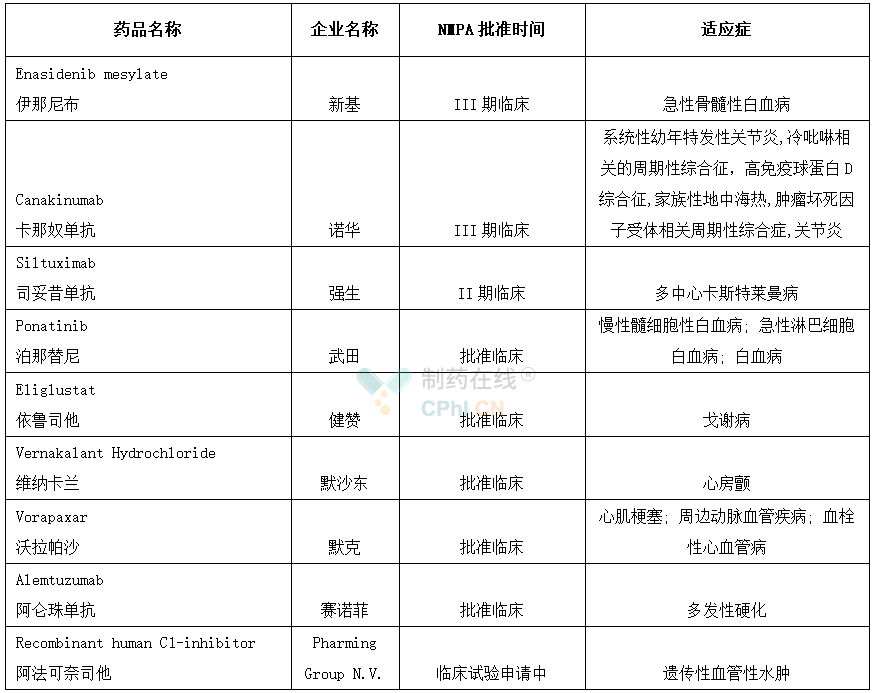
另外22款药物在国内还未有任何进展,其中Acorda的达伐吡啶和Prestwick丁苯那嗪虽未在国内有进展,但印度阿拉宾度和印度瑞迪博士实验室已分别在国内提交达伐吡啶和丁苯那嗪的进口申请。夏尔的艾替班特的化合物专利已在国内到期,但还未在国内上市,但成都圣诺生物已提交仿制药上市申请,豪森的3.1类新药艾替班特已被批准临床,且值得一提的是,豪森的艾替班特已于近日在美国获批。新基的阿普斯特同艾替班特情况相似,石药集团已于近日提交其仿制药上市申请。而第一三共沙丙蝶呤虽未在国内有任何进展,但是默克的沙丙蝶呤已经在国内获批,商品名为科望。
未在国内申报的临床急需境外药品
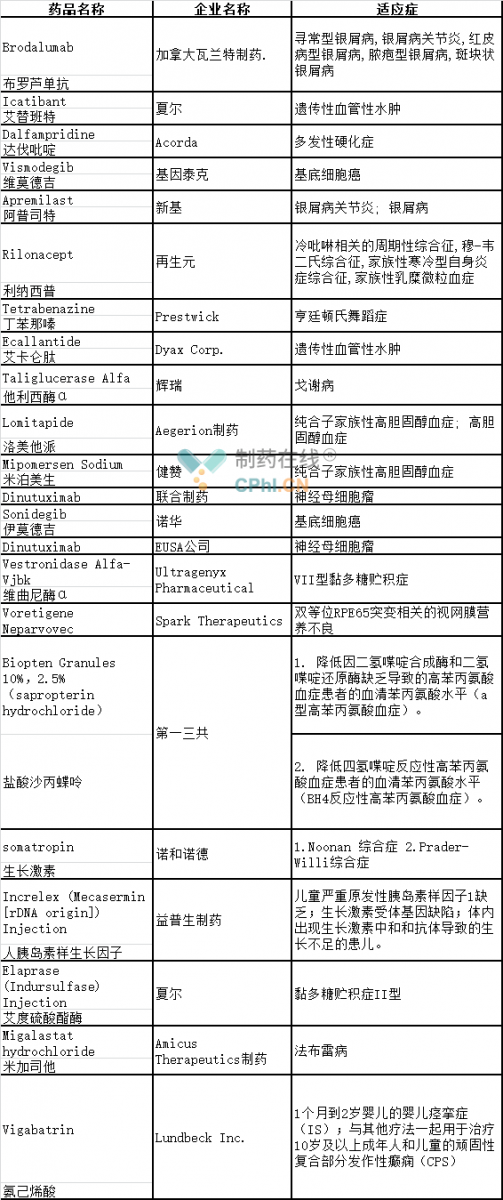
时隔一年多,这两批临床急需境外药品差不多已有一半被批准,9款在审评审批的路上,从这些数据可以看出国家出台的一系列加快境外药品审评审批政策对临床急需境外药品的审批具有强大的推动作用。此外,为了促进这些药品在国内的获批上市,国外企业与国内企业也开始联起手来。衷心期盼上述未批准药品可以早日在国内获批,造福众多国内患者。
参考资料:
[1] CDE、NMPA官网
[2] insight数据库
点击下图进行CPhI & P-MEC China 2020观众预登记抽奖,奖品多多!



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57