6月11日,据CDE官网武田国际贸易有限公司5.1类新药醋酸艾替班特注射液的上市申请被CDE受理,这是继2018年成都圣诺生物首家报产艾替班特注射液后,国内第二家企业递交该遗传性血管性水肿(HAE)药物的上市申请。

艾替班特(icatibant)原研药是Jerini AG(Jerini AG2008年被Shire收购,Shire后又被武田收购)研发的一款特异性的缓激肽B2受体拮抗剂,通过阻断水肿形成的关键介质--缓激肽发挥作用。2008年该药首次在欧盟被批准用于治疗成人HAE的急性发作,商品名为Firazyr,2011年被FDA通过优先审评加速批准用于治疗18岁以上HAE的急性发作,2017年又被欧盟批准扩大适应症人群,用于2岁及以上儿童和青少年HAE患者。
据PDB数据显示,近年来艾替班特全球市场规模持续增长,2018年市场销售达4.1亿美元。而且在美国已有艾替班特仿制药获批上市,分别是梯瓦和江苏豪森。
遗传性血管性水肿(HAE),是一种常染色体显性遗传病,主要表现为反复发生的皮肤、呼吸道和内脏器官肿胀,在全球范围内的发病率为1/10000至1/50000。研究发现HAE 的发病主要是由于血清 C1 抑制物(C1-INH)缺乏导致,而按照C1-INH的水平和功能,可将 HAE 分为 3 型。其中I 型患者(占 85%)的 C1-INH 水平降低伴功能降低,II 型患者(占 15%)的血清 C1-INH 正常但功能降低,III 型较罕见,患者的 CI-INH 水平和功能均正常,多在雌激素水平较高如口服避孕药或妊娠时发生。
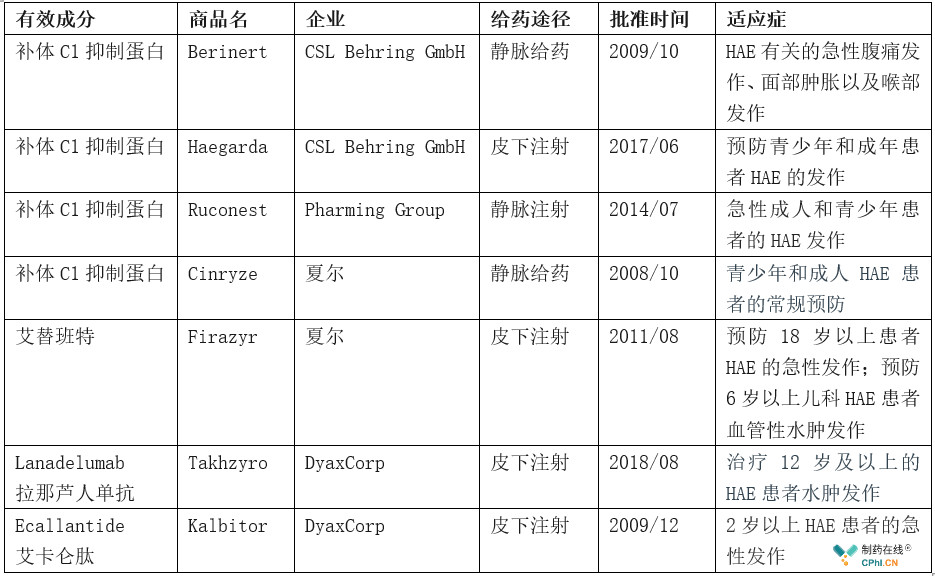
目前,HAE还没有可治愈的办法,不过美国FDA已经批准了多款预防或治疗HAE药物(详见下表),其中Berinert、Haegarda、Ruconest和Cinryze属于C1酯酶抑制物(C1INH),艾替班特是一款选择性缓激肽B2受体拮抗剂,用于C1酯酶抑制剂缺乏HEA,艾卡仑肽是一款选择性、可逆性血浆激肽释放酶抑制剂。
在国内,HAE于2018年被列入国家卫生健康委员会等5部门联合制定了《第一批罕见病目录》。然而,目前国内还没有治疗HAE急性发作的有效药物,预防用药也只有达那唑,该药是一种甾体杂环化合物,为雄激素17α-乙炔睾丸酮的衍生物,主要用于治疗子宫内膜异位症,不过也可用于治疗纤维囊性乳腺病、自发性血小板减少性紫癜、遗传性血管性水肿、系统性红班狼沧、男子女性性乳房、青春期性早熟。
2018年,Shire的艾替班特注射液被列入《我国第一批临床急需境外药品名单》。考虑到纳入境外已上市临床急需新药名单的药品,若尚未进行申报的或正在我国开展临床试验的,经申请人研究认为不存在人种差异的,均可提交或补交境外取得的全部研究资料和不存在人种差异的支持性材料,直接提出上市申请。笔者在CDE官网查询,未查到Shire或武田在国内开展艾替班特临床试验的信息,猜测此次武田是直接递交艾替班特注射液的上市申请。
不过值得一提的是,在国内早已有两家国内企业开始布局艾替班特市场,其中成都圣诺生物制药进展最快,早已于2018年按3类仿制药递交了上市申请。而另外一家企业是江苏豪森,已于2016年被批准临床。虽然江苏豪森艾替班特在国内进展较慢,但已于今年3月在美国被批准用于治疗HAE。
此外,除了艾替班特,武田制药的另外一款HAE药物--拉那芦人单抗也已在国内报产,该药较其他HAE药物使用方便,仅需每月皮下注射一次。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57