近日,第三批国家药品集采开标,在制药行业再次掀起轩然大波。“一瓶水买一年的药”、“男性的幸福不再烦恼”、“原研产品纷纷出局”......集采品种降幅惊人的背后,更多的是整个行业对超低价中标结果的困惑。那么,在仿制药必须面对如此低价榜单的当下,创新药未来的定价也要开始自危了吗?且从长远来看,低价中标对于我国药品研制的未来发展,会有哪些影响呢?
第三批国采中选结果令行业再次沸腾
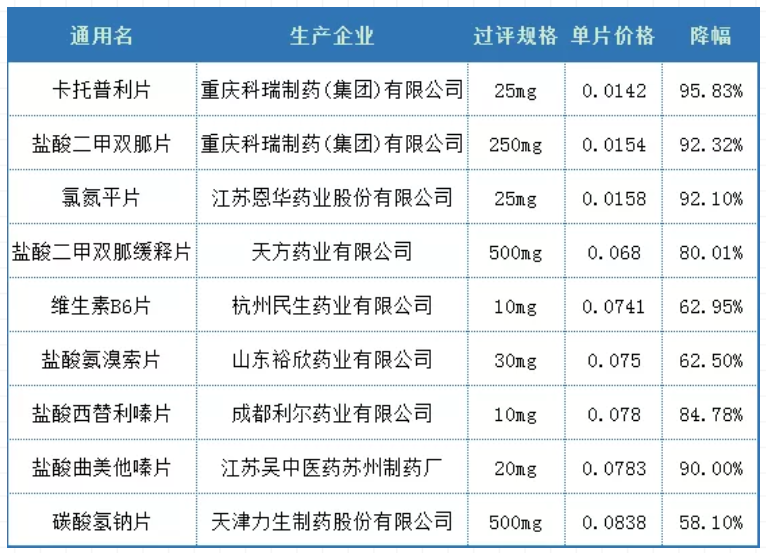
本次国家药品集采结果最终出炉后,共有55个品种采购成功,药品品种数量接近前两次之和。进一步统计,单片价格低于1毛钱的最低中标品种就有9个(以通用名统计);重庆科瑞制药(集团)有限公司的卡托普利片为本次集采单片价格最低(0.0142元/片),其次是该公司的盐酸****片(0.0154元/片)。
除上述品种外,更令行业吃惊的品种,为辉瑞“伟哥”的仿制品种西地那非,齐鲁制药以每片2元左右的最低价,成为唯一中标企业,原研辉瑞出局(当然,伟哥的主战场不在医院)。
表1.1 第三批集采~“单价”<1毛钱的最低中标品种
仿制药的集采限价,对创新药的开发是否构成影响?
此次国内集采的结果,可以说给所有仿制药企业又上了一堂记忆深刻的课,那么,仿制药的低价过评,对于创新药的未来走势,会有影响吗?
这里,我们先说说我国新药企业的类型。兴业证券研究所曾将我国创新药企业分为1.0/2.0/3.0三个模式。1.0模式,即老牌大型药企由仿到创,逐步布局创新药领域,如恒瑞;2.0模式,即纯粹的创新型研发企业,如信达、百济等;3.0模式,即参与国际合作的开放式创新药企,这也是近年发展极快的一种模式。
1.0老牌大型药企,虽然大都已经上市融资,但在早年就已经初步完成了资本积累,仿制药业务往往是新药开发的重要经济支柱,于此时遇到如此杀价的集采,虽不至于伤筋动骨,但势必会做出调整;而比较惨的就是那些初创型且尚未上市的中型企业,如有品种遇到这几轮集采,倘若没有做好准备,其创新业务就相当被动了。而2.0/3.0类型药企的创新药开发,资金主要来源于融资,仿制药于集采中的拼杀,理论上短期不会波及到创新药的开发过程。
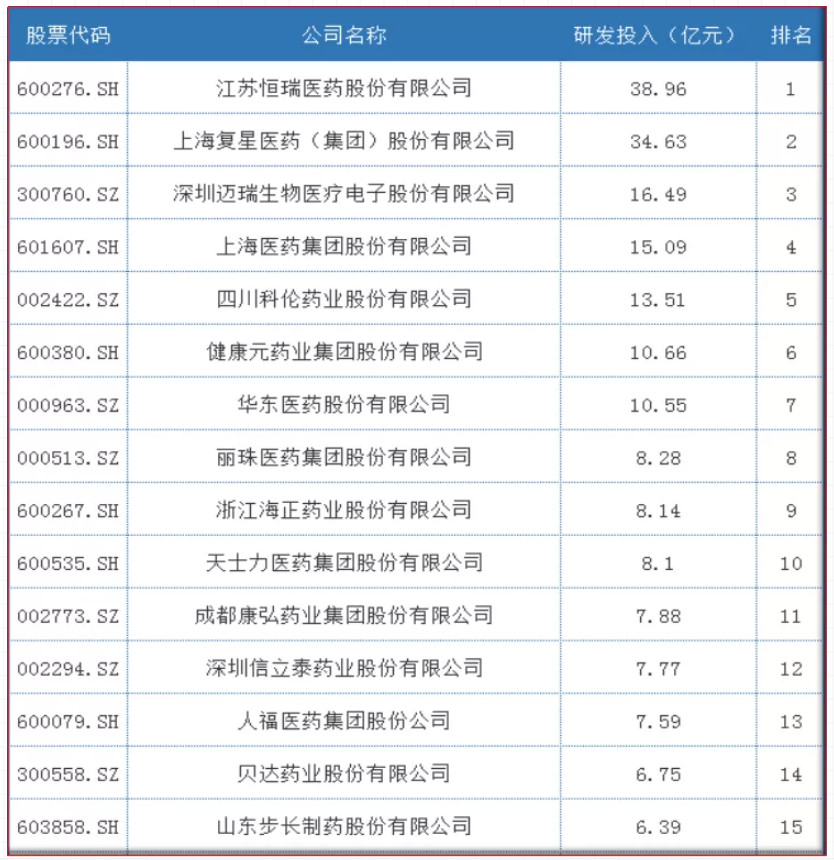
表1.2 2019年国内上市药企研发投入
创新药的价格,由谁来定?
今天的“带量采购、低价中标”,虽然令制业界“苦不堪言”,但也是历经了多年的市场调查与政策调控,尤其是价格政策方面,更是出台了《药品价格管理暂行办法》(1996)、《药品政府定价办法》(2000)、《药品差比价规则》(2011)等等...
而对于创新药来说,通常新药的定价更多的是来源于药企。原则上,企业的单独定价要以成本核算为基础,但由于政府部门很难核实新药从研发到开发再到上市的真实成本,故新药单独定价实际上为自主定价。而药企为了快速回收前期成本,同时开展其他项目,一般会定价较高,以防止后续仿制药的市场分羹。比如,《药神》里面的格列卫、冰桶挑战里的SMA天价药等。
但倘若新药的价格完全是由政府来定,为了提高药品消费者的整体福利,势必会对药品价格实行价格上限规制,如若再没有下限限制,新药就面临着白菜价的可能。高风险不再有高收益,投资人自然会撤离这个行业,长久来说,弊端更多。
且有大批的国内外学者对此进行过多年研究,而结论大都是“过低的药品定价最终会影响制药业的投资决策,使得研发资金相应减少”、“药品价格适当提高将有利于我国制药企业发展”,“创新药管制价格与研发支出的均衡不仅可以保证患者的效用,还可以保证药企的合理研发投入水平”...
日本药品定价政策非常值得借鉴!
日本无论是药品研发,还是相关的药品政策,都很值得借鉴。早年间,日本对于新药的价格制定,是基于成本计算和参照同类产品价格并根据平均国外价格进行调整后制定。新药的价格审定、新剂型/新规格的药品价格审定,每年都有多次;且每2年会对药价基准中收载的所有品种进行价格调整,调查对象为所有的批发商、部分医院及诊所,调查期为1个月。由于注重市场调查,药品的政府定价与市场实际销售价格能够保持基本持平。
日本的创新药在获得批准上市后,企业即可申请新药价格收载。根据事先调查的基础价格,由厚生劳动省相关部门与企业举行听证,后由相关部门做出核定草案,再由另一组织进行定价,形成最终价格后报中央医疗保险协会总会批准。
日本的原研药政策同国外大部分国家类似,会有一定的独占期,独占期过后仿制药上市;首仿(原研药价格的70%左右)在药价基准中被收载后,该原研药须进行价格调整,但幅度不会太大(有具体公式),会根据药事法批准时间和是否作为长期收载品种决定。
整体而言,日本的药价制定机制,会更好的复合市场机制,且会更为灵活的进行调整。
总结
综上,笔者认为:
1)仿制药的超低价中标集采,势必会对创新药业务形成一定的冲击,很多公司会根据集采结果来调整公司内部创新药业务的研发投入;
2)仿制药价格的走低,一定程度上会对创新药的价格造成竞争,无论从药物经济学的角度还是风险获益比的结果,面对同类中如此悬殊的价格差,老百姓很难选择刚刚上市的新药;
3)新药公司需要更加深入挖掘市场需求及变化,以更为合理的计算出新药的上市价格;
4)持续的最低价中标,对国内药品研发,弊大于利。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57