人类酪氨酸激酶蛋白由四个成员组成:JAK1、JAK2、JAK3和TYK2。这些蛋白是治疗自身免疫性疾病和血液恶性肿瘤重要的靶标。目前,美国食品和药物管理局(FDA)批准的JAK抑制剂包括tofacitinib(辉瑞)、baricitinib(礼来/Incyte)、ruxolitinib(Incyte)和upadacitinib(AbbVie),而且,大量其他JAK抑制剂目前正在进行各种临床试验。辉瑞的JAK1抑制剂Abroctinib(图一,1),于2018年2月被FDA授予中重度特应性皮炎的突破性疗法。为满足临床研究和上市需求,辉瑞的研发人员一直在开发安全高效的Abroctinib生产工艺。
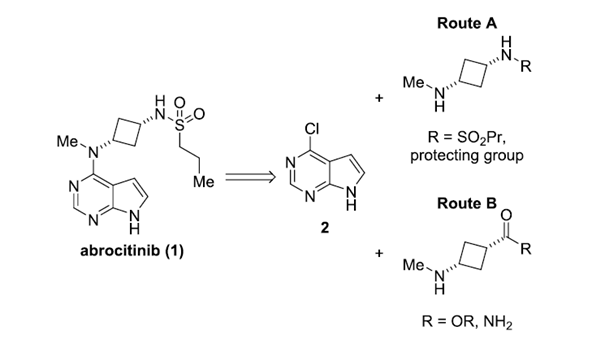
图一 Abroctinib两条初始合成工艺
目前,合成Abroctinib主要有两种策略,如图一所示:Route A,向4-氯吡咯嘧啶2中添加二氨基环丁烷;Route B,向2中添加单氨基环丁烷并随后进行胺化。获得顺式-1,3-二氨基环丁烷将是这两种战略的关键挑战。当下,合成1,3-二氨基取代环丁烷的方法较为局限,主要有:[2+2]环加成、还原胺化、卤化物/磺酸盐胺化和官能团重排。合成这类低分子量二胺主要的挑战包括:PH依赖的溶解度、挥发性和难以进行反应分析。
虽然Route A具备收敛性,但需要合成氨基经保护基保护的二环丁烷。在Route B中较早地引入吡咯嘧啶核可以获得物理性质较好的中间体,如溶解性、结晶度较好,但合成片段后需要结合胺化反应。这两种策略都需要利用高能硝烯型重排,该步骤也是Abroctinib制备工艺的关键所在。
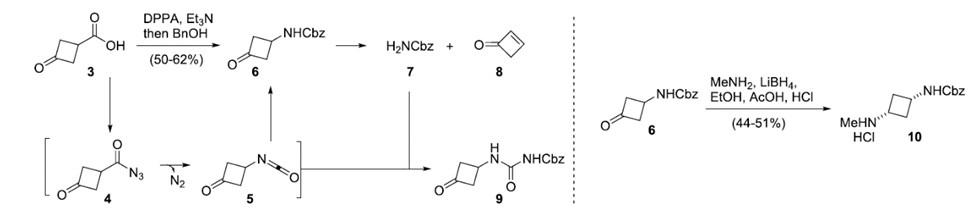
图二 利用Curtius重排来构建二氨基环丁烷10
图二是利用Curtius重排来构建二氨基环丁烷10的方案。在三乙胺存在下,环丁酮-3-羧酸3与二苯基磷酰叠氮(DPPA)反应生成酰基叠氮中间体4;加热酰基叠氮化物发生硝基重排生成异氰酸酯5,而异氰酸酯5被苯甲醇捕获生成苄基氨基甲酸酯6。由于6会分解,该反应中会存在7、8、9等副产物,研究人员通过多种优化,但未能成功有效避免这些副产物的生成。对于化合物6转化为中间体10,研究人员发现使用低温还原胺化有利于得到所需的顺式异构体10,可以得到4:1的非对映体。通过分离和连续重结晶可以使非对映体比率提高到>99:1。该方案未早期临床研究提供了公斤级的中间体6,但由于以上挑战,以及中间体4存在安全风险(爆炸),开发一种替代方法势在必行。
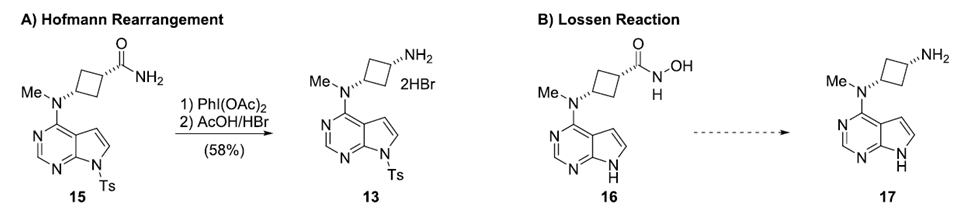
图三 替代硝烯型重排反应方案
Hofmann(霍夫曼)重排已在多公斤规模上使用,因此作为Curtius重排的替代方案进行了研究(图三A)。由于氧化剂与富含电子的吡咯嘧啶不相容,需要谨慎选择试剂、保护基团策略和反应条件。研究证明,以PhI(OAc)2做为氧化剂的条件是可行的,在醋酸中用HBr处理后,可以58%的产率得到二氢溴酸盐13。但由于该方法需要使用保护基,辉瑞公司并未采纳该方案。而与Curtius和Hofmann重排相比,Lossen重排反应需要的催化剂相对较少,因为氮是以羟肟酸形式引入(图三B)。通常使用的试剂是脱水剂,并且与无保护的吡咯嘧啶更相容。
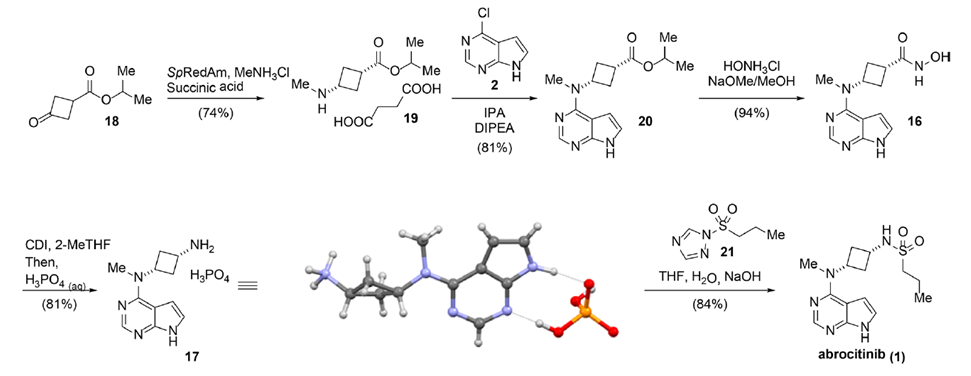
图四 Abroctinib改进合成工艺
以Lossen重排做为关键反应的Abroctinib改进合成工艺如图四所示,该反应在合成异丙酯中间体18后,经过还原胺化得到中间体19;而后与原料2发生取代反应得到中间体20;中间体20与羟胺盐酸盐反应得到中间体16;中间体16在CDI作用下发生Lossen重排得到关键二胺中间体17;研究人员通过单晶结构确认了中间体17的绝对构型;最后,中间体17与化合物21缩合即可得到目标产物Abroctinib。
通过改进后的合成工艺,辉瑞公司成功实现了Abroctinib的合成,并将在此基础上进行商业化路线开发。该工艺涉及步骤主要包括催化还原胺化以得到顺式环丁烷环、SNAr反应缩合未保护的吡咯嘧啶核、Lossen重排、以及使用新的磺酰转移试剂进行磺酰化,成功实现了产率、中间体性质、安全性的全面提升,为Abroctinib的未来需求提供了强有力的保障。
参考文献:
1. A Selective JAK1 Clinical Candidate for the Treatment of Autoimmune Diseases. J. Med. Chem. 2018, 61 (3), 1130?1152;
2. Development of a Nitrene-Type Rearrangement for the Commercial Route of the JAK1 Inhibitor Abrocitinib, Org. Process Res. Dev. 2020.
作者简介:云天,药物化学博士,主要从事小分子药物研究,尤其擅长小分子药物的合成工艺及后期药物开发研究,已完成多个抗癌药物分子的合成和活性评估。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57