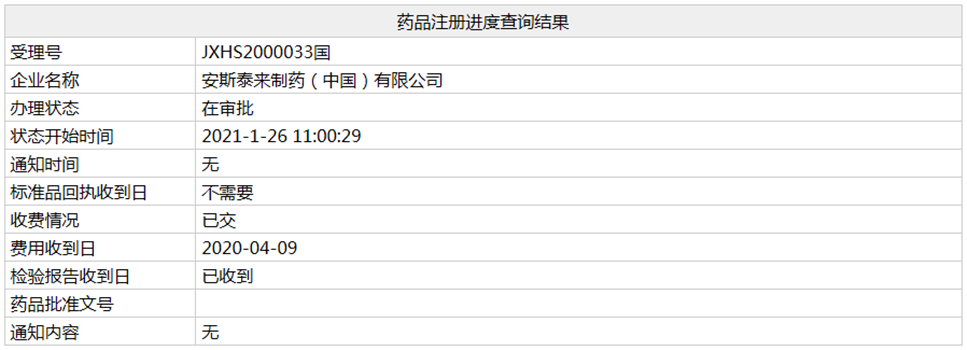
1月26日,安斯泰来「富马酸吉瑞替尼片」的上市申请(相关受理号为JXHS2000033)在NMPA的状态变更为"在审批",这意味着该药即将在国内获批,适应症为:治疗携带FLT3突变的复发性或难治性急性髓系白血病(AML)成人患者。
急性髓系白血病(AML)是一种影响血液和骨髓的癌症,其发病率随着年龄增长而增加,是成年人最常见的白血病类型之一。其中,FLT3-ITD突变影响约30%的AML患者,与恶化的无病生存和总体生存相关,而FLT3-TKD突变影响约7%的AML患者。研究发现,FLT3突变AML患者预后差,化疗后的生存期中位数不到6个月。近十年来,复发难治性AML的治疗进展缓慢,生存期短,并发症多,除了挽救性化疗、造血干细胞移植外,治疗手段十分有限,亟需新的有效治疗方法和药物。
吉瑞替尼(gilteritinib,Xospata)是安斯泰来与与日本寿制药株式会社合作发现的一款FMS样酪氨酸激酶3(FLT3)抑制剂,对FLT3跨膜区内部串联重复(ITD)和FLT3酪氨酸激酶结构域(TKD)2种不同的突变具有抑制作用。值得一提的是,该药曾在美国、日本、欧盟被授予了孤儿药资格,同时在美国还被授予快速通道资格,在日本被授予SAKIGAKE资格。
2018年10月,吉瑞替尼率先在日本被批准用于治疗FLT3突变的复发或难治性AML成人患者。随后,该药又先后于2018年11月和2019年10月在美国和欧洲获批。而吉瑞替尼在日本、美国和欧洲的获批均是基于ADMIRAL研究的结果。
ADMIRAL研究旨在评估Xospata与挽救性化疗治疗复发性或难治性FLT3mut+AML患者的疗效和安全性。其最新结果显示,与挽救性化疗组相比,Xospata治疗组患者总生存期(OS)显著延长(中位OS:9.3个月 vs 5.6个月,HR=0.64[95%CI:0.49-0.83],p=0.0004)、一年生存率提高一倍(37% vs 17%)、伴有完全或部分血液学恢复的完全缓解率提高一倍(34.0% vs 15.3%)。安全性方面,Xospata治疗组最常见的≥3级不良事件为发热性 中性粒细胞减少(45.9%)、贫血(40.7%)、血小板减少(22.8%)。
在国内,吉瑞替尼于2020年3月递交上市申请,2020年7月被CDE纳入优先审评范围,拟定适应症是:用于治疗携带FLT3突变的复发性或难治性急性髓系白血病(AML)成人患者。2020年11月,该药被CDE列入《第三批临床急需境外新药名单》。
在我国,据估计2018年有19,700例AML新增病例,预计到2030年将达到24,200例。如今,不满一年,吉瑞替尼的上市申请进入行政审批阶段,未来一旦正式获批,将为复发难治性AML患者提供一种新的选择。
安斯泰来拥有开发、制造、潜在商业化Xospata的独家全球权利,为了加速Xospata的推广,安斯泰来已于去年12月宣布与百洋医药携手加深合作,其中百洋将为吉瑞替尼提供从进口保税通关及仓储物流等一体化,以及全渠道商业化平台解决方案,全面提升FLT3突变的急性髓系白血病(AML)成年患者的用药可及性。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57