Part 1
国内仿制药研发批准动态
01
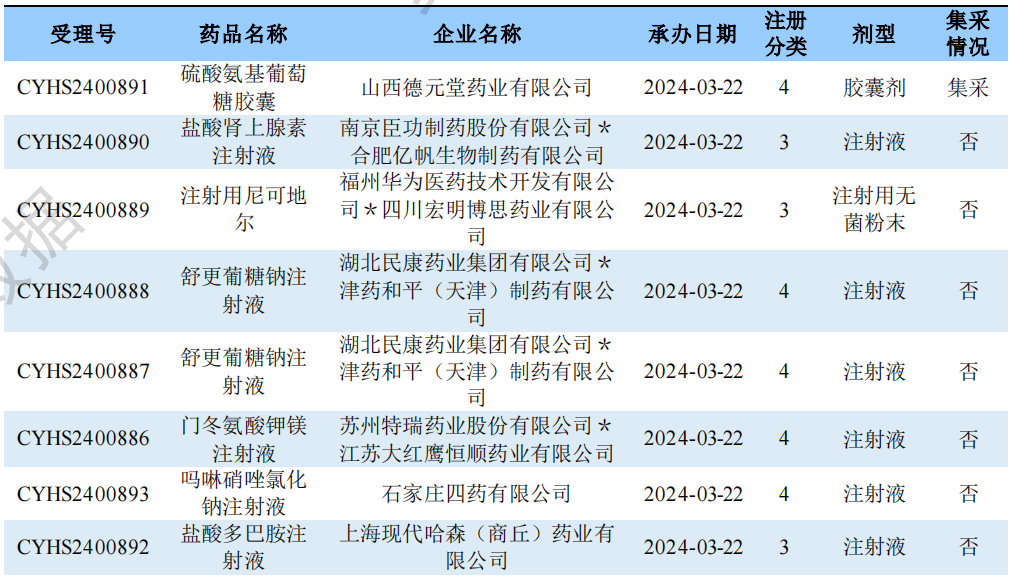
新注册分类品种首家批准上市情况
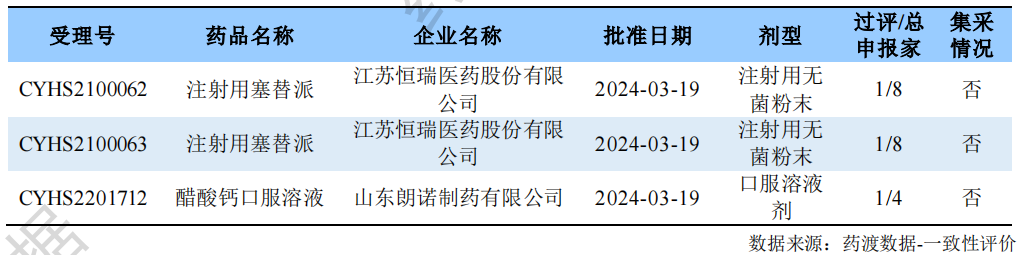
根据药渡数据调研,本次统计周期(2024.03.16-03.22)新增3个新注册分类首家过评受理号,涉及2个品种,包含1个注射剂,1个口服溶液剂,与上次统计周期相比,本次增加2个新注册分类首家过评品种。
新注册分类首家过评情况
02
一致性评价品种首家批准上市情况
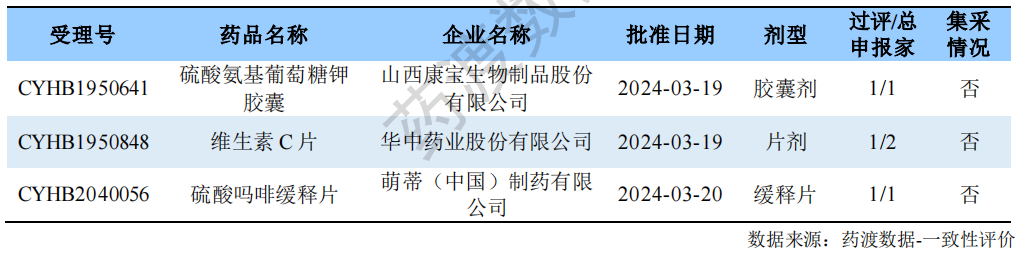
根据药渡数据调研,本次统计周期(2024.03.09-03.15)新增3个一致性评价首家过评受理号,涉及3个品种,包含1个胶囊剂,2个片剂。与上次统计周期相比,本次增加2个一致性评价首家过评品种。
一致性评价首家过评情况
03
新注册分类品种批准上市情况
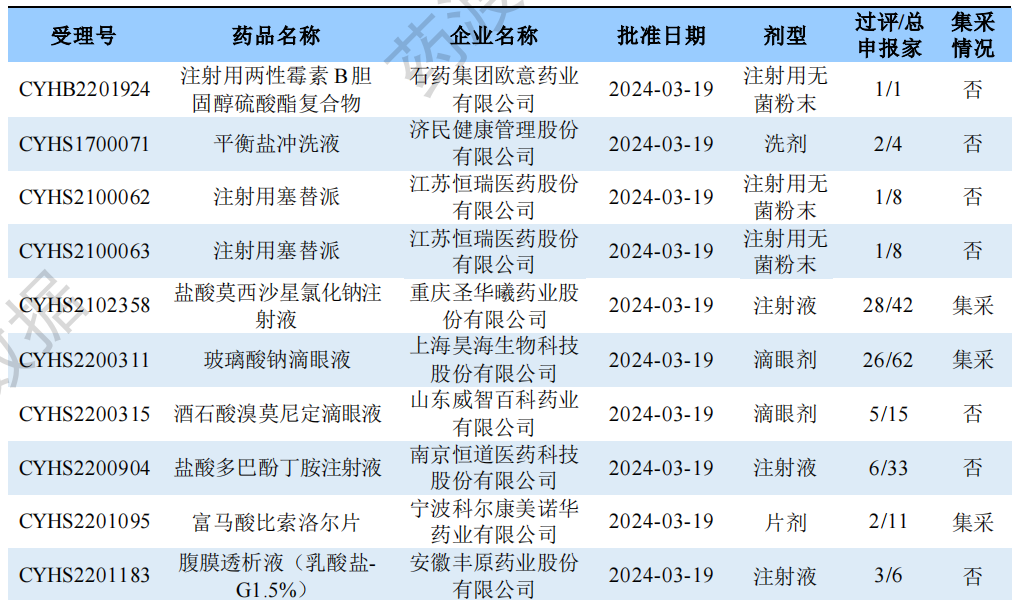
根据药渡数据调研,本次统计周期(2024.03.16-03.22)新注册分类新增26个过评受理号,涉及23个品种,包括3个滴眼剂,1个干混悬剂,1个口服溶液剂,6个片剂,1个吸入溶液剂,1个洗剂,10个注射剂。与上次统计周期相比,本次增加5个新注册分类过评品种。
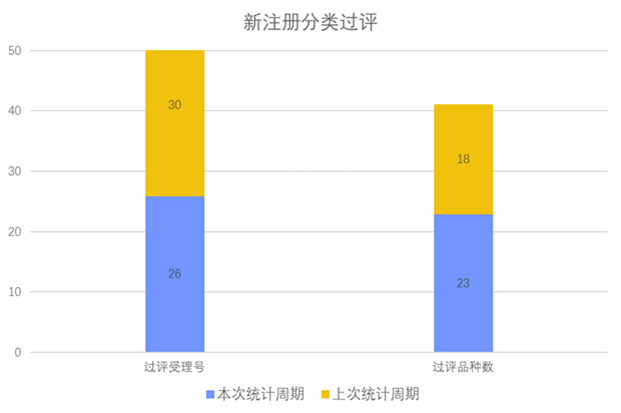
新注册分类品种过评情况(部分)
04
一致性评价品种批准上市情况
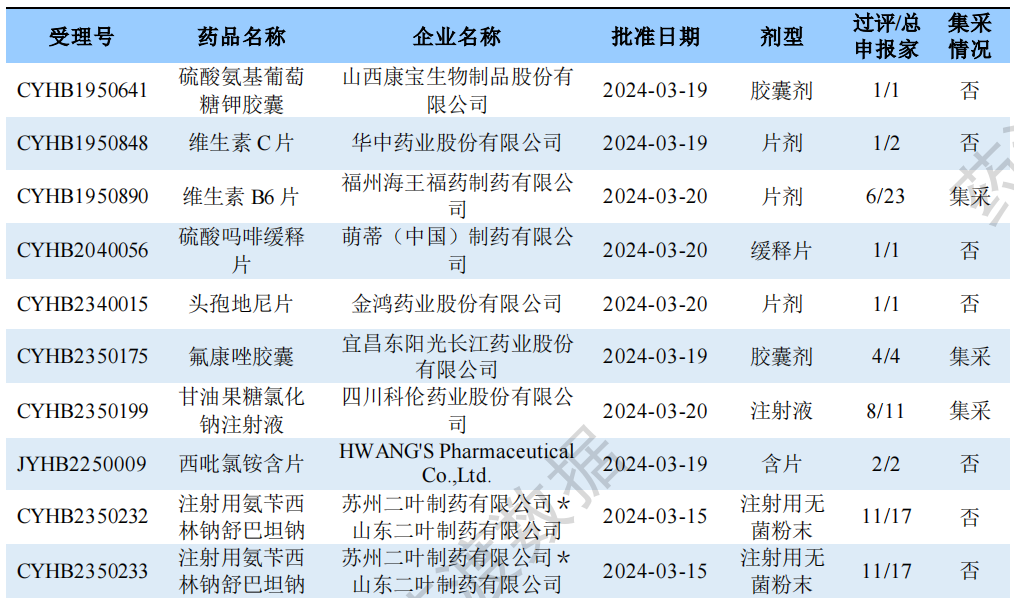
根据药渡数据调研,本次统计周期(2024.03.16-03.22)一致性评价新增12个过评受理号,涉及11个品种,包括3个胶囊剂,5个片剂,3个注射剂。与上次统计周期相比,本次增加7个一致性评价过评品种。
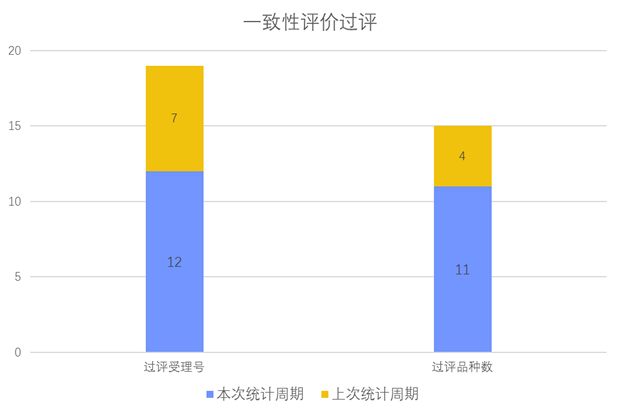
一致性评价品种过评情况
西吡氯胺含片
西吡氯铵属于一种阳离子季铵化合物,作为表面活性剂,具有广谱的抗菌作用。西吡氯铵含片临床上通常用于急性、亚急性咽炎,牙龈炎。西吡氯铵含片作为一种局部用药,能减少或抑制牙菌斑的形成,具有保持口腔清洁,清除口腔异味的作用;同时不会出现全身吸收,避免了全身用药,从而减少了全身不良反应的发生。
日本大正制药联合熊本大学的相关研究结果显示,西吡氯铵在浓度为0.05%时足以使新冠病毒的病毒颗粒膜破裂,抑制新冠病毒的复制和传播;同时,西吡氯铵能保持口腔内长久的适宜酸碱环境,进而改变口腔唾液pH值和提高唾液流速,可以明显减轻患者口干咽干症状,并有效地缓解咽痛和咽部充血等“刀片嗓”症状。
根据药渡数据库调研显示,目前国内共有3家企业拥有西吡氯铵含片的生产批文,其中台湾黄氏制药占据国内8成以上的市场份额,排名第2、3位的分别是山东新时代和四川健能,2022年度销售额为5610万元。成都倍特药业的新3类报产申请已获受理,正在等待进入审评审批流程。
后疫情时代,也许是欠了所谓“免疫债”,流感、普通感冒、支原体肺炎一波一波的等感染不断到来,对于咽干咽痛等典型感染症状,西吡氯铵含片未来市场可期。此次黄氏制药/郑州灏瑞医药继山东新时代药业拿下该品种的“第2家”过评称号,西吡氯铵含片的未来市场格局必将有所动荡,未来市场如何变幻,药渡将持续关注。
05
仿制药品种批准临床情况
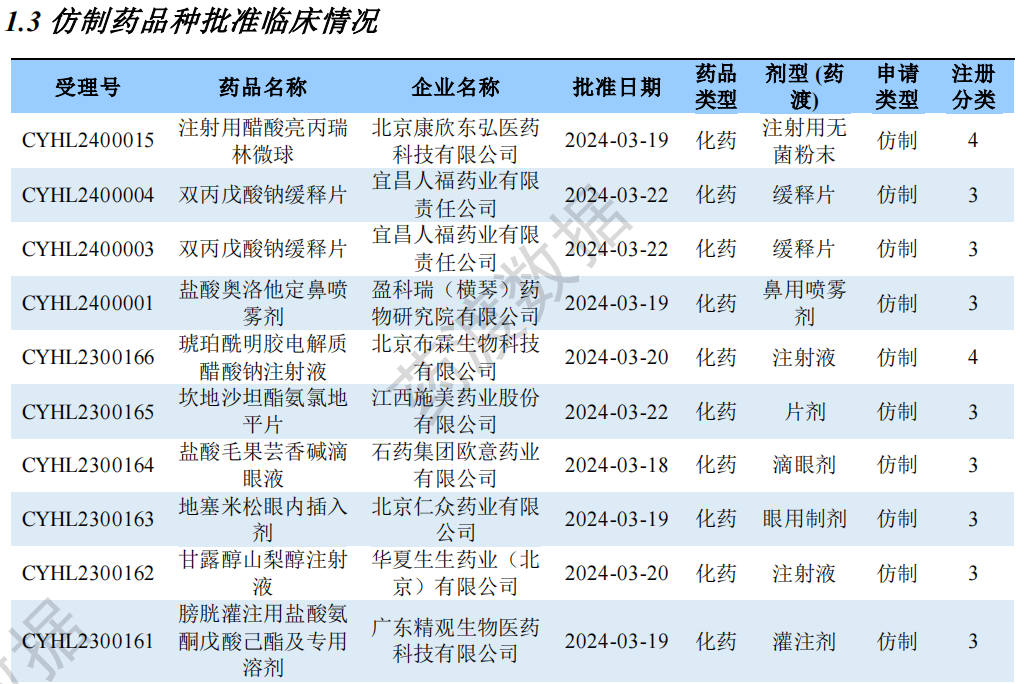
Part 2
国内仿制药研发批准动态
01
新注册分类品种申报上市情况
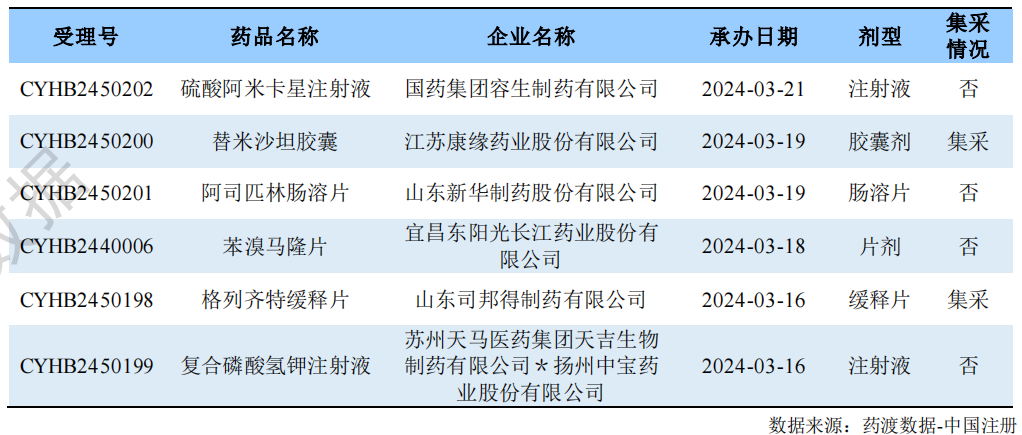
根据药渡数据调研,本次统计周期(2024.03.16-03.22)新注册分类数据新增47个新报受理号,涉及37个品种,包括1个滴眼剂,4个胶囊剂,1个颗粒剂,11个片剂,1个吸入喷雾剂,1个吸入溶液剂,18个注射剂。与上次统计周期相比,本次减少8个新注册分类申报品种。
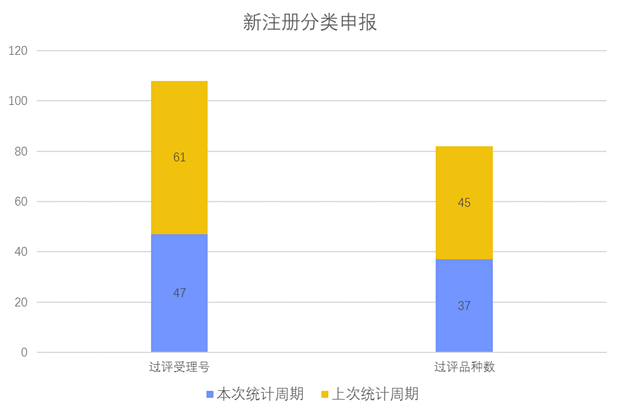
新注册分类品种申报受理情况(部分)
02
一致性评价品种申报上市情况
根据药渡数据调研,本次统计周期(2024.03.16-03.22)一致性评价数据新增6个新报受理号,涉及6个品种,包括1个胶囊剂,3个片剂,2个注射剂。与上次统计周期相比,本次增加2个一致性评价申报品种。
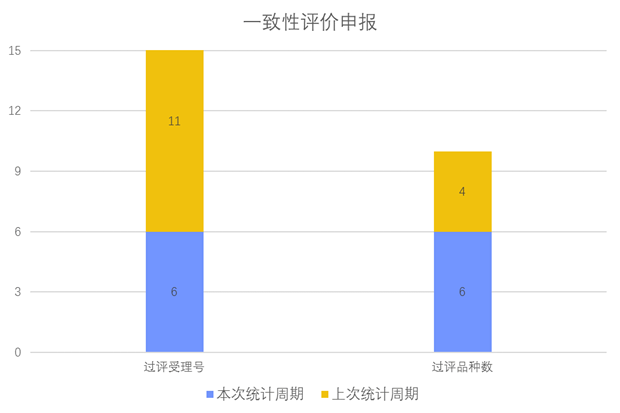
一致性评价申报受理情况
03
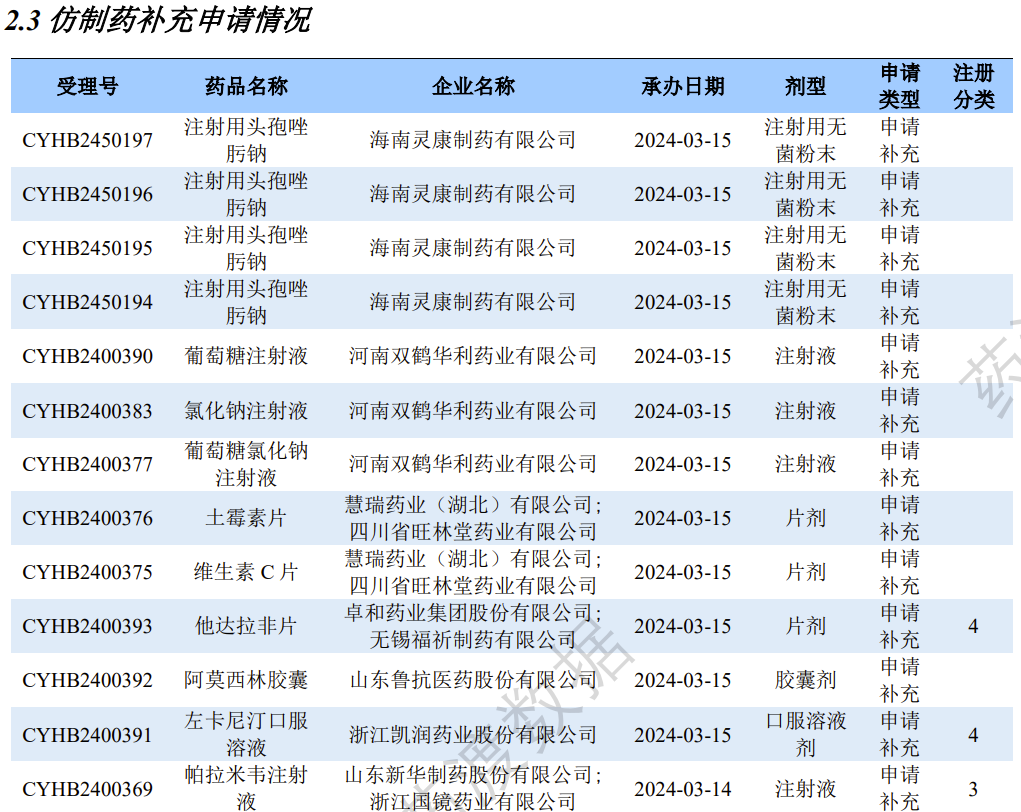
仿制药补充申请情况
04
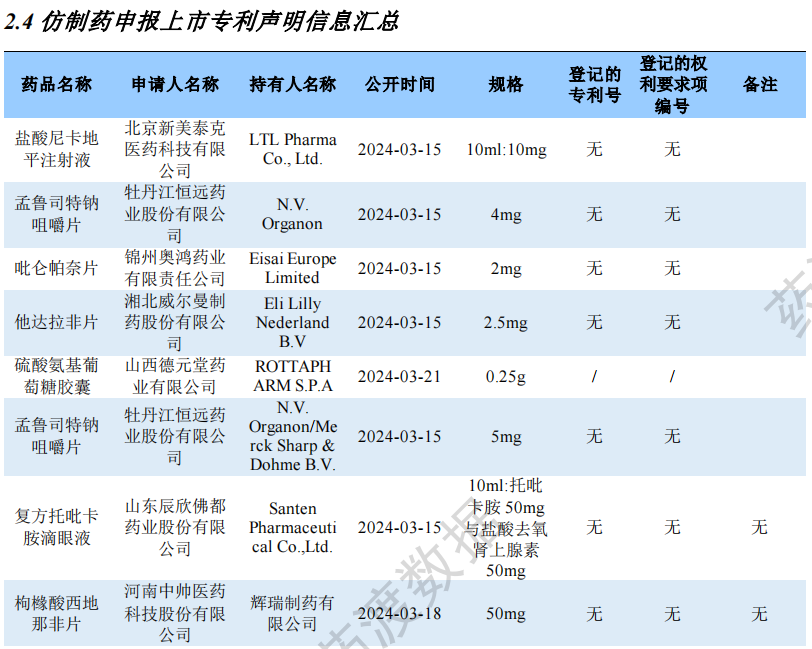
仿制药申报上市专利声明信息汇总
Part 3
国内仿制药研发领域热点聚焦
01
国内仿制药研发领域政策法规相关动态
关于公开征求《化学仿制药参比制剂目录(第八十批)》(征求意见稿)意见的通知
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第八十批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。公示期限:2024年03月18日~2024年03月29日(10个工作日)。
02
国内仿制药研发领域热点新闻
北陆药业:关于钆贝葡胺注射液通过一致性评价的公告
2024 年3月19日,北京北陆药业股份有限公司发布公告称,公司于近日收到国家药品监督管理局颁发的关于钆贝葡胺注射液的《药品补充申请批准通知书》(通知书编号:2024B01144),钆贝葡胺注射液通过仿制药质量和疗效一致性评价。现将有关事宜公告如下:
一、药品基本情况
药品通用名称:钆贝葡胺注射液
剂型:注射剂
规格:10 ml : 5.290 g 钆贝葡胺(相当于钆贝酸 3.340 g,葡甲胺1.950 g)
注册分类:化学药品
原药品批准文号:国药准字H20203008
包装规格:1瓶/盒,10 瓶/盒
药品注册标准编号:YBH04772024
审批结论:经审查,本品通过仿制药质量和疗效一致性评价。
二、药品相关信息
钆贝葡胺注射液是一种适用于肝脏、中枢神经系统和血管的诊断性磁共振成像(MRI)的顺磁性对比剂。根据相关网数据显示,钆贝葡胺注射液在中国公立医疗机构终端的销售额近年来呈逐年上涨态势,2022 年超过1.6 亿元,2023 上半年以约 16.6%的增速继续上涨。钆贝葡胺注射液是由意大利 BraccoImaging S.P.A.公司研发,目前包括公司在内已有 2 家企业通过或视同通过仿制药质量和疗效一致性评价。
三、对公司影响及风险提示
公司产品钆贝葡胺注射液通过仿制药注射剂质量和疗效一致性评价,是国家药品监管部门对公司研发、生产综合能力和产品质量的认可,为公司后续其他仿制药一致性评价工作再次积累了宝贵经验,对公司研发能力的提升具有积极意义。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57