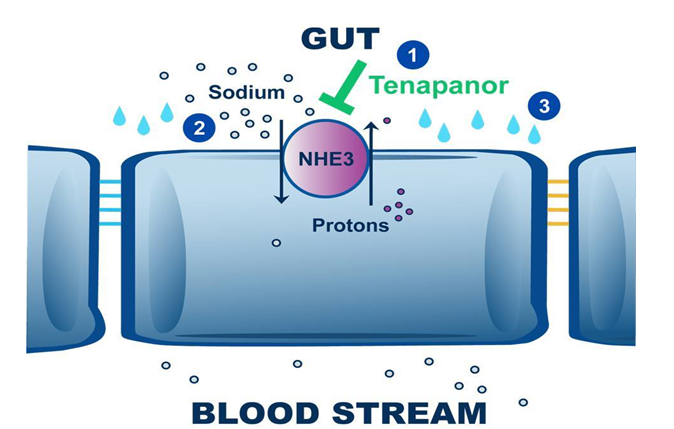
近日,Ardelyx公司在研药物Tenapanor用于治疗便秘型肠易激综合征(IBS-C)的新药申请获得FDA批准,这意味着为IBS-C患者从此再多一新选择。作为肠道钠/质子交换器亚型3 (NHE3)的抑制剂,Tenapanor通过抑制或阻断胃肠道(GI) NHE3的转运而减少饮食中钠的吸收,导致肠道内钠离子增加,从而增加肠道的液体,减轻便秘症状(详细作用机制见下图)。去年11月FDA就已受理了Tenapanor用于治疗IBS-C的新药申请,如今作为首 个治疗IBS-C的NHE3抑制剂类药物,公司预计其上市后的峰值销售额有望达到4-5亿美元。
Ardelyx是一家专注于胃肠道疾病和心肾疾病领域的生物制药公司,成立于2007年,2014年在纳克达斯上市。2012年,阿斯利康以2亿7千万美元的高价与Ardelyx公司达成合作协议开发tenapanor,然而2015年tenapanor在治疗慢性肾病和二型糖尿病的临床试验惨遭滑铁卢,最终导致Ardelyx与阿斯利康分手,后又将tenapanor从阿斯利康公司手中赎回独自开发,并将适应症对准高磷血症和IBS-C。2017年复星医药与Ardelyx签订《License Agreement》,获得在区域内(即中国大陆、中国香港及中国澳门特别行政区)及领域内(即治疗、诊断及预防与便秘型肠易激综合征、终末期肾病高磷血症,以及其他美国食品药品管理局和/或国家食品药品监督管理总局批准的其他适应症)独家临床开发和商业化NHE3受体抑制剂Tenapanor药物制剂的权利。
此次tenapanor提交的新药申请是基于两项的3期临床试验,其中第一项3期临床T3MPO-1达到预期,第二项3期临床T3MPO-2达到主要终点和所有次要终点,T3MPO-2是一个为期26周、双盲、安慰剂对照、多中心的随机临床试验,主要终点为12周中6周的联合应答率,共包括593名满足ROME III诊断标准的IBS-C患者,试验中患者随机分配到治疗组(n = 293)和安慰剂组(n = 300),每日两次接受50毫克的tenapanor或安慰剂。试验包括为期两周的筛查期,在此期间,患者每日以电话日记的形式记录肠道运动频率和腹痛评分。最终试验结果显示:在12周中至少有6周的时间,与安慰剂组相比,更多的tenapanor治疗组患者 (36.5%比23.7%,p < 0.001) 腹痛减少至少30%,在一周之内,接受治疗的患者增加至少一次或多次完整自然排便 (CSBM) 。此外,在12个周中的6周和9周期间内,tenapanor对CSBM和腹痛缓解率均有统计学意义,并且在整个26周的研究中都有一致的反应。
然而T3MPO-1和T3MPO-2两个临床研究都暴露出一个问题,试验中有相当比例的患者出现了腹泻的副作用,且有患者因腹泻导致临床治疗中断。除了上述两项临床试验,Ardelyx又继续开展一项名为T3MPO-3的长期研究,试验中约有9.2%的患者出现了腹泻的情况,1.7%的患者因腹泻中断治疗,总停药率仅为2.1%。最终结果显示tenapanor治疗的平均达标率约98%,且在接受治疗的240名患者中具有良好的耐受性。该项临床试验表明tenapanor腹泻的副作用发生在治疗的早期,但随着时间的延长会逐渐回归正常。
Tenapanor不仅对IBS-C患者有效,tenapanor联合磷酸盐粘合剂,还可显著降低患者血液中的磷酸盐水平,且9月初,Ardelyx就宣布tenapanor治疗透析患者高磷血症的关键性3期临床试验达到主要终点和所有次要终点,预计Ardelyx也将会尽快提交tenapanor用于治疗高磷血症的适应症申请。
关于IBS-C及其获批药物
肠易激综合征(IBS)是一种以腹痛、腹胀或腹部不适为主要症状的功能性肠病,常伴有排便习惯(频率和/或性状)的改变,根据主要异常排便习惯,可分为IBS便秘型(IBS-C)、IBS腹泻型(IBS-D)、IBS混合型(IBS-M)和IBS不定型(IBS-U)4个主要亚型。2015年调查数据显示全球IBS患病率为1.1%-45%,且女性发病率高于男性。
当前便秘型肠易激综合征(IBS-C)的临床治疗药物主要为泻剂、促动力剂和促分泌剂,其中泻药主要用于改善IBS-C患者的便秘症状,适用于轻、中度便秘,且既往的研究表明,容积性泻剂可能会加重腹胀和腹痛症状,刺激性泻剂会导致腹部绞痛,渗透性泻剂中乳果糖会增加腹胀症状。促动力药通过刺激胃肠蠕动、加快胃肠传输来改善慢性便秘症状,适用于腹胀、胀气和便秘型IBS。而促分泌剂通过促进肠液分泌,增加粪便含水量而增加排便频率,作为IBS-C新型的治疗药物,具有靶点和作用机制明确、特异性高、不良作用小等独特优势。
在此之前,FDA批准用于治疗IBS-C的药物包括Ironwood公司的利那洛肽(Linaclotide,商品名Linzess)、诺华的替加色罗(tegaserod,商品名Zelnorm)和Sucampo医药公司的鲁比前列酮(Lubiprostone,商品名Amitiza),详见下表:

替加色罗是唯一被批准用于治疗IBS-C的选择性血清素-4(5-HT4)受体激动剂,不但可促进胃肠动力,而且可调节内脏对疼痛的感觉。于2002年首次获得FDA批准(商品名为Zelnorm),2003年4月在国内获批(商品名为泽马可)。该药通过激活5HT4受体来促进乙酰胆碱的释放,进而促进胃肠道的蠕动和分泌。但由于其潜在的心血管(CV)安全问题,曾一度被暂停销售,撤出市场。2007年7月FDA又限制使用替加色罗用于满足特定指导原则的女性IBS-C患者及55岁以下的慢性特发性便秘(CIC)患者,目前FDA又批准重新引入替加色罗口服片剂用于治疗小于65岁的女性的IBS-C。
鲁比前列酮是一种氯离子通道激活剂,可活化胃肠道细胞膜上的CIC-2,增加肠液的分泌和肠道的运动性。2006年被FDA批准治疗慢性特发性便秘,2008 被FDA批准用于女性IBS-C患者。2013-2017年的全球销售额在2-4亿美元之间。
利那洛肽是Ironwood制药研发的含有14个氨基酸残基,是FDA批准全球首 个鸟苷酸环化酶-C(GC-C)受体激动剂,于2012年8月被FDA批准用于治疗成人慢性特发性便秘(CIC)和IBS-C,商品名为Linzess,由Ironwood与艾尔健(Allergan)联合营销。在欧洲,其商品名为Constella,由艾尔健负责营销。在日本,由安斯泰来负责其在日本市场的开发及商业化(2009年两家达成该协议)。今年1月国家NMPA批准利那洛肽用于治疗IBS-C,商品名为令泽舒®,由阿斯利康与Ironwood制药(两家2012年达成合作协议)共同负责令泽舒?在中国的开发及上市推广。利那洛肽可谓是便秘治疗领域品牌药处方市场的领导者,自2012年上市以来,已有近150万患者接受了近700万处方的治疗。而且利那洛肽有一项加框警告,提示患者和医务人员该药不应用于年龄≤17岁的患者。
除上述三款获批药物,Synergy制药公司的普卡那肽(plecanatide)治疗IBS-C的申请正在审评中,原本预计去年获批,但至今还未传来获批消息。普卡那肽是含16个氨基酸残基的多肽,最初由美国Callisto制药公司研制,后转让给Synergy制药公司开发,2017年1月被FDA批准用于治疗CIC患者,商品名Trulance。2018年8月,罗欣药业与Synergy制药达成许可协议,获得在中国大陆、中国香港和中国澳门独家开发和销售普卡那肽的权利。汤森路透预测其在2020年将4亿美元的销售额。
参考资料:
[1] Ardelyx (ARDX) Shares Soared After Positive Phase III Results for Tenapanor
[2] Suares NC, Ford AC. Prevalence of and risk factors for chronic idiopathic constipation in the community: systematic review and meta-analysis. Am J Gastroenterol. 2011;106:1582-1591.
[3] Alexander C. etal. American College of Gastroenterology monograph on the management of irritable bowel syndrome and chronic idiopathic constipation. Am J Gastroenterol 2014 Aug;109 Suppl 1:S2-26



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57