近日,阿斯利康SGLT-2抑制剂达格列净片的上市申请(相关受理号为:JXHS2000027/28)在NMPA的状态变更为"在审批",这意味达格列净即将在国内获批用于治疗射血分数降低的心力衰竭(HFrEF)成人患者,以降低心血管死亡和心力衰竭恶化风险,并改善心力衰竭症状。
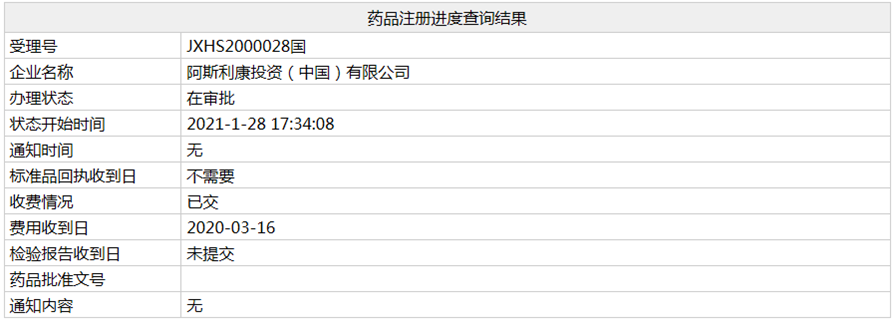
值得一提的是,前几日达格列净刚在国内递交新适应症上市申请,相关受理号为:JXHS2100009/10。据该药在国内外的审批进度,笔者推测新申报的适应症是:慢性肾 脏疾病(CKD),无论患者是否患有2型糖尿病。
心力衰竭(HF)是一种危及生命的慢性疾病,影响全球约6400万人,过半的患者会在诊断后的五年内死亡。根据射血分数(EF:即每搏输出量占心室舒张末期容积量的百分比)的数值,心衰可分为两大类,即射血分数降低型心衰(HFrEF)和射血分数保留型心衰(HFpEF),其中射血分数降低型心衰表现为左心室心肌未能充分收缩进而使得循环及外周组织的血液供应减少。心衰是65岁以上患者住院的主要原因之一,为患者带来了巨大的经济负担。
达格列净(dapagliflozin,Forxiga(欧盟)/Farxiga(美国))是一款每日仅需口服一次的选择性钠-葡萄糖协同转运蛋白2(SGLT-2)抑制剂,独立于胰岛素发挥作用,在肾 脏中选择性抑制SGLT-2,不仅可以帮助患者从尿液中排出多余的葡萄糖,而且还具有减肥、降低血压的额外益处。
作为全球批准的首 款SGLT-2抑制剂,达格列净最早于2012年11月在欧盟被批准用于辅助饮食和运动,控制II型糖尿病成人患者的血糖,随后上述适应症于2014年1月在美国获批。随后,该药又于2019年3月在欧盟和日本被批准作为胰岛素的口服辅助治疗药物,用于1型糖尿病成人患者的治疗,具体适应症为:作为胰岛素的口服辅助治疗药物,用于接受胰岛素治疗但血糖水平控制不佳并且身体质量指数(BMI)≥27kg/m2(超重或肥胖)1型糖尿病(T1D)成人患者,改善其血糖控制,这又使其成为首 个被批准治疗T1D的SGLT-2抑制剂。但因糖尿病酮症酸中毒(DKA)风险,该适应症在美国拒批。
研究发现:心脏、肾 脏和胰 腺之间存在密切联系,达格列净也被推进用于心肾事件的预防。近年来,达格列净在拓展适应方面频频传来捷报。
♦ 2019年8月,被FDA授予快速通道资格(FTD),用于伴或不伴2型糖尿病的慢性肾 脏病(CKD)患者,延缓肾功能衰竭进展以及预防CV和肾 脏死亡。
♦ 2019年10月,被FDA批准用于降低患有2型糖尿病和其他心血管疾病风险的成年人因心力衰竭而住院的风险。
♦ 2020年5月,被FDA批准该药用于射血分数降低的心力衰竭(HFrEF)成人患者(伴或不伴2型糖尿病),以降低心血管(CV)死亡和心衰住院的风险。
♦ 2020年10月,被FDA授予治疗CKD的突破性 药物资格。
♦ 2020年11月,达格列净先后在欧盟和日本被批准用于治疗射血分数降低的心力衰竭。
♦ 2021年1月,治疗CKD的上市申请被FDA授予优先审评资格。
达格列净是全球首 个获批治疗心衰的SGLT2抑制剂。若CKD适应症获批,达格列净将再斩获首 个,成为首 个获批治疗CKD的SGLT2抑制剂。除此之外,达格列净还被评估用于HFpEF,预计研究数据将于2021年下半年公布。
达格列净在国外获批治疗HFrEF是基于DAPA-HF研究的结果。该研究是一项国际、多中心、平行分组、随机、双盲III期研究,在4744名心力衰竭且射血分数降低(LVEF≤40%)的患者(无论是否患有2型糖尿病)中展开,旨在评估在标准治疗基础上加用达格列净 10mg每日一次与安慰剂相比的疗效。主要复合终点是首次出现心衰恶化事件(住院或同等事件,如心衰紧急就诊)或心血管死亡。中位随访时间为18.2个月。
结果显示:在标准治疗基础上加用达格列净,与安慰剂相比,可将复合结局的风险降低26%,全因死亡风险降低17%。而安全性与该药物过去安全性研究中的表现一致。
在国内,达格列净最早于2017年3月被NMPA批准作为一种单药疗法,用于2型糖尿病成人患者改善其血糖控制,商品名为安达唐,成为国内批准的首 个SGLT2抑制剂。2019年,达格列净经过医保谈判,最终以全球最 低价格4.36元/片(10mg)、2.56元/片(5mg)进入国家医保,且成功续约2020年医保。此外,达格列净还在国内递交了4个上市申请,其中2019年6月CDE受理的上市申请已被拒批,具体适应症未知。
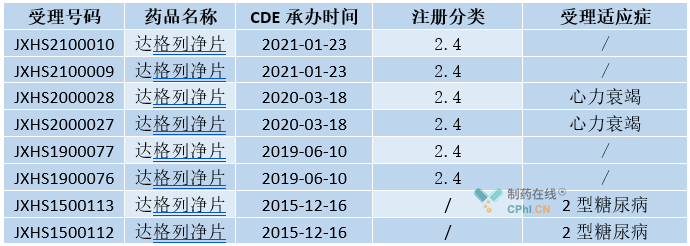
据公司财报,达格列净上市后销售额逐年攀升,于2017年突破10亿美元大关,成为重磅级产品,但近几年来,达格列净销售额年增长率逐渐下滑,销售额仍未突破20亿美元。近年来随着新适应症的顺利获批,预计达格列净销售额有望再创新高。
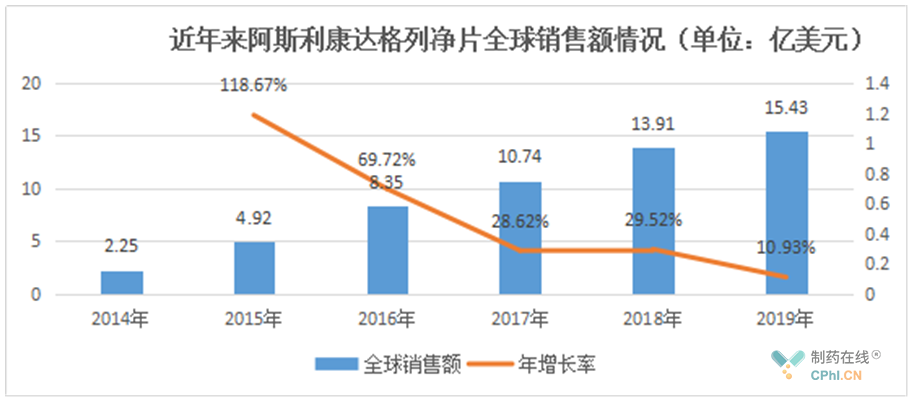
不过,对于达格列净的市场预期也不能太过乐观。据悉,达格列净的化合物中国专利CN03811353.8与药用丙二醇水合物晶型中国专利CN200780024135.X分别将于2023年5月与2027年6月到期,但目前已有企业开始布局。其中,鲁抗医药、印度阿兰宾度制药和福元医药已先后递交了仿制药上市申请,双鹭药业正在进行BE试验,此外,还有十余家企业获批临床。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57