3月9日,CDE官网显示,辰欣药业4类仿制药特立氟胺片的上市申请获受理,这是继海纳制药 /盛世泰科之后,国内第二家特立氟胺仿制药报产。

原研特立氟胺(Teriflunomide)是赛诺菲开发的一种口服嘧啶合成酶抑制剂和免疫调节剂,主要通过抑制二氢乳清酸脱氢酶阻止淋巴细胞中嘧啶的合成。2012年9月,该药在美国被批准用于治疗成人复发型 多发性硬化(商品名为 Aubagio),2013 年 9 月在欧盟批准用于治疗成人复发-缓解型多发性硬化。
多发性硬化(MS)是一种严重、终身、进行性、致残性的中枢神经系统脱髓鞘疾病。根据病程,MS可分为四型,即复发缓解型(RR)、继发进展型(SP)、原发进展型(PP)和进展复发型(PR),其中复发缓解型最常见,约占 85%。据统计,全球约有2000多万MS患者,国内大约有3万多确诊MS患者。
目前,MS无法治愈,只能通过急性期激素冲击治疗和疾病修正治疗(DMT),控制炎症反应,抑制免疫细胞活性,从而达到减少复发次数、延缓病情进展、改善预后的目的。截止目前,全球已经批准多款DMT药物如干扰素β-1b特立氟胺、芬戈莫德、富马酸二甲酯、西尼莫德和奥扎莫德等。
特立氟胺使用方便,每天仅需口服一次,目前已在全球70多个国家和地区获批上市。据赛诺菲财报, Aubagio上市后销售额一直处于增长状态,2020年达到20.45亿欧元(约24.8亿美元),成为赛诺菲2020年销售额排名第三的重磅产品。
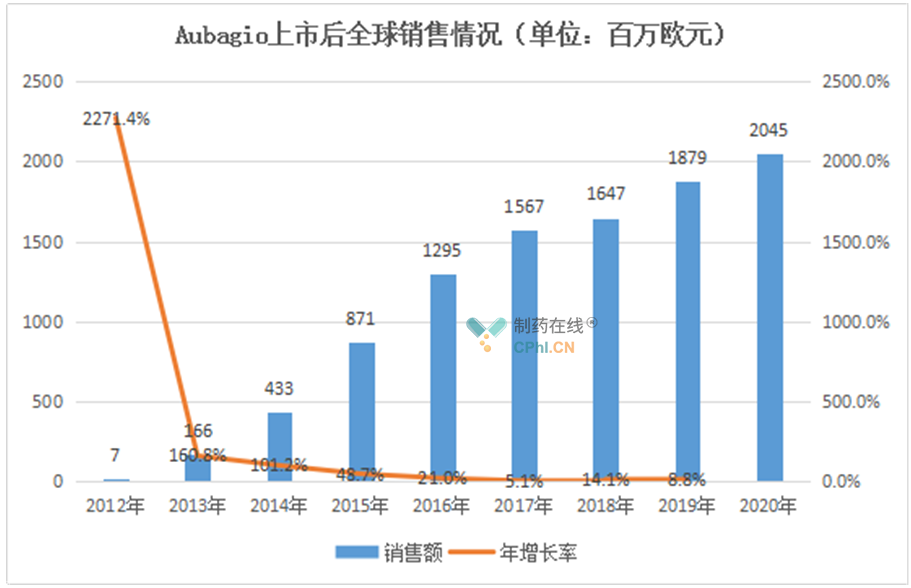
在国内,特立氟胺于2018年7月被NMPA批准用于治疗复发型MS,商品名为奥巴捷,成为我国首 个获批上市的口服DMT药物。2019年,该药被纳入国家医保目录,2020年被NMPA批准用于治疗临床孤立综合征(CIS)。CIS是多种脱髓鞘疾病的首发表现,约50%~85%的CIS患者会演变成RRMS,其中又有15%的患者会进一步发展为SPMS。
目前,特立氟胺已被《中国多发性硬化专家共识》(2018年版)推荐为DMT中的一线口服治疗药物。其TOWER研究的中国人群亚组显示,特立氟胺14mg可降低年复发率(ARR)达到71.2%,在中国的真实世界证据(RWE)数据中,回顾性研究2018-2020年武汉地区使用特立氟胺的病人,且病程大于6个月,其ARR下降幅度达75%以上。
据悉,一盒(14mg*28片)特立氟胺的价格为8290元,对于需要长期服药的MS患者来说仍是不小的负担。据insight数据库,目前国内已有多家企业布局特立氟胺仿制药市场,其中海纳制药 /盛世泰科和辰欣药业已经递交上市申请,瑞阳制药处于BE试验阶段,此外还有4家批准临床,1家申请临床试验。未来一旦有仿制药获批上市,特立氟胺的价格将会出现明显下降,届时将会惠及更多的MS患者。
此外,值得一提的是,随着国家对罕见病的重视以及审批制度的改革,近年我国已经批准有多款口服DMT药物,如芬戈莫德(商品名:捷灵亚)、西尼莫德(商品名:万立能)和特立氟胺等,其中芬戈莫德和西尼莫德成功入围2020年医保。
不过,目前列入《临床急需境外新药名单》4款MS药物,还有三款未获批,其中富马酸二甲酯(商品名:Tecfidera)由渤健研发,最早于2013年3月在美国获批,2014年1月在欧洲获批,目前在国内已经报产。该药治疗MS的作用机制尚不完全清楚,一般认为富马酸二甲酯(DMF)降解成其活性代谢产物富马酸单甲酯(MMF),MMF上调核因子Nrf2通路,Nrf2通路与氧化应激应答有关。达伐吡啶(商品名为Ampyra)由AcordaTherapeutics研发,2010年1月在美国获批,2011年7月在欧洲获批,该药是一种广谱钾通道阻滞剂,其作用机制尚未完全阐明,在动物研究实验中, 达伐吡啶被证明能够通过抑制钾离子通道而增加脱髓鞘轴突的动作电位的传导,改善MS患者的步行状态,目前该原研药未在国内有任何进展。阿仑单抗是健赞开发的一种针对单核细胞和淋巴细胞表面CD52的单克隆抗体,2013年9月在欧洲被批准用于活动性RRMS,商品名为Lemtrada,2001年5月在美国获批。不过该药有严重的不良反应,特别是继发性自身免疫性疾病,目前该药已经在国内获批临床。
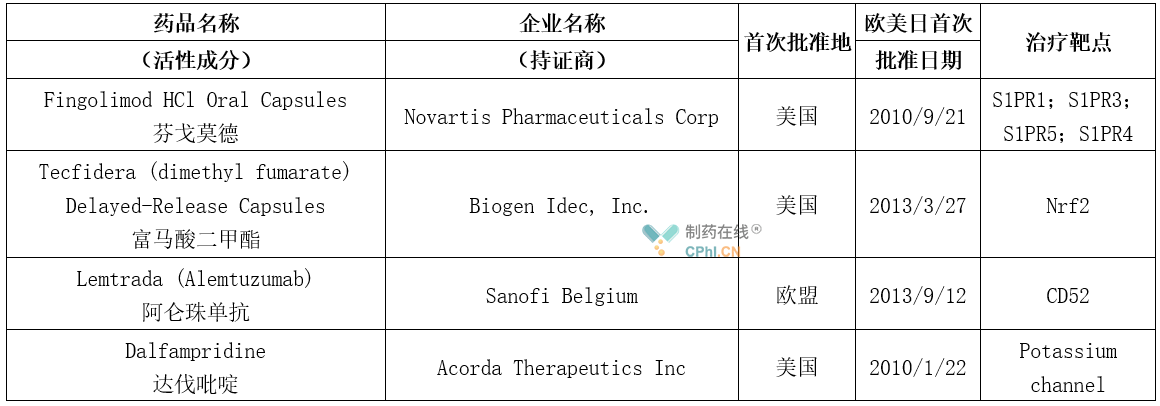
据悉,我国MS患者使用标准 DMT治疗比例仅有10%,远低于欧美国家的 DMT 使用率(86%)。期待未来有更多的MS药物获批,造福众多MS患者。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57