日前,扬子江药业集团瑞戈非尼片的4类仿制药上市申请获CDE受理,成为国内首家递交该品种仿制药上市申请的企业。

原研瑞戈非尼(regorafenib,Stivarga)是拜耳开发的一款多靶点激酶抑制剂,除能阻断促血管生成激酶 VEGFR 1-3,还可以阻断肿瘤微环境中的多种激酶,如TIE-2、RAF-1、BRAF V600、KIT、 RET、 PDGFR及FGFR,这些激酶单独和联合调控肿瘤的生长、基质微环境的形成及疾病的进展。
截止目前,Stivarga已经获批多种适应症,(1)既往接受过以氟尿嘧啶、奥沙利铂和伊立替康为基础的化疗、抗 VEGF 治疗和如果是野生型KRAS患者,接受抗EGFR治疗的转移性结直肠癌(CRC)患者(FDA 2012/09,EMA 2013/09);(2)不能手术摘除和Gleevec 、Sutent 药物治疗无效的胃肠道恶性间质瘤(GIST)患者(FDA 2013/02,EMA 2014/07);(3)曾使用多吉美(索拉菲尼)进行治疗,但病情依然未得到有效控制的肝癌患者(FDA 2017/04,EMA 2017/08)。
此外,2019年6月,拜耳与基石药业合作,评估Stivarga与基石药业PD-L1单克隆抗体CS1001联合治疗包括胃癌等多种癌症的安全性、耐受性、药代动力学(PK)以及抗肿瘤活性。同年7月,拜耳又与百时美施贵宝和小野制药签署临床合作协议,评估Stivarga联合Opdivo用于治疗微卫星稳定性转移性结直肠癌(MSS mCRC)的疗效。
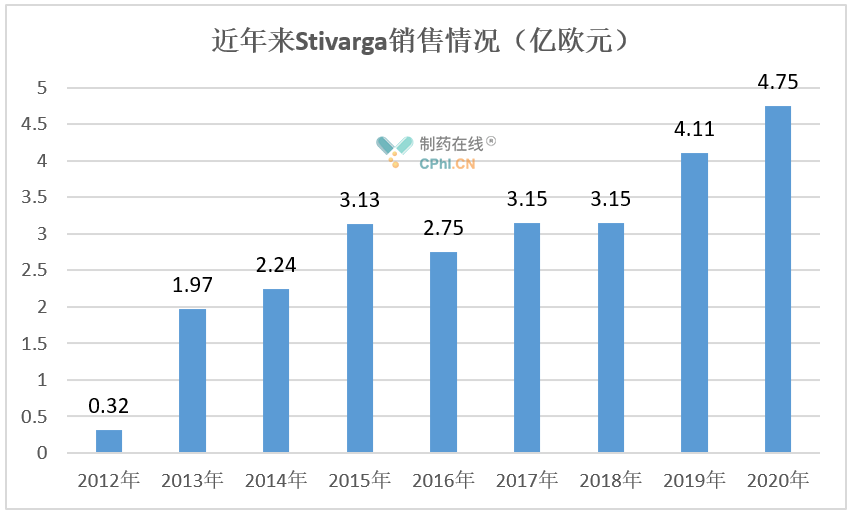
Stivarga由拜耳和Onyx制药(2013年8月被安进收购)共同推广,目前已在全球100多个国家获批上市,惠及20多万肿瘤患者。据拜耳财报,该药自上市后整体保持增长趋势,2020年销售额达4.75亿欧元。
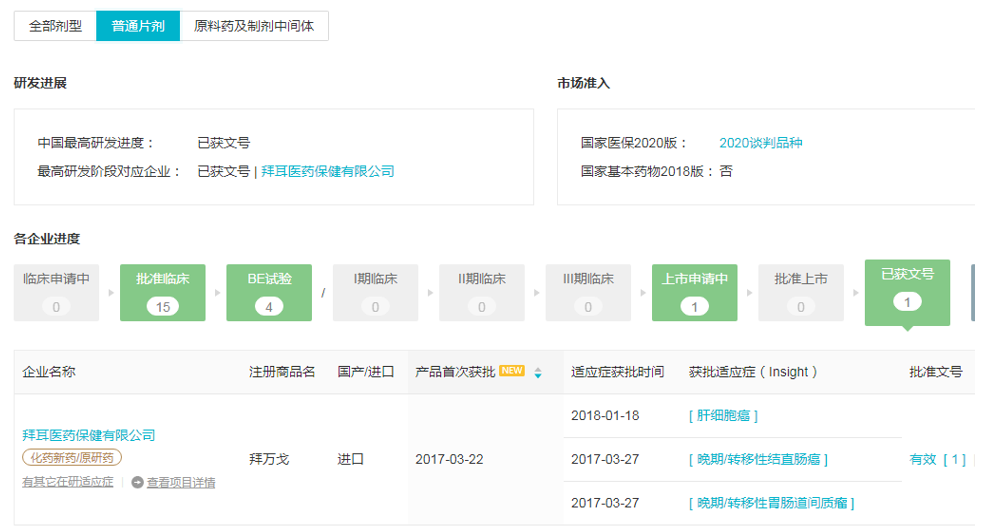
在国内,原研瑞戈非尼(商品名:拜万戈)于2017年5月被NMPA批准用于治疗晚期/转移性结直肠癌和胃肠道间质瘤,2018年1月又被批准用于治疗曾接受过索拉非尼治疗的肝细胞癌患者,2018年10月进入国家医保,而且成功续约2020年国家医保,且再次降价。
在肝癌治疗领域,瑞戈非尼作为首 个创新二线靶向治疗药物,开启了肝癌药物全程管理的时代,亚洲人群数据显示单药治疗组患者生存时间长达16.3个月,中国数据显示索拉非尼+瑞戈非尼序贯方案生存时间长达35.3个月;在转移性结直肠癌治疗领域,中国真实世界研究显示瑞戈非尼120mg剂量组生存获益长达16.7个月。目前,瑞戈非尼是2019版原发肝癌国家规范推荐的肝癌二线唯一标准治疗和结直肠癌、胃肠间质瘤各大规范指南推荐的三线标准治疗。
据米内网数据,瑞戈非尼2018年、2019年在国内城市公立医院终端销售额分别为3017万元(+13017.39%)和3.76亿元(+1146.57%),2020年销售额再创新高,仅上半年销售额就达到3.22亿元。
目前,据insight数据库国内已有多家企业开始布局瑞戈非尼市场,其中扬子江药业进展最快,已递交上市申请,据其进行的生物等效性试验推测申报的适应症是结直肠癌、胃肠道间质瘤和肝细胞癌。齐鲁制药、南京正大天晴、北京双鹭药业、湖南科伦制药正在进行BE试验,此外还有15家企业已经获批临床。
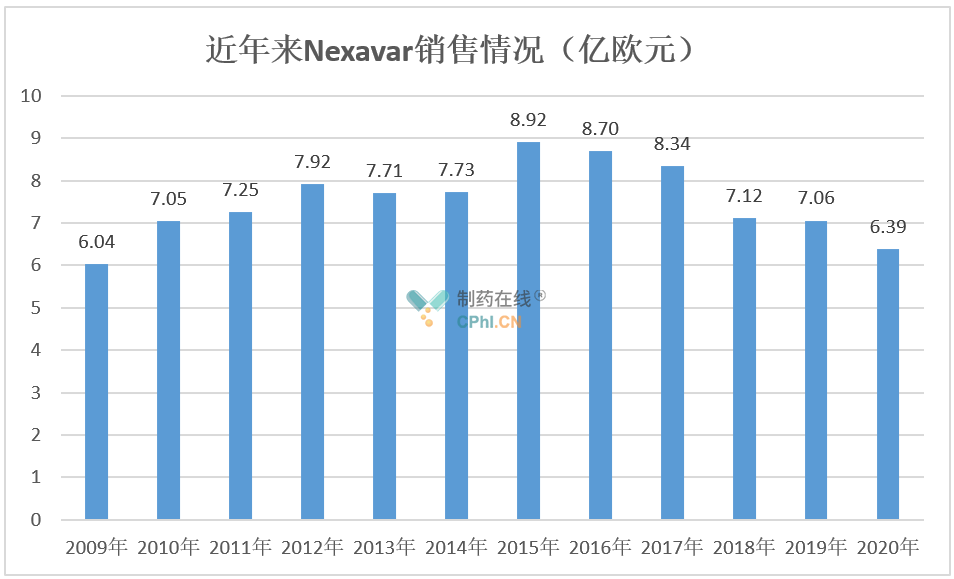
除了瑞戈非尼,拜耳还有一款口服多靶点激酶抑制剂--索拉非尼(sorafenib,Nexavar)。Nexavar于2005年12月被FDA批准用于治疗既往经α干扰素或白介素2(IL-2)治疗失败或被认为不适用这类疗法的晚期肾细胞癌(RCC)患者,随后于2007年11月被FDA批准用于不能手术治疗的肝细胞癌患者,2013年11月被FDA批准用于治疗局部晚期或转移性**碘(RAI)难治性分化型甲状腺癌。据拜耳财报,Nexavar销售额在2015年达到峰值(约8.92亿美元),近年来出现下滑,不过仍高于瑞戈非尼。
原研索拉非尼(商品名为多吉美)于2006年9月在国内获批被批准用于治疗晚期/转移性肾细胞癌,随后又被批准用于治疗肝细胞癌(2008/06)和甲状腺癌(2017/03)。索拉非尼于2017年进入国家医保,而且成功续约2020年国家医保。
据insight数据库,目前国内江西山香药业和重庆药友制药已先后于2020年8月5日和12日取得索拉非尼仿制药生产批件。此外,正大天晴、扬子江药业和辅仁药业正在进行BE试验,豪森药业、齐鲁制药等8家企业获批临床。而且,值得一提的是,两款国产索拉非尼在第四批全国药品集中采购中成功中选,这将进一步侵蚀原研索拉非尼的国内市场。
此外,我国泽璟制药自主研发的多靶点激酶抑制剂--多纳非尼(即氘代索拉非尼)已在国内报产(相关受理号为:CXHS2000010),适应症为治疗一线治疗晚期(无法手术或转移性)肝细胞癌。ZGDH3试验结果显示:与索拉非尼相比,在未接受过系统治疗的不可手术或转移性晚期肝细胞癌患者中,多纳非尼治疗组的中位总生存期(mOS)显著优于对照药物索拉非尼治疗组,达到统计学上差异显著性且具有临床意义的延长,而且多纳非尼组在3级及以上不良事件发生率、与药物相关的导致停药或减量的不良事件发生率等方面显示出更优的安全性。目前,该药凭借优异的疗效被纳入2020年版《CSCO原发性肝癌诊疗指南》,且作为I级专家推荐(1A类证据)。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57