葛兰素史克旗下两款重磅**/药物迎来新进展。
01GSK长效HIV药物专利授权给MPP
日前,葛兰素史克ViiV表示已将HIV暴露前预防(PrEP)长效疗法cabotegravir的专利授权许可给了MPP(日内瓦药品专利池组织),并开始与MPP商定相关的自愿许可条款。
ViiV表示,双方正在努力尽快实现自愿许可授权,以期在低收入和中等收入国家大规模使用cabotegravir疗法进行HIV暴露前预防。截至2021年12月,Viiv已通过一项类似的交易,将旗下另一款艾滋病药物dolutegravir的仿制药,提供给中低收入国家至少2000万艾滋病毒感染者使用。
早在2014年,MPP和ViiV就签署了dolutegravir合作协议,当时距离该疗法获得欧洲批准仅两个月时间,距离获得美国FDA批准仅8个月。ViiV和MPP当时就表示,从历史上看,新HIV疗法的仿制药版本在发达国家首次亮相后,平均需要7到9年后才能提供给发展中国家使用。
ViiV和MPP新闻稿中明确表示,自愿许可标志着双方艾滋病疗法合作准入计划中的重要一步,但其中“重大复杂性和相关担忧因素”仍然存在。ViiV指出,一方面,像cabotegravir这样的长效注射剂比口服抗逆转录病毒 药物更难制造。此外,合作还可能存在资本投资的需求,比如与逆转录病毒 药物相比,长效注射疗法的市场需求症会“不断变化且不太明确”。
为了确保其许可合作最终顺利成功,ViiV表示将与资助者、采购机构、社区团体和仿制药制造商合作,找到可行和可持续的解决方案,以尽快实现仿制药制造。在cabotegravir仿制药上市之前,ViiV承诺以非营利价格为低收入、最不发达国家和所有撒哈拉以南非洲国家等的公共项目提供长效注射剂。
在美国市场,该疗法目前正在以Apretude品牌名称进行销售,于去年12月获得了美国FDA批准,成为了第一款无需每日服药就能预防HIV感染的疗法。该疗法是一种整合酶抑制剂,能够抑制HIV病毒的基因序列整合到人体免疫细胞的基因组中。
两个月前,葛兰素史克控股的HIV医药公司ViiV Healthcare宣布,美国FDA已批准Cabenuva(cabotegravir/rilpivirine,卡博特韦/利匹韦林),用于治疗年龄在12岁及以上、体重在35公斤及以上、无治疗失败史、对cabotegravir或rilpivirine均无已知或疑似耐药、已实现病毒学抑制(HIV-1 RNA<50拷贝/毫升)的HIV-1青少年感染者。(详情请点击《美国FDA批准GSK长效HIV药物Cabenuva,用于青少年感染者》)
与此同时,辉瑞(Pfizer)和默克(Merck)去年也与MPP达成了合作协议,以促进全球以可负担的价格获得COVID-19抗病毒 药物。
02GSK HPV**希瑞适两剂次接种程序在华获批
近日,葛兰素史克(GSK)宣布,根据国家药品监督管理局(NMPA)的审评结果,其HPV**希瑞适(双价人乳头瘤病毒吸附**[HPV16/18型])适用于9-14岁女孩的两剂次接种程序已获得批准。由此,希瑞适成为中国获批9-14岁女孩两剂次接种程序的首 个进口HPV**。
高危型人乳头瘤病毒(HR-HPV)在女性生殖道持续性感染是导致宫颈癌的主要原因。在中国女性生殖系统恶性肿瘤中,宫颈癌的发病率和死亡率居于第一位。我国2020年宫颈癌新发病例约11万,死亡病例约5.9万,且其发病率和死亡率呈上升、年轻化趋势。流行病学研究显示,HPV16和HPV18型是宫颈癌中最常见的高危型HPV型别,在中国,约84.5%的宫颈鳞癌病例都与这两个高危型HPV感染有关。
在适龄女性人群中接种HPV**将会显著降低宫颈癌和癌前病变的发病率,从而降低疾病负担。由于HPV主要通过性接触传播,9-14岁未发生性行为的女孩是HPV**的首要接种人群。为实现在本世纪末全面消除宫颈癌,世界卫生组织(WHO)《加速消除宫颈癌全球战略》确定了2030年阶段性目标,包括2030年90%的女孩在15岁前完成HPV**全程接种。
2017年WHO《HPV**立场文件》明确推荐9-14岁女性接种两剂次HPV**。希瑞适此次获批的两剂次接种程序是指,年龄在9-14岁的女孩可选择在第0、6月分别接种1剂次**完成免疫程序。
研究表明,与15-25岁(在该年龄范围内已验证了希瑞适对宫颈各级别病变的**保护效力)女性的三剂次接种程序(第0、1、6月各接种一剂)相比,9-14岁女孩接种两剂次(第0、6月各接种一剂)所诱导的HPV16和18型抗体水平与接种三剂次的15-25岁人群相似。研究显示,9-14岁女性按照第0、6月免疫程序接种2剂次希瑞适,免疫应答可持续至少60个月6;据数学模型预测,95%的受试者接种后产生的高于自然感染的HPV16/18抗体可以持续至21年以上。
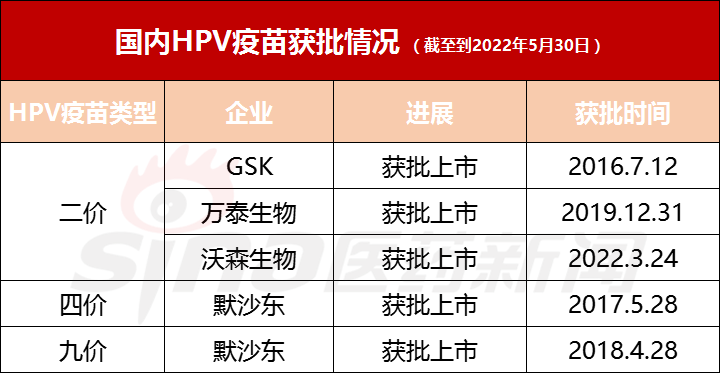
目前,我国批准上市的HPV**共5种,分别为万泰生物的二价**、沃森生物二价**、英国葛兰素史克(GSK)的二价**,以及美国默沙东的四价**和九价**。总体上看,HPV**依然处于供不应求状态,我国适龄女性HPV**接种率较低。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57