看点
• 2023年4月CDE新增一致性评价受理号93个(52个品种、55家企业)
• 2023年4月有147个受理号(含视同通过)涉及88个品种过评
根据药智数据企业版——仿制药一致性评价分析系统显示,2023年4月份新增一致性评价受理号93个,通过/视同通过一致性评价受理号共147个(视同通过受理号十8个)。(文末附2023年4月申报与过评一致性评价详情表)
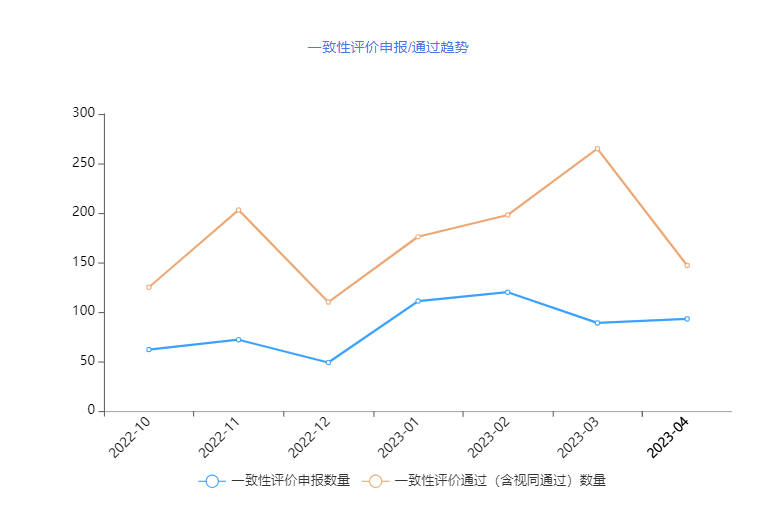
图1 2022年十月-2023年04月申报/通过趋势
4月过评详情
2023年4月,有39个一致性评价受理号和十8个仿制药上市申请受理号视同通过一致性评价,涉及十8家企业的88个品种。其中由于部分新批准药品还没能收集到详细信息等原因,导致一致性评价数据库中的数据和注册数据可能会存在差异,现在将整理出的2023年4月首家过评的6个药品信息放在文末附表1中,供大家参考。
• 过评企业
2023年4月各企业通过品种数的差距较小,石家庄四药有3个品种通过/视同通过一致性,苏州东瑞制药有限公司有2个品种过评,分别占据榜一和榜二位置;上海安必生制药技术有限公司分别与江苏安必生制药有限公司和青岛百洋制药有限公司联合申报的雷贝拉唑钠肠溶片和艾司奥美拉唑镁肠溶干混悬剂也在本月过评。详情见下图。
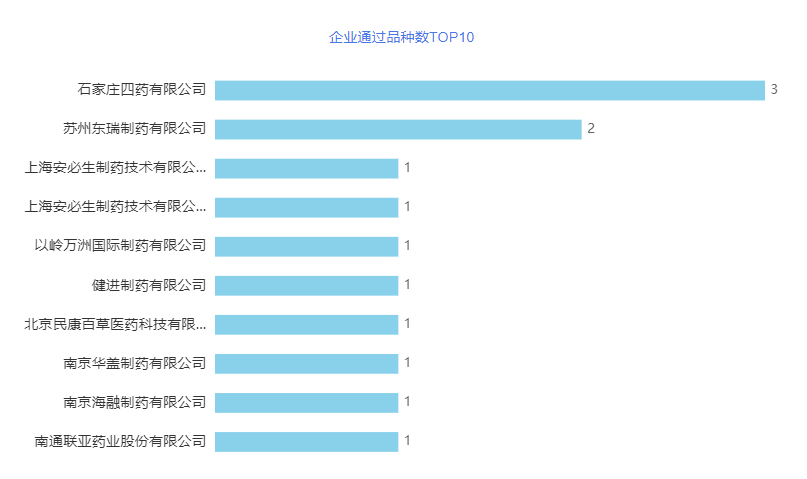
图2 2023年04月企业通过品种数TOP十
石家庄四药有限公司是以化学制剂、原料药、中药制剂和医用包材为主,产业链较为齐全的综合制药集团。2019年5月,氟康唑片通过一致性评价补充申请打响了公司仿制药一致性评价的第一枪,虽然首 个品种通过一致性评价的时间较其他企业晚,但从2020年开始,通过一致性评价的品种数量在不断攀升,到2023年4月,已有45个品种通过/视同通过一致性评价,其中2023年共有11个品种过评,仅4月就有3个品种过评,分别为:复方电解质注射液(Ⅱ)、碳酸氢钠注射液和腹膜透析液(乳酸盐-G2.5%)。
东瑞制药主要从事头孢类抗生素以及系统专科药物的开发、制造及销售。头孢类抗生素产品包括中间体、原料药和粉针剂;系统专科药物覆盖抗过敏、心血管系统、消化系统、泌尿系统和内分泌系统,剂型有片剂、胶囊剂、颗粒剂。苏州东瑞制药有限公司目前已有17个品种通过/视同通过一致性评价,2023年4月通过的两个品种分别为:利伐沙班片和氨氯地平阿托伐他汀钙片。
• 过评品种
泊沙 康唑注射液、艾司奥美拉唑镁肠溶干混悬剂和阿加曲班注射液并列榜单第一,各有3个企业过评。详情见下图。
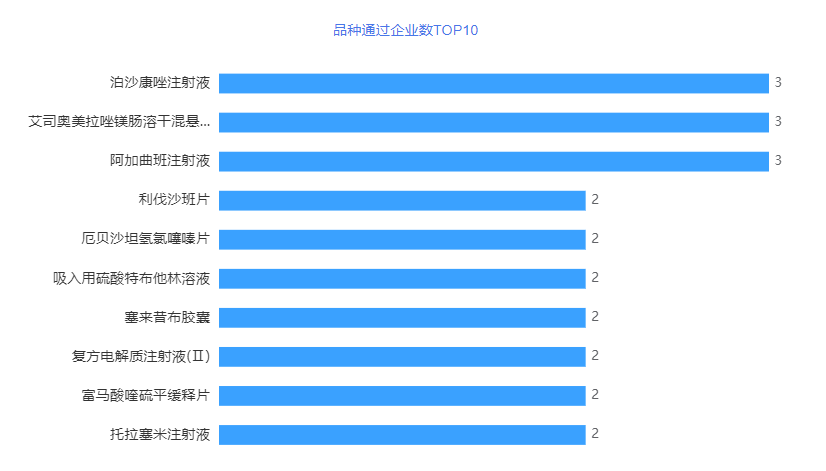
图3 2023年3月品种通过品种数TOP十
泊沙 康唑,是一种抗真菌感染的药物,通过抑制真菌细胞膜上的羊毛甾醇14-脱甲基酶而产生抗真菌作用,为乙类医保药品。泊沙 康唑注射液4月过评一致性企业分别为:先声药业有限公司、武汉启瑞药业有限公司和海南倍特药业有限公司,均为仿制药视同通过一致性评价。目前,泊沙 康唑注射液共有16家企业申报仿制药上市申请(暂无一致性评价补充申请),其中有4家企业过评,3家企业批准临床,3家企业未被批准,还有6家企业尚在审评审批过程中。
艾司奥美拉唑镁肠溶干混悬剂,于2007年首次在瑞典批准上市(商品名:Nexium?),规格为十mg,随后在美国、欧洲各国及日本上市,主要适应症为(1)胃食管反流病(GERD):反流性食管炎的治疗,已经治愈的食管炎患者预防复发的长期治疗,GERD的症状控制;(2)与适当的抗菌疗法联合用药根除幽门螺杆菌,并且:愈合与幽门螺杆菌相关的十二指肠溃疡,预防与幽门螺杆菌相关的消化性溃疡复发;(3)需要持续非甾体抗炎药(NSAID)治疗的患者:与使用NSAID治疗相关的胃溃疡治疗。目前国内上市药品中,共有5家企业的十批文,均为2023年过评的仿制药,其中2023年4月有上海安必生制药技术有限公司、成都苑东生物制药股份有限公司和江苏奥赛康药业有限公司三家企业过评。
阿加曲班注射液,适应症为用于对慢性动脉闭塞症(血栓闭塞性脉管炎、闭塞性动脉硬化症)患者的四肢溃疡、静息痛及冷感等的改善。目前,已有15家企业通过/视同通过一致性评价,在2023年4月通过的三家企业分别为:湖南恒生制药股份有限公司、山东华铂凯盛生物科技有限公司和吉林省东盟制药有限公司;目前还有12家企业已经递交仿制药上市申请或一致性评价补充申请。
52个品种申报,注 射剂超80%
2023年4月份,CDE新增一致性评价受理号93个,涉及55家企业的52个品种,其中注 射剂申报比例再创新高,超过申报的80%。
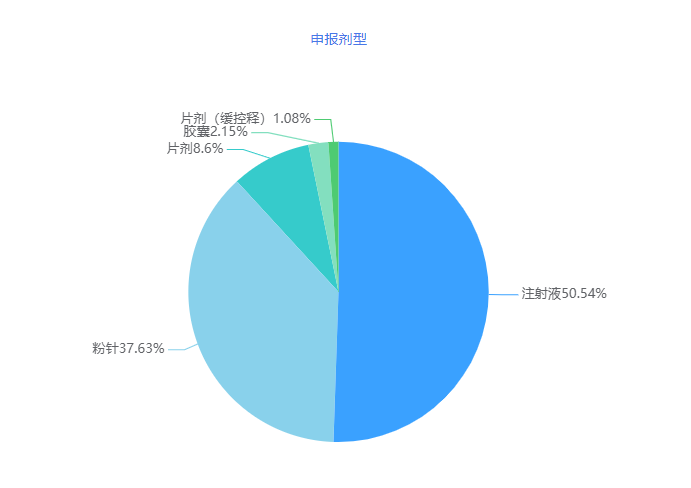
图4 2023年4月申报剂型详情
• 申报品种
2023年4月,注射用头孢唑肟钠一致性评价补充申请企业数量再次位居榜首,有4个企业,注射用头孢呋辛钠和硫酸阿米卡星注射液各有3家企业申报,并列第二。详情见下图。
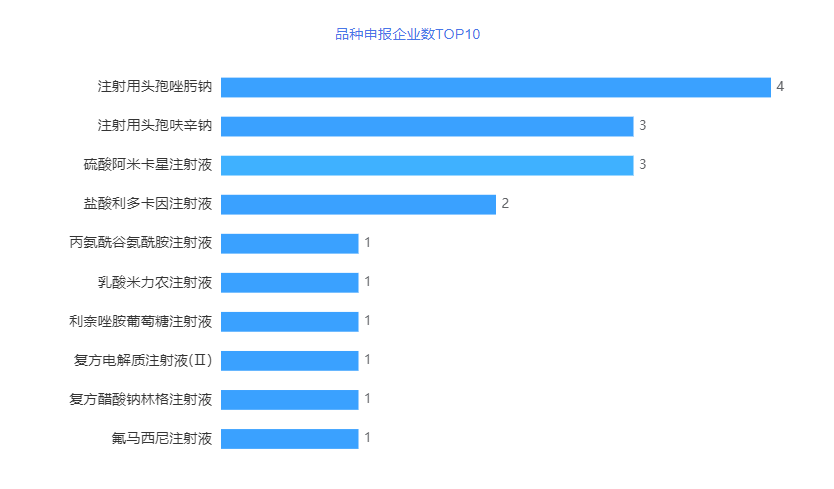
图5 2023年4月品种申报企业数TOP十
注射用头孢唑肟钠,适属于头孢类抗生素,适应症为敏感菌所致的下呼吸道感染、尿路感染、腹腔感染、盆腔感染、败血症、皮肤软组织感染、骨和关节感染、肺炎链球菌或流感嗜血杆菌所致脑膜炎和单纯性淋病。注射用头孢唑肟钠4月有山东润泽制药有限公司、山东罗欣药业集团股份有限公司、广州白云山医药集团股份有限公司白云山制药总厂和海南灵康制药有限公司4家企业共9个受理号申报。目前该药品共有8家企业提交一致性补充申请,还有3家企业提交仿制药上市申请,尚无过评企业。
注射用头孢呋辛钠,适用于未确定的细菌感染,或敏感细菌引起的感染。此外还可用于预防各种手术后的感染。注射用头孢呋辛钠4月有3家企业提交一致性补充申请,分别为广州白云山医药集团股份有限公司白云山制药总厂、苏州东瑞制药有限公司和国药集团国瑞药业有限公司;该药品目前已有17家企业过评一致性,还有17家企业在审评过程中。
硫酸阿米卡星注射液,适应症为本品适用于铜绿假单胞菌及部分其他假单胞菌、大肠埃希菌、变形杆菌属、克雷伯菌属、肠杆菌属、沙雷菌属、不动杆菌属等敏感革兰阴性杆菌与葡萄球菌属(甲氧西林敏感株)所致严重感染,如菌血症或败血症、细菌性心内膜炎、下呼吸道感染、骨关节感染、胆道感染、腹腔感染、复杂性尿路感染、皮肤软组织感染等。硫酸阿米卡星注射液4月一致性补充申请受理企业分别为:中孚药业股份有限公司、四川美大康华康药业有限公司、山东方明药业集团股份有限公司。硫酸阿米卡星注射液目前有且仅有成都倍特药业股份有限公司通过一致性评价,目前还有8家企业在审评审批过程中。
• 申报企业
2023年月企业申报品种数差异极小,广州白云山医药集团股份有限公司白云山制药总厂、杭州民生药业股份有限公司和江苏恩华药业股份有限公司各有2个品种申报并列第一。详情见下图。
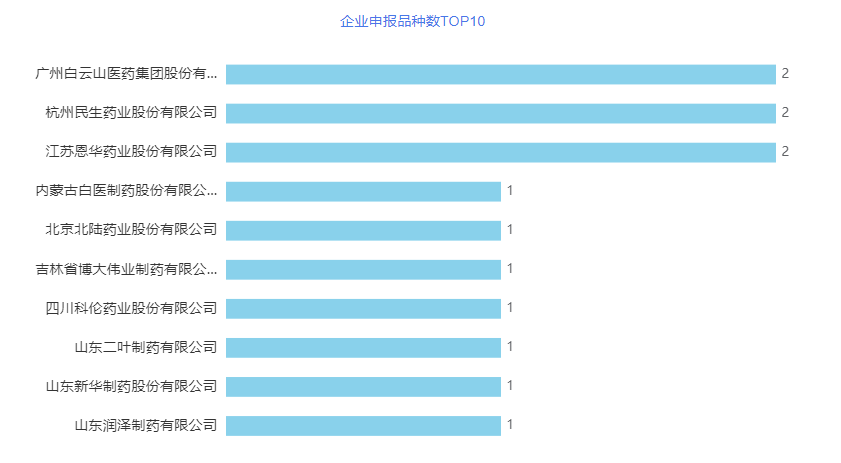
图6 2023年4月企业申报品种数TOP十
广州白云山医药集团股份有限公司白云山制药总厂是广药集团旗下最大的制药工业企业和国内实力较强的单体制药工业企业,也是国内著名的抗生素、抗ED药生产企业,集科研、生产、销售于一体;目前拥有11个剂型超过300个品规的产品,抗生素产品群声势浩大,几乎涵盖了所有抗菌消炎常用品种;抗ED药物产品群异军突起,白云山金戈成为国内首 个上市的国产“伟哥”。2022年,白云山盐酸达泊西汀片上市,与金戈组成男科用药双子星。目前公司已有16个品种通过/视同通过一致性评价,2个首家过评品种,还有6个品种尚在申报过程中。
杭州民生药业股份有限公司创建于1926年,是中国最早的四大西药厂之一。公司目前有13个品种通过/视同通过一致性评价,其中两个品种为首家过评企业,还有15个品种处于审评审批过程中。
江苏恩华药业股份有限公司战略定位于中枢神经药物领域市场,主要从事中枢神经系统药物的开发、生产和销售,是一家专注于中枢神经药物细分市场的企业,主要类别包括麻 醉类、精 神类和神经类。公司目前已有20个品种通过/视同通过一致性评价,其中8个品种为首家过评企业,目前还有9个品种处于审评审批过程中。
附表1:2023年4月首家通过一致性评价详情表
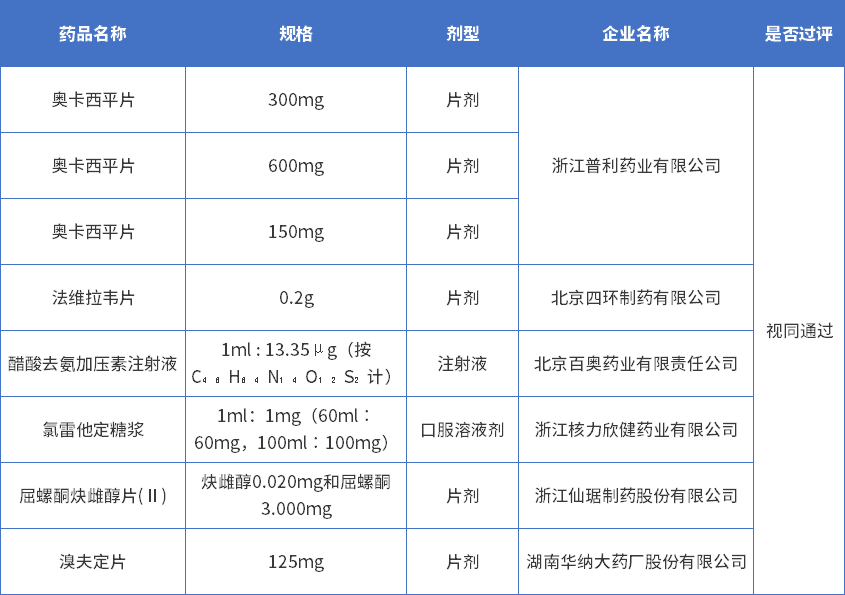
附表2:2023年4月通过(含视同通过)一致性评价详情表
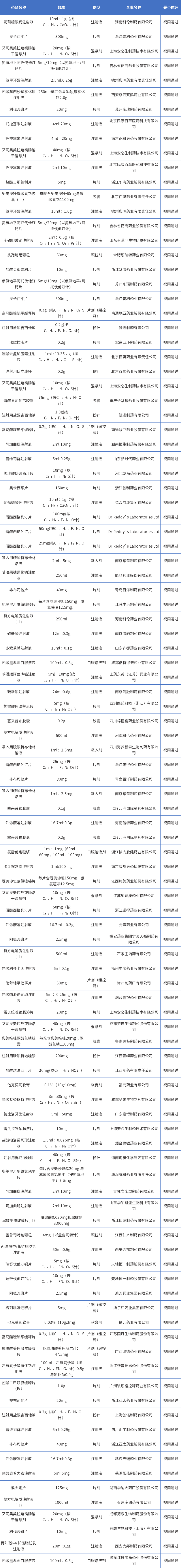
附表3:2023年4月申报一致性评价详情表
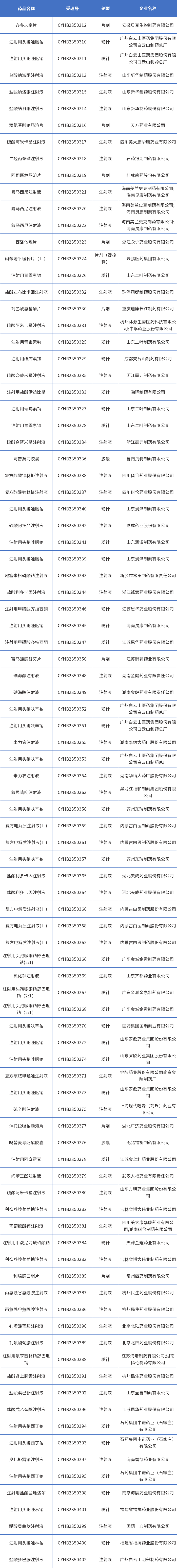
数据截至2023年4月30日
数据来源:药智数据企业版——仿制药一致性评价分析系统



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57