近日,威尚生物宣布其具有高穿透血脑屏障能力的靶向ATM的创新药物WSD0628获美国食品和药物管理局(FDA)R01基金拨款支持正在进行中的I/IIA临床开发。FDA ODD R01资金是用于支持具有潜力的和创新性的临床研究为评估孤儿药的安全性和/或有效性,用于治疗未满足临床需求的罕见疾病,对罕见病的药物开发具有广泛而积极的影响。
今年2月8日,威尚生物宣布美国FDA已授予其穿透血脑屏障的靶向ATM创新药物WSD0628用于治疗恶性神经胶质瘤的孤儿药资格。
威尚生物是一家全球性药物研发公司,主要专注于未满足临床需求的脑部肿瘤靶向药物研发。公开资料显示,该公司的运作模式以基因学为基础,寻找生物靶点、验证靶点、设计化合物,并与全球合作伙伴开展合作。
WSD0628是威尚生物研发的一款高活性、高选择性、高穿过血脑屏障能力的放疗增敏剂创新药物。据悉,该药物在临床前研究中展现了良好的PK和安全窗口,且在多种颅内PDX模型中包括但不限于脑胶质瘤、儿童脑干肿瘤、癌症脑转移等,联合放疗显著延长了总生存期。
ATM与肿瘤
ATM(Ataxia Telangiectasia Mutated)基因是共济失调毛细血管扩张症的致病基因,ATM蛋白为ATM基因编码的产物。一旦ATM基因发生突变,ATM蛋白不能正常表达,将会导致DNA损伤修复机制失调。最新研究表明,ATM蛋白表达以及活性的改变跟肿瘤的发生关系密切,提示ATM可能成为肿瘤治疗过程中一个新的潜在作用靶点。
大约45%的套细胞淋巴细胞瘤和T细胞前淋巴细胞白血病病例含有ATM突变。在结肠直肠癌、胃癌和肺腺癌中,10%-20%的病例有ATM突变。在胰 腺导管腺癌、乳腺癌、头颈部鳞状细胞癌和胆囊癌中,ATM突变的频率低于10%。
更多的临床前/临床试验研究表明:在化疗抗性方面,肿瘤细胞可以上调P38、HMGA水平以促进ATM基因表达;在放疗抗性方面,由于肿瘤细胞中ATM的高表达,导致辐射抗性的肿瘤细胞对化疗存在抵抗;在存活方面,ATM还可通过活化AKT以促进肿瘤细胞存活。另由于ATM的研究定位更倾向于合成致死,故与其他药物进行联合使用的临床应用也相对较多。
全球在研靶向ATM抑制剂进展
现阶段,ATM靶点药物尚无获批上市品种,除威尚生物的WSD0628外,当前进入临床阶段的ATM抑制剂还有4个,分别为阿斯利康公司的AZD-1390、MerckKGaA公司的M-4076、XRadTherapeutics公司的XRD-0394和石药集团的SYH2051。整体处于临床I期阶段,适应症主要为实体瘤,覆盖胶质母细胞瘤、转移性脑癌、头颈部鳞状细胞癌。
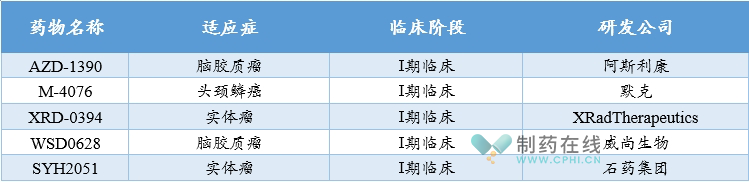
全球在研ATM抑制剂整理
AZD-1390
AZD-1390开发公司为阿斯利康,口服给药,为ATM激酶抑制剂,用于治疗肿瘤,包括胶质母细胞瘤和转移性脑癌。2017年6月,一项开放标签、单中心、探索性I期研究分析了AZD-1390(使用静脉注射[11C]AZD-1390微剂量)在健康男性(n=8)中的脑暴露情况,中位Tmax为20分钟。2018年4月,在英国和美国启动了一项针对复发性/原发性胶质母细胞瘤和脑转移患者的I期试验,以评估安全性、耐受性和药代动力学。2020年9月,启动一项研究以评估AZD1390和奥拉帕利联合用药的安全性试验。
M-4076
M-4076开发公司为Merck KGaA,口服给药,为ATP竞争性、高选择性的小分子ATM抑制剂,可增强DNA双链断裂诱导剂(如放射疗法)的作用,用于癌症治疗,包括头颈部鳞状细胞癌在内的晚期实体瘤。2021年5月,在美国和加拿大启动一项人体首次、开放标签、顺序分配、两部分的I期试验,以确定M-4076单一疗法在晚期实体瘤参与者(预期n=30)中的安全性、耐受性、药代动力学(PK)、药效学(PD)、最大耐受剂量(MTD)和早期药效特点。另早期临床前试验表明,在p53突变的HBCx-9模型中,M-4076(30mg/kg,qd)与PARP抑制剂联合用药,显示出显着的协同抗肿瘤活性。
XRD-0394
XRD-0394开发公司为X Rad Therapeutics,口服给药,为ATM/DNA-PK双重抑制剂,用于治疗转移性、局部晚期或复发性实体瘤。2021年8月,在美国启动了一项人体首次、多中心、开放标签、非随机的Ia期研究,以评估单次给药的安全性和耐受性;另试验还将评估单剂量XRD-0394与姑息性放疗联合治疗的PK曲线和PD疗效。
SYH2051
SYH2051开发公司为石药集团,是一种选择性的ATM抑制剂。公开资料显示,SYH2051通过靶向抑制ATM蛋白激酶及其下游信号蛋白CHK2和KAP1的磷酸化,延迟DNA双链断裂修复,导致持续的DNA双链断裂和ATM介导的细胞週期阻滞,从而抑制肿瘤细胞增殖。临床前研究显示,该产品对ATM靶点选择性好,体内外活性较好,极具临床开发价值。今年6月,SYH2051已获得中国国家药品监督管理局(NMPA)批准,可以在中国开展临床试验,适应症为实体瘤。
结语
ATM,作为合成致死背景下的重要靶点,已有多个品种进入临床,且均处于早期临床。无论是靶点的研究潜力,还是未来可能的市场竞争,都是药企在当下全球创新背景下的优选靶点。
ATM抑制剂作不仅可以作为单一疗法,其在联合疗法上也颇具潜力--不仅可以联合DNA损伤化疗和放疗,还包括其他DNA修复抑制剂和免疫检查点抑制剂。然而,将ATM抑制剂纳入癌症治疗标准还有很长的路要走,期待将来会有更多的ATM抑制剂进入临床并成功上市造福人类。
参考来源
1. Trends in Immunology, April 2021, Vol. 42, No. 4 .doi.org/10.1016/j.it.2021.02.001
2. Mutat Res Fund Mol Mech Mutagen 821(2020).doi.org/10.1016/j.mrfmmm.2020.111695
3. Pharmacology & Therapeutics(2019).doi.org/10.1016/j.pharmthera.2019.07.002



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57