葆元医药和信达生物共同宣布双方合作开发的新一代ROS1/NTRK抑制剂己二酸他雷替尼胶囊(“Taletrectinib”,“他雷替尼”及“泰莱替尼”)的第二项新药上市申请(NDA)已获国家药品审评中心(CDE)受理。适应症为用于未经ROS1 TKI治疗的局部晚期或转移性ROS1阳性非小细胞肺癌(NSCLC)成人患者的一线治疗,他雷替尼首 个适应症为用于经ROS1-TKI治疗失败的ROS1阳性局部晚期或转移性非小细胞肺癌成人,已于2023年11月获CDE受理NDA。

BD交易
根据药渡数据检索可知,他雷替尼最早由第一三共制药开发, 2018年12月第一三共将产品开发、生产和商业化权益授予葆元生物,2021年6月,信达生物与葆元生物达成协议,共同在大中华区(包括中国大陆、香港、澳门及台湾)开发和商业化。
临床疗效
两项NDA均基于临床II期研究TRUST-I(NCT04395677)的积极结果,2023年欧洲肺癌大会(ELCC)发布了TRUST-I试验的最新数据。
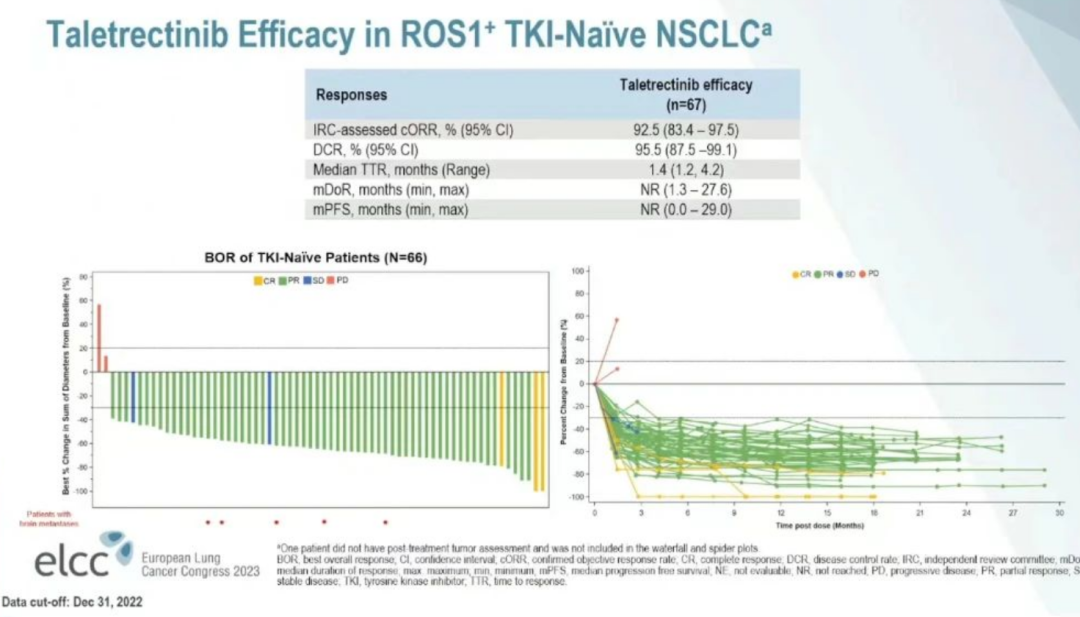
在TKI初治的可评估患者(n=67)中,IRC评估经确认ORR为92.5%(95%CI: 83.4%-97.5%),中位TTR为1.4个月(范围:1.2-4.2);DCR为95.5%(95%CI: 87.5%-99.1%);中位DOR尚未达到(NR:1.3-27.6),中位PFS为NR(0.0-29.0)。
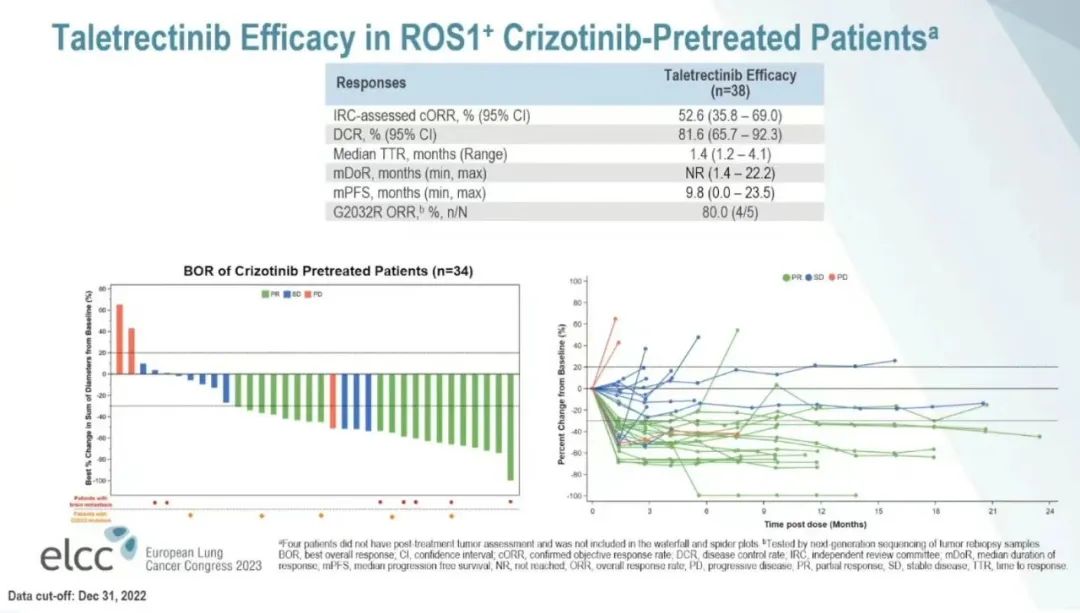
在接受过克唑替尼治疗的可评估患者(n=38)中,IRC评估cORR为52.6%(95%CI: 35.8%-69.0%),中位TTR为1.4个月(1.2-4.1);DCR为81.6%(95%CI: 65.7%-92.3%);中位DOR为NR(1.4-22.2);中位PFS为9.8个月(0.0-23.5个月)。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57