近日,Stemline Therapeutics(美纳里尼全资子公司)/SciClone Pharmaceuticals(赛生药业)递交的「Elacestrant片」临床试验申请获CDE受理。
近日,Stemline Therapeutics(美纳里尼全资子公司)/SciClone Pharmaceuticals(赛生药业)递交的「Elacestrant片」临床试验申请获CDE受理。
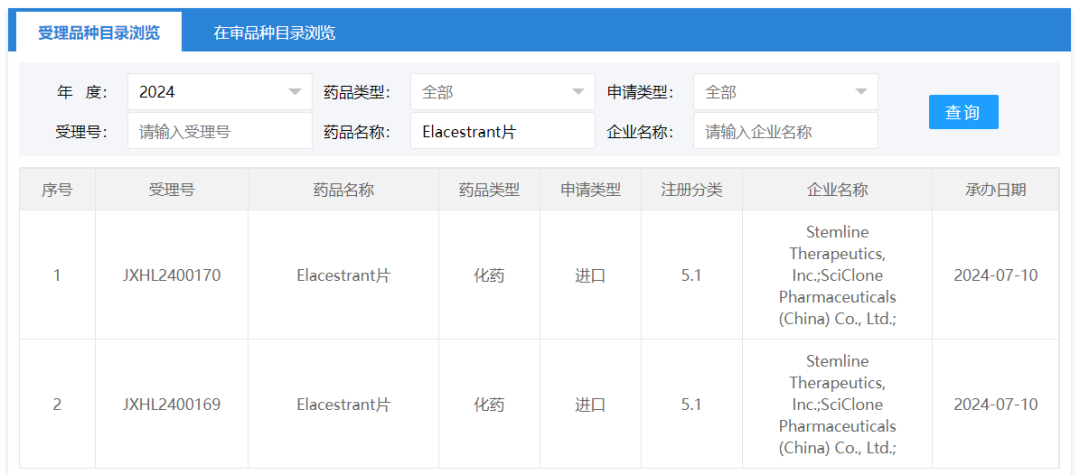
Elacestrant(艾拉司群)是一款口服选择性雌激素受体降解剂(SERD),2023年1月被FDA批准用于绝经后女性和成年男性晚期或转移性乳腺癌,这些既往至少接受过一线内分泌治疗后疾病进展,并伴有雌激素受体1基因(ESR1)突变的雌激素受体(ER)阳性、人类表皮生长因子受体2(HER2)阴性,商品名为Orserdu。
2023年2月,乳腺癌NCCN指南更新至Version 2.2023作出相应推荐:新增“FDA批准的口服SERD药物Elacestrant作为其他推荐方案的2A类证据治疗HR+、HER2-、ESR1突变晚期乳腺癌”。
作为FDA批准的首个口服SERD,业界非常看好Orserdu,预计其2023年销售额将至少达到1.75亿美元。
Elacestrant由Radius Health研发,2020年美纳里尼获得其全球许可。2023年11月,赛生药业与美纳里尼签订独家许可及合作协议,获得Elacestrant在中国境内开发和商业化授权。
乳腺癌是全球女性发病率最高的癌症。据GLOBOCAN 2022发布的数据,2022年全球乳腺癌年新发病例数达231万,死亡病例数达67万。激素受体阳性/人表皮生长因子受体阴性(HR+/HER2-)乳腺癌是最常见的亚型,约占所有乳腺癌的70%。
内分泌治疗是HR+乳腺癌重要的治疗方式,临床常用药物包括选择性雌激素受体调节剂(SERM,如他莫昔芬、托瑞米芬)、选择性雌激素受体降解剂(SERD,如氟维司群)和芳香化酶抑制剂(AI,如来曲唑、阿那曲唑和依西美坦)等。其中SERM如他莫昔芬,其结构与雌激素相似,在靶器官内与雌激素竞争结合ER,阻断雌激素与ER的结合发挥作用。SERD通过与癌细胞表面的ER相结合,降低雌激素受体的稳定性,诱导它们被细胞正常的蛋白降解机制降解,从而降低ER水平,抑制癌细胞的生长。仅从作用机制上看,SERD优于SERM。AI通过抑制雌激素生成发挥抗肿瘤效应,但由于ESR1突变可导致ER不依赖于雌激素而异常活化,这导致AI耐药或者疗效不佳。
上述三类内分泌治疗药物中,SERD获批品种最少,仅两款,即氟维司群和艾拉司群,这两款药物获批时间间隔超20年。其中原研氟维司群(商品名:Faslodex)由阿斯利康(AZ)研发,最早于2002年4月被FDA批准单药用于抗雌激素药物(如他莫昔芬)治疗后病情仍趋恶化的绝经后ER+乳腺癌,随后又被批准单药一线治疗绝经期HR+、HER2-晚期乳腺癌。此外,Faslodex还被批准联合多种药物用于治疗乳腺癌,如联合ATK抑制剂Truqap(Capivasertib)用于治疗接受内分泌治疗期间或之后出现复发或进展,且存在一个或多个PIK3CA、AKT1或PTEN基因改变的成人HR+、HER2-乳腺癌;联合CDK4/6抑制剂Ibrance(哌柏西利)用于接受内分泌治疗后进展的HR+、HER2-转移性乳腺癌女性患者;联合CDK4/6抑制剂Verzenio(阿贝西利)用于治疗晚期或转移性HR+、HER2-乳腺癌女性患者。此外,Faslodex联合PI3K抑制剂Inavolisib(GDC-0077)和哌柏西利治疗HR+、HER2-,且携带PIK3CA突变的局部晚期或转移性乳腺癌成人患者的NDA正在接受FDA优先审查。
Faslodex曾是销售额超10亿美元的重磅品种,但随着专利到期,仿制药的获批上市,其销售额急剧下滑,已由2018年的10.28亿美元下降至2023年的2.97亿美元。
艾拉司群是全球批准的第二款SERD。已公布的III期临床研究EMERALD结果显示:在内分泌治疗耐药的ESR1突变患者中,艾拉司群组的中位无进展生存期(PFS)为3.8个月,而氟维司群或AI组为1.9个月,艾拉司群组12个月PFS率达26.8%,而氟维司群或AI组为8.2%。此外,艾拉司群在临床使用上有一个巨大优势,即口服给药,而氟维司群需通过肌肉注射给药。
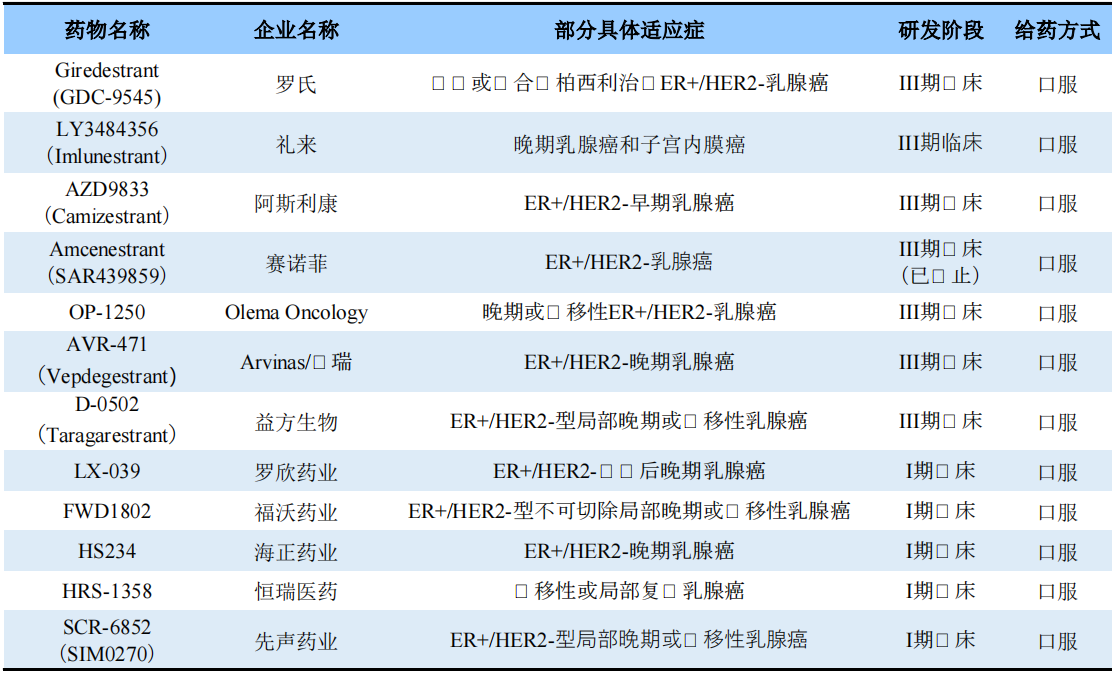
SERD是药企争相布局的热门领域,目前全球还有多款在研,详见下表。与氟维司群不同,在研SERD几乎全通过口服给药。药物类型上,除了小分子化药,在研在研SERD还涉及PROTAC降解剂,如ARV-471。
全球部分在研SERD
资料来源:公开资料、药渡数据
研发进度上,多款SERD进入III期临床。
罗氏的Giredestrant是一种高效、非甾体类口服SERD,临床前疗效优于氟维司群等药物,耐受性良好,在ESR1突变和既往接受过氟维司群治疗的晚期乳腺癌患者中单药治疗或与哌柏西利联合使用时显示出良好的抗肿瘤活性。
礼来的Imlunestrant是一款口服SERD,并具有单纯拮抗性。其专门设计用于在整个给药期间提供持续的雌激素受体靶点抑制,而不受ESR1突变状态的影响。I期临床试验中,Imlunestrant在接受过多种前线疗法的乳腺癌患者中获得早期积极疗效。目前,Imlunestrant正在进行EMBER-3、 EMBER-4两项大型全球III期临床,其中EMBER-3研究旨在比较Imlunestrant+研究者选择的内分泌疗法、Imlunestrant+阿贝西利相较Imlunestrant单药治疗ER+、HER2-局部晚期或转移性乳腺癌的PFS是否改善。EMBER-4研究旨在评估Imlunestrant辅助治疗对比标准辅助内分泌疗法,在既往接受2至5年辅助内分泌治疗的 ER+、HER2- 早期乳腺癌且具有较高复发风险的患者中的疗效和安全性。此外,礼来还在探索Imlunestrant联合阿贝西利和LOXO-783(PI3Kα H1047R抑制剂)的潜力。
阿斯利康的Camizestrant是新一代口服SERD和纯ERα拮抗剂,在一系列临床前模型(包括具有ER激活突变的模型)中显出抗癌活性。I期研究SERENA-1结果显示:Camizestrant单独给药或联合哌柏西利给药时,Camizestrant耐受性良好,且具有良好的抗肿瘤作用。SERENA-2研究探索性分析显示:Camizestrant在早期和持续抑制雌激素受体基因突变(ESR1m)ctDNA方面均优于氟维司群,并且早期ESR1m ctNDA水平减少≥50%与Camizestrant治疗的PFS延长相关。SERENA-3研究显示:75mg Camizestrant可实现最大程度的ER降解和Ki67抑制。此外,Camizestrant联合哌柏西利或阿贝西利一线治疗ESR1突变、ER+转移性乳腺癌、以及联合哌柏西利一线治疗ER+局部晚期或转移性乳腺癌的两项3期临床正在进行中。
赛诺菲的Amcenestrant是一种优化的口服SERD,但由于其单药治疗既往接受过激素治疗的ER+、HER2-局部晚期或转移性乳腺癌的2期临床试验AMEERA-3、以及其联合哌柏西利治疗晚期一线ER+、HER2-晚期乳腺癌的3期临床试验AMEERA-5的失败,赛诺菲2022年终止了Amcenestrant的全球开发。
Olema Oncology的OP-1250是一款兼具完全雌激素受体拮抗剂(CERAN)和SERD活性的口服小分子,能有效且完全地抑制ER(AF1和AF2转录激活域)的活性,阻断ER驱动的转录活性,抑制ER驱动的乳腺癌细胞生长,并诱导ER降解。已公布的OP-1250治疗晚期ER+、HER2-乳腺癌的首个I/II期临床试验结果显示:OP-1250表现出极好的药代动力学特性,支持每日给药1次,且具有良好的耐受性和明确的疗效信号。2022年7月,该药被FDA授予快速通道资格,用于治疗此前接受一种或多种内分泌疗法(至少一种疗法结合了CDK4/6抑制剂)后疾病进展的ER+、HER2-的转移性乳腺癌。
Arvinas与辉瑞共同开发的ARV-471是一款可诱导ER活性降解的强效、选择性、口服可生物利用的PROTAC蛋白降解剂。临床前研究显示:ARV-471可在肿瘤细胞内降解几乎所有的ER分子,并在许多ER驱动的动物肿瘤模型中,引起肿瘤大量的缩小。而且,与标准护理氟维司群相比,ARV-471无论是作为单一药物还是与CDK4/6抑制剂联合使用时,均显示出优越的抗肿瘤活性。
最新公布的ARV-471治疗局部晚期或转移性ER+、HER2-乳腺癌的II期临床试验VERITAC队列数据显示:所有患者的临床获益率(CBR)为38%,其中针对ESR1野生型患者的CBR为20%,针对ESR1突变型患者的CBR为51.2%。不过ARV-471针对所有患者的CBR与前两年公布的数据相比较低。
ARV-471联合哌柏西利治疗局部晚期或转移性ER+、HER2-乳腺癌的Ib期临床试验ARV-471-mBC-101数据显示:所有患者的CBR为63%,其中ESR1突变患者的CBR为72%,ESR1野生型患者的CBR为53%。当使用3期试验推荐剂量(RP3D)200 mg时,CBR为67%,其中ESR1突变患者的CBR为79%,ESR1野生型患者的CBR为43%。在31例可评估患者中,ORR为42%。在15名可评估的接受RP3D的患者中,ORR为53%,其中ESR1突变患者的ORR为60%,ESR1野生型患者的ORR为40%。患者的中位PFS为11.2个月。接受RP3D治疗的患者的mPFS为13.9个月,其中ESR1突变患者的mPFS为13.9个月,ESR1野生型患者的中位PFS为11.2个月。此外,在所有vepdegestrant剂量组中,无论ESR1突变状态如何,患者的循环肿瘤DNA(ctDNA)水平在经过一个治疗周期后显著降低(平均变化-98.9%);在RP3D剂量下,ESR1突变型患者的ctDNA在7个治疗周期中持续下降。
目前,ARV-471单药二线治疗ER+、HER2-乳腺癌,以及联合哌柏西利二线治疗ER+、HER2-转移性乳腺癌的两项3期临床试验正在进行中。
益方生物的D-0502是其自主研发的一款口服SERD,临床前研究和临床研究均显示其具有优良的抗肿瘤活性及安全性。已公布的Ib期临床试验结果显示:D-0502单药治疗ER+、HER2-女性乳腺癌安全性良好,并初步展现出可喜的抗肿瘤效果——CBR为47.1%,ORR为15.7%。在与氟维司群CONFIRM研究相似的受试者中,D-0502单药治疗的CBR为50.0%,ORR为12.5%,DCR为70.0%,中位PFS为7.4个月。目前,D-0502针对既往经治ER+、HER2-局部晚期或转移性乳腺癌的注册性III期临床试验正在进行中。此外,D-0502还被开发联合哌柏西利治疗局部晚期或转移性ER+、HER2-乳腺癌。
除了上述药物,还有多款在研SERD处于I期临床,这些药物大多由我国药企开发。其中海正药业的HS234是一种口服SERD,同时兼备拮抗和促进雌激素受体降解的作用。先声药业的SIM0270是新一代口服SERD,具有高活性、高血脑屏障通透性和良好的安全性。
鉴于乳腺癌患者群体的逐年攀升,SERD的市场规模也将同步增长。弗罗斯特沙利文分析,2030年全球SERD市场规模有望达到66亿美元,其中中国市场达到86亿元。然而,目前全球已获批的SERD药物屈指可数,原研氟维司群的市场规模随着专利到期,仿制药的获批上市急速骤减。艾拉司群有望凭借口服、临床效果优势,逐步侵蚀氟维司群市场。纵观在研SERD,多款进入III期临床,但整体试验数据并不十分亮眼,未来谁将率先出线还无法预测。不过在研SERD不断优化,除了小分子,还包括PROTCA降解剂,而且部分在研SERD还具有雌激素受体拮抗剂活性。期待在药企的不懈坚持下,SERD市场早日迎来新生力量。
参考资料:
1.《益方生物D-0502治疗ER阳性、HER2阴性乳腺癌Ib期研究结果亮相2023 SABCS》.益方生物.2023年12月08日
2.《2023 ESMO|邵志敏教授:未来可期,口服SERD药物Camizestrant将成为乳腺癌内分泌治疗新方法》.医学界肿瘤频道.2023年10月23日
3.《口服SERD桂冠难夺!赛诺菲、罗氏相继失败,益方生物加入竞争》.同写意.2022年04月28日
4.《AZ、礼来、益方……群雄逐鹿SERD口服药》.一度医药.2023年03月09日




![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57