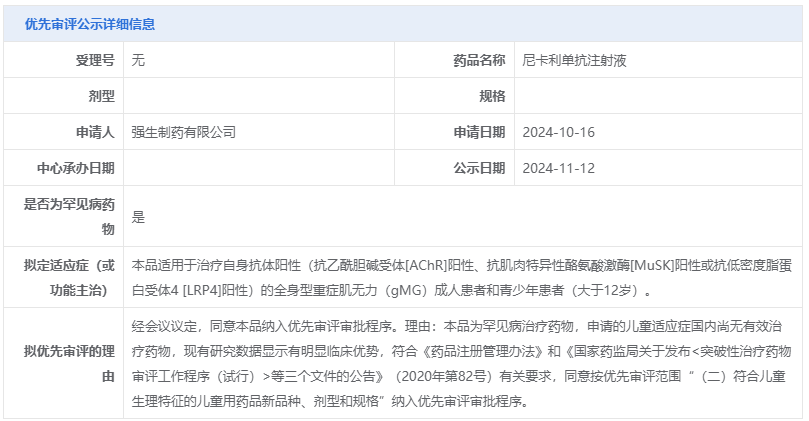
2024年11月12日,从CDE官网公示可知,强生申报的尼卡利单抗(Nipocalimab)注射液拟纳入优先审评,适应症为自身抗体阳性(抗乙酰胆碱受体[AChR]阳性、抗肌肉特异性酪氨酸激酶[MuSK]阳性或抗低密度脂蛋白受体4 [LRP4]阳性)的全身型重症肌无力(gMG)成人患者和青少年患者(大于12岁)。
尼卡利单抗原研公司为Momenta,是一款可与FcRn结合的IgG1抗体,可通过选择性阻断IgG与FcRn的相互作用,降低循环IgG。2020年8月,强生以约65亿美元收购Momenta,由此获得了尼卡利单抗。2024年8月30日,强生宣布已向FDA递交FcRn靶向抗体尼卡利单抗用于全身性重症肌无力(gMG)的BLA申请。
尼卡利单抗III期Vivacity-MG3研究取得了积极结果。该试验达成主要终点,接受尼卡利单抗联合标准治疗(SOC)的患者在改善gMG疾病指标日常生活活动(MG-ADL)评分方面优于安慰剂联合SOC。
这项双盲、安慰剂对照研究招募了广泛的抗AChR+、抗MuSK+和/或抗LRP4+患者,这些患者约占gMG患者群体的95%。与基线相较,在第22、23和24周,接受尼卡利单抗联合SOC治疗的患者在MG-ADL评分上平均改善了4.70分,显著高于安慰剂联合SOC治疗患者的3.25分(P=0.002)。试验中尼卡利单抗的安全性和耐受性与其他试验一致。不良事件、严重不良事件和导致停药的不良事件的总体发生率与安慰剂联合SOC组相似。
参考文献
1、CDE官网
2、药渡:首个!强生FcRn抗体重症肌无力三期临床成功,递交上市在即
3、强生制药官网



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57