今日(11月12日),根据国家药品监督管理局药品审评中心(CDE)官网公示,荣昌生物自主研发的全球首 款注射用重组B淋巴细胞刺激因子(BLyS)/增殖诱导配体(APRIL)双靶点的新型融合蛋白泰它西普(RC18,泰爱®),新适应症成人全身型重症肌无力(gMG)拟纳入优先审评。
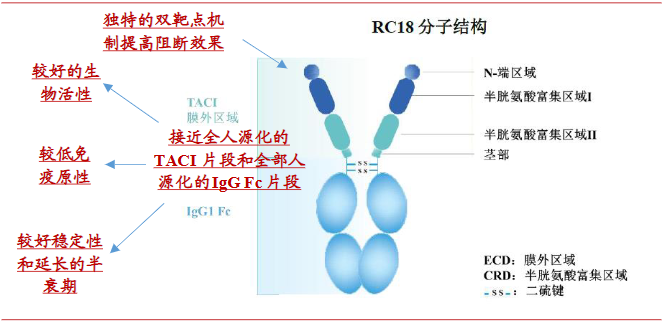
泰它西普是TACI-Fc融合蛋白,由TACI的胞外特定的可溶性部分与人血清中免疫球蛋白G1(IgG1)的可结晶片段(Fc)构成。TACI是一种跨膜蛋白受体,属于肿瘤坏死因子受体超家族成员,配体为APRIL和BlyS。采用接近全人源化的TACI片段和全部人源化的IgG Fc片段,有效降低了潜在的免疫原性,提高了安全性,并且具备更佳血清稳定性及较长半衰期。
泰它西普治疗成人全身型重症肌无力(gMG)的多中心、随机、开放的II期临床研究结果显示,在第24周,泰它西普240mg组QMG评分(重症肌无力评分Quantitative Myasthenia Gravis Score,重症肌无力临床研究中最常用的量表之一)平均降低9.6分,第12周QMG评分降低9.5分,这表明泰它西普可快速地改善临床症状。同样,240mg组的MG-CAS(MG临床绝 对评分,作为gMG严重程度的衡量指标,得分越高表示残疾程度越高)自基线至第4周下降且在整个研究中持续。在第24周,240mg组患者获得QMG临床意义应答(下降3分)的累积百分比为100%,获得QMG显著应答(下降5分)的累积百分比为86.7%。
参考文献
1、CDE官网
2、荣昌生物官网
3、东海证券研报:荣昌生物(688331):核心产品快速放量,新适应症加速推进



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57