近日,浙江华海药业股份有限公司(以下简称“华海药业”或“公司”)的控股子公司上海华奥泰生物药业股份有限公司(以下简称“华奥泰”)及华博生物医药技术(上海)有限公司(以下简称“华博生物”,系华奥泰的下属全资子公司)、浙江华海生物科技有限公司(以下简称“华海生物”)收到国家药品监督管理局(以下简称“国家药监局”)核准签发的 HB0028 注射液和 HB002.1T 注射液的《药物临床试验批准通知书》,现将相关情况公告如下:
一、药物基本情况
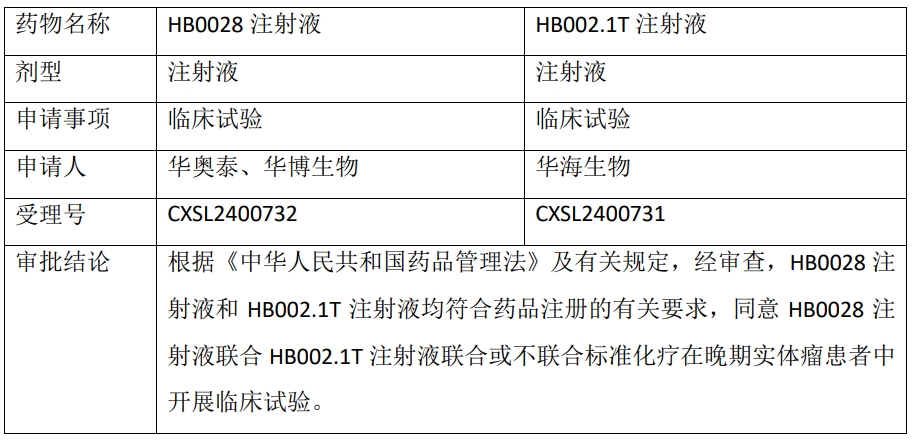
二、药物的其他相关情况
2024 年 10 月,公司下属子公司华奥泰、华博生物、华海生物向国家药监局提交了 HB0028 注射液和 HB002.1T 注射液联合用药的临床试验申请;近日,国家药监局同意 HB0028 注射液联合 HB002.1T 注射液联合或不联合标准化疗在晚期实体瘤患者中开展临床试验。
HB0028 注射液是靶向程序性死亡受体配体 1(PD-L1)和转化生长因子-β(TGF-β)的双特异性抗体。HB0028 的抗 PD-L1 部分可通过阻断 PD-L1 与其受体 PD-1 和 CD80(B7-1)的结合,解除 PD-L1/PD-1 信号通路介导的免疫抑制作用、活化细胞毒 T 淋巴细胞,抑制肿瘤生长;与此同时,HB0028 的抗TGF-β 部分可与 TGF-β 结合,解除 TGF-β 介导的对 T 细胞和自然杀伤细胞的免疫抑制、调节性 T 细胞活化、肿瘤血管生长和上皮细胞向间充质细胞转化等促进肿瘤生长和转移的因素。目前 HB0028 正在临床 I 期,针对多种实体瘤进行探索。
从市场情况来看,目前尚无 PD-L1/TGF-β双抗药物上市。国内进展最快的是江苏恒瑞医药股份有限公司的 SHR-1701,已向国家药监局提交上市申请。
截至目前,公司在 HB0028 注射液项目上已合计投入研发费用约人民币 5,313 万元。
HB002.1T 注射液是用于治疗晚期实体瘤的融合蛋白类新药,以血管内 皮生长因子(vascular endothelial growth factor receptor, VEGFR)为靶点,可阻断其生物学活性。
HB002.1T 为 VEGFR1 第二个膜外 Ig 样结构域保留若干侧翼序列直接和 IgG1 的 Fc 段融合蛋白,与同靶点上市药物贝伐珠单抗比较,HB002.1T 在分子设计、以及临床前药理药效有独特优势,临床Ⅰa 期数据表明其有很宽的安全性窗口、较长的半衰期、并初步表明抗肿瘤的积极疗效信号。
从市场情况来看,全球已有数款 VEGF 靶点的创新药产品上市,其中最知名的是罗氏制药的贝伐珠单抗,于 2004 年成为第一个临床使用的血管生成抑制剂。
截至目前,公司在 HB002.1T 注射液项目上已合计投入研发费用约人民币 11,916万元。
HB002.1T 与 HB0028 联合,一方面通过阻断 VEGF:VEGFR 信号阻碍肿瘤生长所必需的新生血管生长和营养供应、促进肿瘤细胞中 T 淋巴细胞的浸润来阻止或减缓癌症的发展;另一方面 PD-L1/TGF-β双特异性抗体可以阻断 PD-L1:PD-1、PD-L1:CD80、TGF-β RII:TGF-β1 的信号通路,解除肿瘤微环境的免疫抑制状态,促进肿瘤浸润免疫细胞的增殖,增强肿瘤浸润免疫细胞的杀伤活性。临床前结果表明,HB002.1T 联合 HB0028 对肿瘤的抑制效果优于等剂量的 HB002.1T 和 HB0028 单药。
目前全球尚无同时靶向 VEGF、PD-L1 及 TGF-β这三条信号通路的药物上市。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57