过去25年,自身免疫性疾病治疗领域经历了从广谱抗炎到靶向精准调控的深刻变革(图1)。以肿瘤坏死因子(TNF)抑制剂(如英夫利昔单抗和阿达木单抗)为代表的细胞因子信号调节药物,奠定了免疫治疗创新的基石,并成为多适应症的标准疗法。近年来,随着白细胞介素(IL)家族抑制剂、JAK/TYK2激酶抑制剂及新兴靶点的崛起,行业正加速向精准化与多样化迈进。全球自身免疫药物市场已稳居第二大治疗领域,2024年TOP100畅销药中自免药物占比15款,总销售额达829.5亿美元。本文将深入分析当前靶点格局、跨疾病影响及未来创新方向。
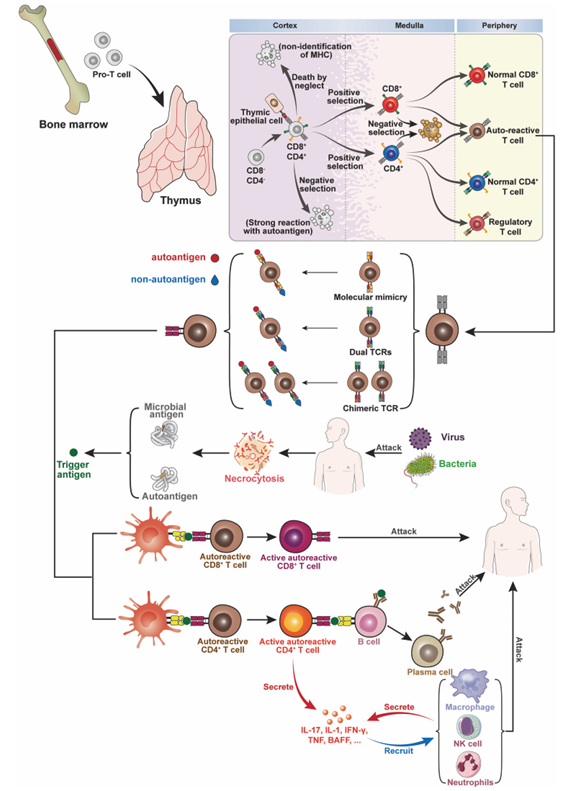
图1.自身免疫性疾病机制的模式图[2]
1、治疗靶点前景:从传统核心到新兴路径的扩展
自 2020 年以来,已推出 4 种针对自身免疫性疾病的 first-in-class 药物,其中 3 种针对皮肤病适应症中的上皮屏障功能障碍和炎症(IL-13、IL-31 和 IL-36 抑制剂)。第四种也在皮肤病学中,是一种酪氨酸激酶 2 (TYK2) 抑制剂,可调节 IL-12 和 IL-23 等细胞因子下游的信号传导。在分析的 92 个治疗靶点中,正在研究的自免药物数量从 2020 年的 131 种增加到 2024 年的 193 种(+47%)(图2)。
TNF超家族与IL家族的持续主导
尽管TNFα抑制剂仍是基石,但靶向TNF超家族其他成员(如OX40、TL1A、BLyS/BAFF)的疗法正快速推进。2020年仅CD40/CD40L轴处于III期,而2024年TL1A、RANK等靶点药物已进入关键试验阶段,其中TL1A抑制剂在克罗恩病和溃疡性结肠炎中展现出潜力。
IL家族则通过选择性增强(如IL-17A/F双靶点抑制剂)、长效化(如GSK的IL-5抑制剂depemokimab)及口服小分子(如礼来的IL-17口服药)实现迭代创新。IL-4、IL-33、IL-18等靶点的首 创新药(first-in-class)成为新焦点,而IRAK4因可同时抑制IL-1家族和Toll样受体信号,被视为多疾病干预的关键靶点(图2)。
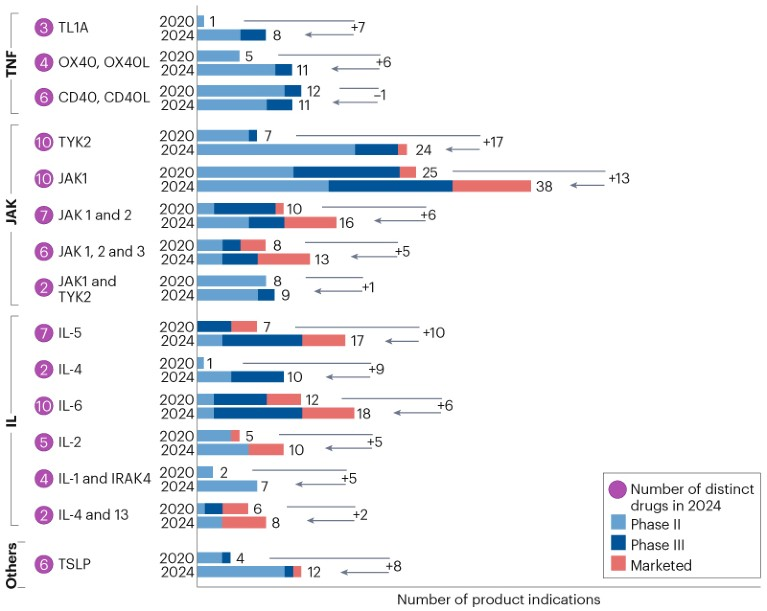
图2.自免在研管线及产品[1]
下游激酶与联合疗法的突破
JAK抑制剂虽在风湿病等领域广泛应用(图2),但其对造血系统的副作用促使行业转向更具选择性的TYK2抑制剂。例如,百时美施贵宝的TYK2抑制剂Sotyktu通过调节IL-12/23通路,在银屑病中展现出优于传统JAK抑制剂的耐受性。联合策略(如IL-17+TNF双靶向、JAK/TYK2双激酶抑制剂)进一步拓宽治疗窗口,尤其在银屑病和克罗恩病中取得进展。
2型炎症性疾病的关键靶点竞争
针对特应性皮炎、哮喘等2型炎症疾病,IL-4/IL-13抑制剂(如度普利尤单抗)通过阻断IL-4Rα亚基,成为多适应症的重磅药物(图2)。TSLP抑制剂(如tezepelumab)则通过靶向上游警报素,在严重哮喘和COPD中取得突破。此外,IL-31(瘙痒通路)和IL-36(脓疱型银屑病)等新靶点的崛起,标志着皮肤病治疗的进一步细分。
2、跨疾病影响:从局部到系统的治疗革新
皮肤病学的领先突破
自2020年以来,皮肤病领域(图3)迎来多款创新药物:
IL-13抑制剂:Tralokinumab和Lebrikizumab用于中重度特应性皮炎,显著改善表皮屏障功能。 IL-17A/F双靶点抑制剂:Bimekizumab在斑块状银屑病中实现更高缓解率(PASI90达80%以上),挑战TNF抑制剂地位。
IL-36抑制剂:Spesolimab成为泛发性脓疱型银屑病的首个特异性疗法。
JAK/TEC抑制剂:辉瑞的Litfulo作为首个获批的脱发治疗药物,凸显激酶抑制剂的多适应症潜力。
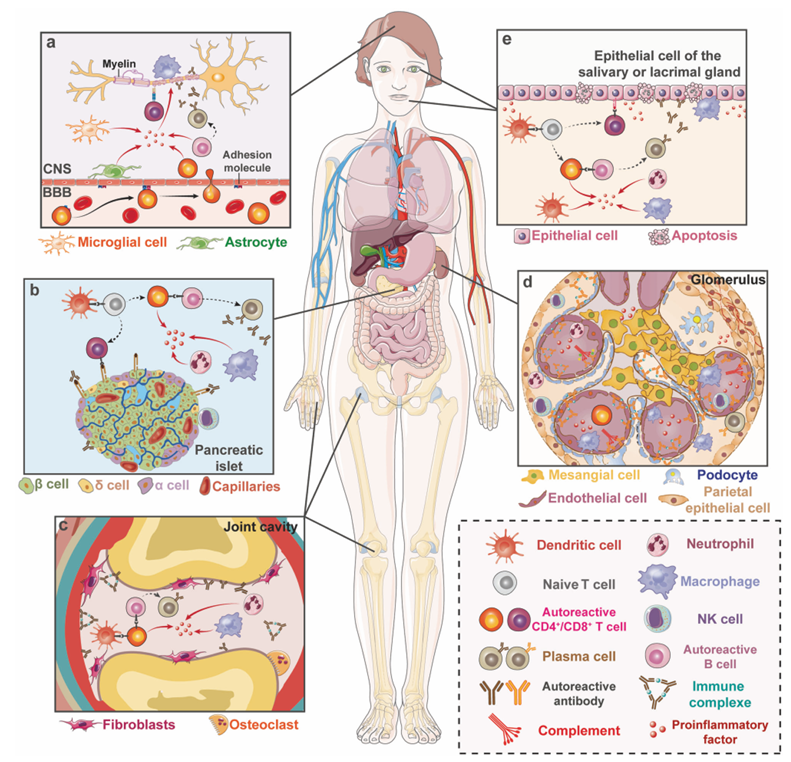
图3.一些典型自身免疫性疾病的模式图[2]
风湿病与胃肠道疾病的扩展
JAK抑制剂在类风湿性关节炎和强直性脊柱炎中持续扩展,选择性JAK1抑制剂(如乌帕替尼)因更低副作用备受青睐。胃肠道领域,IL-23抑制剂(如古塞奇尤单抗)在克罗恩病中对比传统疗法显示优效性,III期试验中内镜缓解率提升76%。嗜酸性食管炎则通过IL-4/13靶向药物(如度普利尤单抗)实现症状显著改善。
呼吸系统与系统性疾病的新机遇
首个TSLP抑制剂tezepelumab在严重哮喘中降低急性发作率,而IL-33靶向药物(如itepekimab)为COPD提供新治疗类别。系统性红斑狼疮(SLE)和干燥综合征(图3)则通过CD40/CD40L轴(如dazodalibep)和BAFF抑制剂探索突破。
3、未来展望:精准医疗与多维创新
新兴靶点与首 创新药的竞争
TL1A与OX40/OX40L轴:默克的tulisokibart和罗氏的RVT-3101以及赛诺菲/Teva 的 duvakitug等TL1A抑制剂在炎症性肠病中进入III期,有望为克罗恩病和溃疡性结肠炎患者带来新的治疗方案;安进的 rocatinlimab 和赛诺菲的 amlitelimab 是靶向 OX40/OX40L T 细胞活化轴的新型药物,有望解决 IL-4 和 IL-13 产生的关键上游调节因子。
IL-33:阿斯利康的tozorakimab(IL-33/ST2双靶点)和赛诺菲的itepekimab是两种针对 IL-33 的竞争性候选药物,预示COPD等呼吸疾病治疗的进一步分化。
此外,CD40/CD40L轴可能引入全身性疾病的治疗替代方案,包括治疗干燥综合征的达唑达利贝 (Amgen) 和治疗系统性红斑狼疮的达匹利珠单抗 (Biogen/UCB)(图2)。
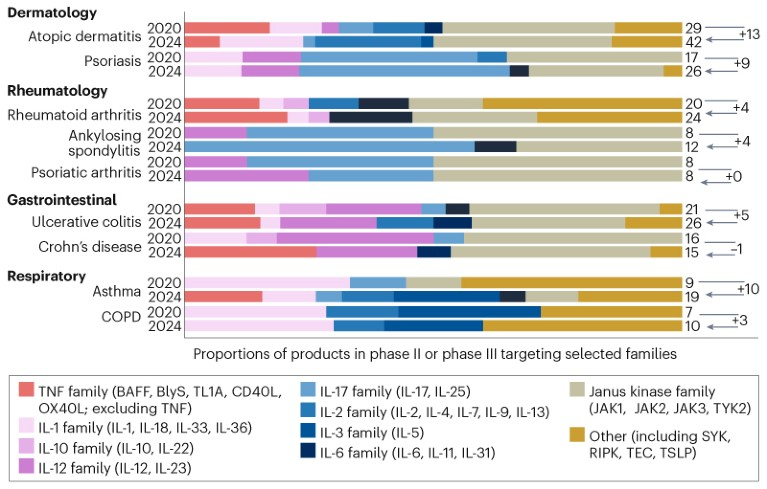
图2.按治疗领域划分的选定自身免疫性疾病的管道靶点前景(II 期和 III 期)的演变[1]
从剂型优化到生物标志物
中国自免市场快速增长,2030年预计达231亿美元,但生物药占比仍低于全球(2021年32.9% vs. 全球69.8%)。医保覆盖与仿制药冲击(如芦可替尼首仿上市)将加速市场洗牌,而国产IL-17抑制剂(恒瑞、智翔金泰)有望打破外资垄断。
口服小分子(如礼来的IL-17口服药)与长效注射制剂(如每月一次的IL-5抑制剂)提升患者依从性。生物标志物驱动的分层治疗(如IL-23抑制剂的黏膜愈合指标)正成为临床研究核心,助力精准患者筛选。
联合疗法与多适应症拓展
IL-17+TNF双靶向策略在银屑病关节炎中探索协同效应,而JAK/TYK2双激酶抑制剂可能平衡疗效与安全性。多适应症布局(如度普利尤单抗覆盖皮炎、哮喘、嗜酸性食管炎)成为药企提升产品生命周期的重要策略。
结语
自身免疫治疗正迈向以机制驱动、患者为中心的新时代。未来十年,随着疾病特异性靶点的解析,以及基因编辑、多组学技术的应用,个体化治疗方案将逐步实现。中国凭借庞大的患者基数与创新药企崛起,或重塑全球市场格局。
参考资料:
[1]Fauconnier, Alexandre et al. “Trends in the drug target landscape for autoimmune diseases.” Nature reviews. Drug discovery, 10.1038/d41573-025-00061-7. 3 Apr. 2025,
[2] Song, Yi et al. “Evolving understanding of autoimmune mechanisms and new therapeutic strategies of autoimmune disorders.” Signal transduction and targeted therapy vol. 9,1 263. 4 Oct. 2024,
[3] Fugger, Lars et al. “Challenges, Progress, and Prospects of Developing Therapies to Treat Autoimmune Diseases.” Cell vol. 181,1 (2020): 63-80.



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57