3月21日,第一三共HER2ADC新药Trastuzumab Deruxtecan(DS-8201,商品名:Enhertu)的上市申请获得NMPA受理。

(资料来源:CDE)
2020年12月,DS-8201被CDE纳入突破性治疗品种,单药用于既往接受过一种或一种以上治疗方案的HER2阳性局部晚期或转移性胃或食管胃结合部(GEJ)腺癌成人患者的治疗。因此,笔者推测此次申报上市的就是此适应症。
药物临床试验登记与信息公示平台显示,DS-8201在中国开展了4项Ⅲ期临床试验。
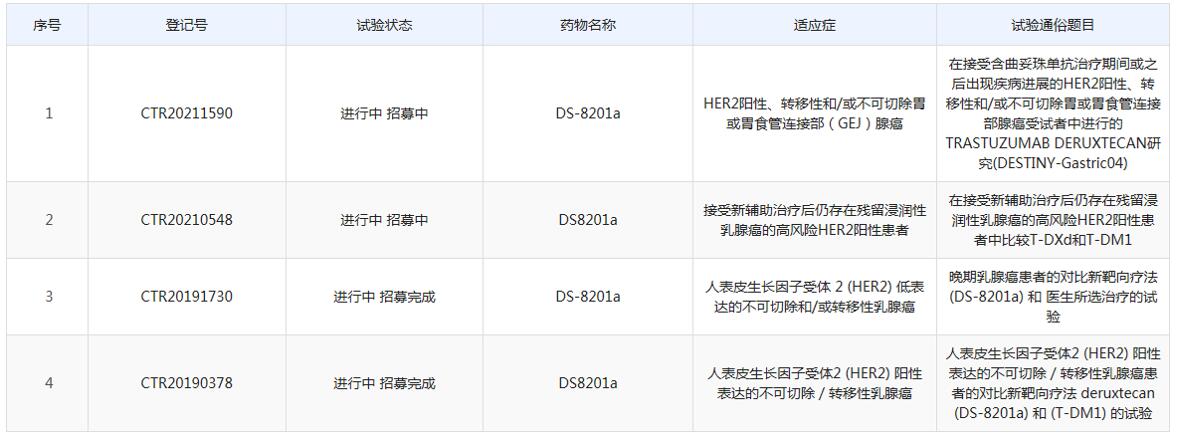
(资料来源:药物临床试验登记与信息公示平台)
DS-8201是由第一三共和阿斯利康合作开发推广的一种新型靶向HER2的ADC药物,由人源化抗HER2lgG1抗体、可裂解的四肽连接子和拓扑异构酶-I抑制剂(喜树碱类衍生物DXd)组成。DS-8201从可裂解linker、高DAR、强bystander效应等角度构建了更高效的ADC技术平台。
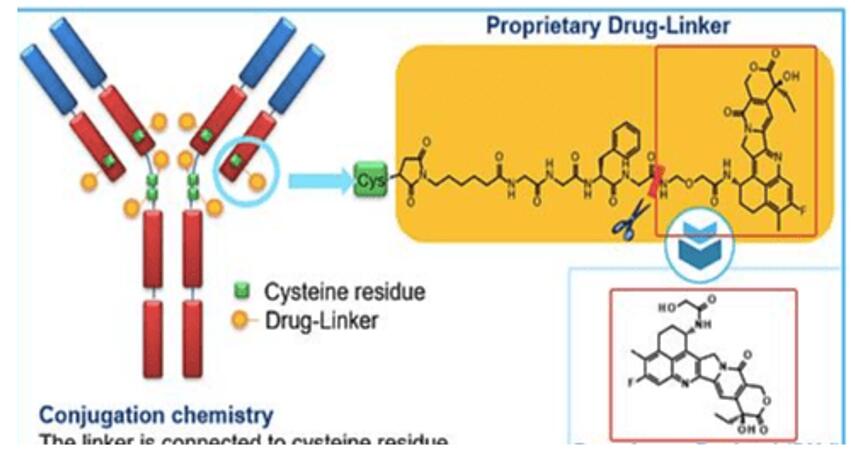
(图片来源于公开资料)
两个适应症获批上市
目前,DS-8201共有两个适应症获批上市。
2019年12月,DS-8201获FDA加速批准,用于治疗无法切除或转移性HER2阳性乳腺癌患者,这些患者转移后都接受过两种或两种以上抗HER2治疗为基础的治疗方案;
2021年1月,DS-8201获FDA批准,用于治疗局部晚期或转移性的HER2阳性胃或胃食管腺癌患者,患者既往接受过一种曲妥珠单抗为基础的治疗方案;
此外,其他适应症也在获批路上。
2020年5月,DS-8201获FDA授予突破性疗法认定,用于治疗在铂类化疗期间或之后疾病进展的HER2突变型转移性非小细胞肺癌患者;
2022年1月,DS-8201被FDA授予优先审评资格,用于治疗既往接受过抗HER2方案的不可切除或转移性HER2阳性乳腺癌成人患者。
除了乳腺癌、胃癌和肺癌之外,DS-8201在结直肠癌和子宫癌肉瘤中的研究数据也非常好。
据WHO统计,2020年全球5大癌种分别是乳腺癌、肺癌、结直肠癌、前列腺癌和胃癌,未来适应症顺利获批的话,DS-8201可以说囊括了4大癌种。
中国有3款ADC药物上市
截至目前,全球共有十多款ADC药物获批,3款在中国获批上市。
全球已获批ADC药物信息
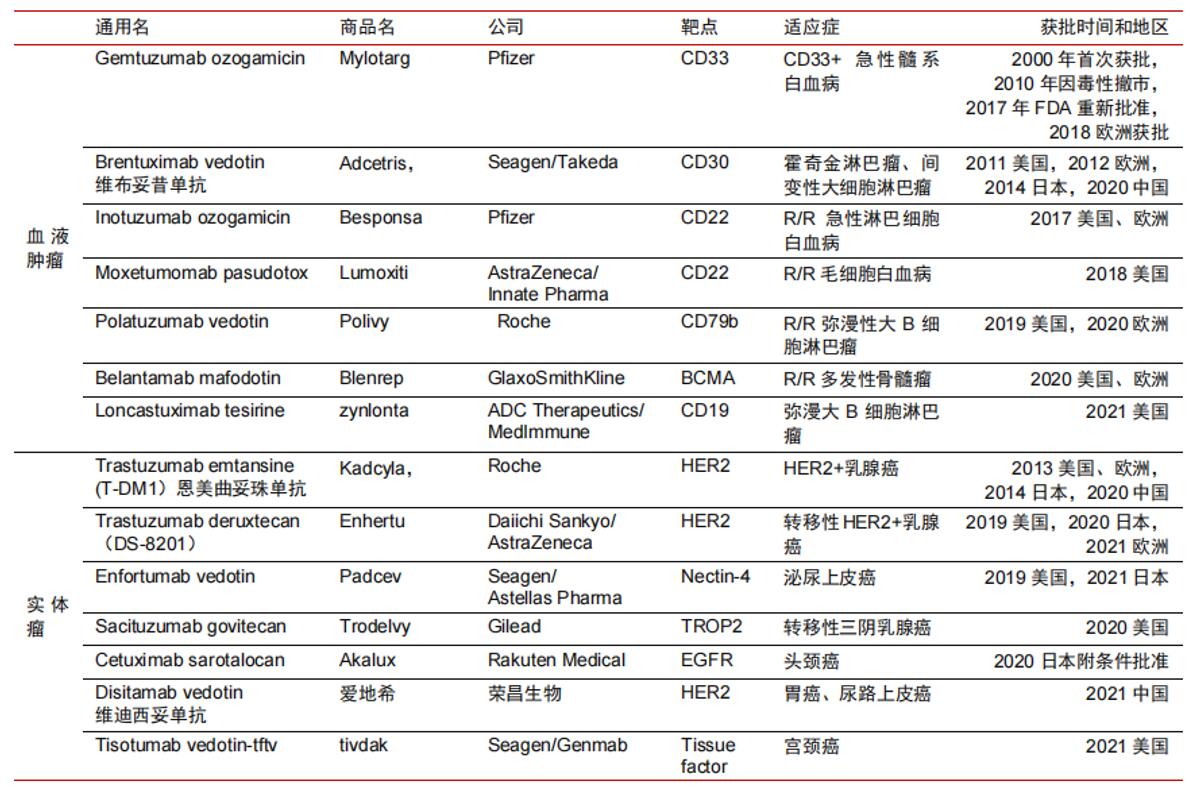
(来源于公开资料)
除此之外,国内还有2款ADC药物已经递交上市申请,也就是说有3款ADC药物处于申请上市阶段。
处于临床III期研究阶段的ADC药物共14款。其中,国产ADC仅有两款,分别来自东曜药业和百奥泰(已终止),其他企业通过licensein引进海外ADC。
国内ADC药物研发进展
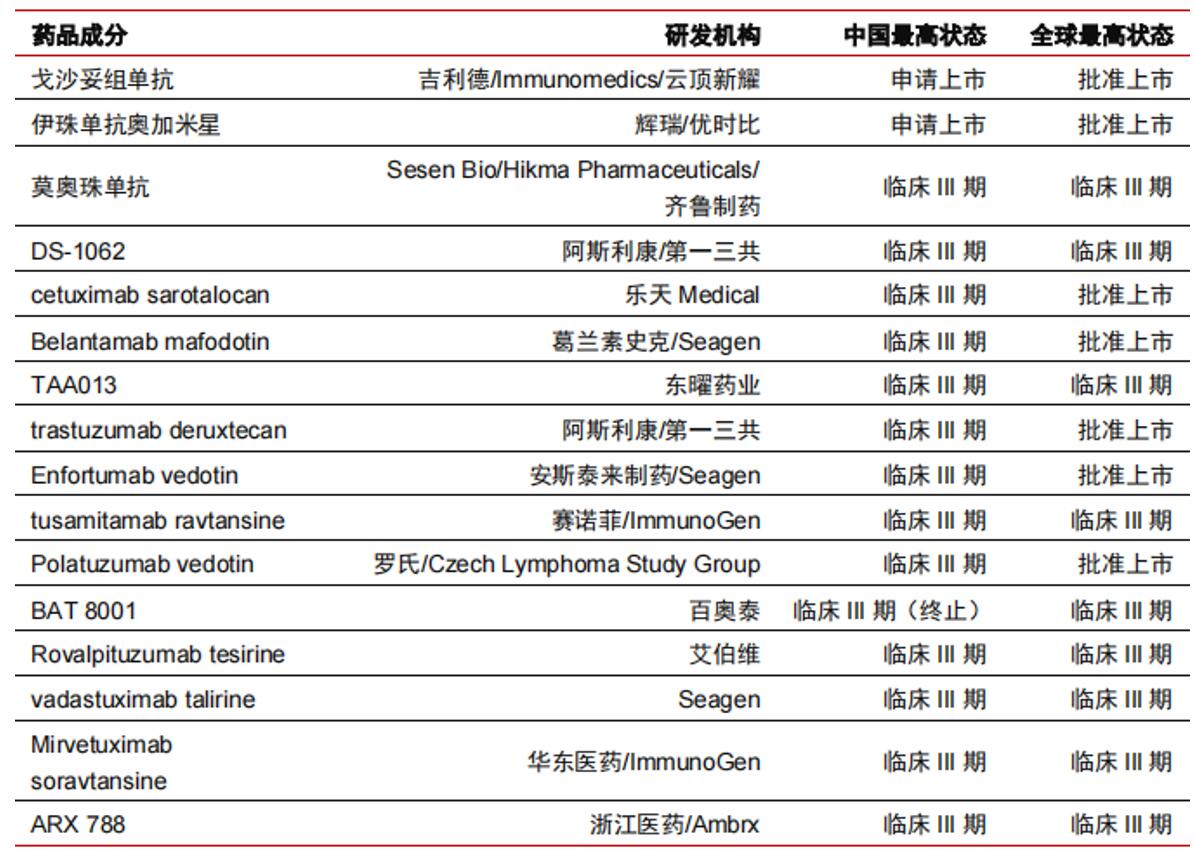
(来源于公开资料)
参考资料:源头创新,领跑国内ADC和融合蛋白赛道



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57