
罕见病首次出现在1867年的一篇论文上,该文报道了一个无法确诊也无治疗手段的罕见骨病。后来,人们把这类发病率极低的疾病统称为罕见病,而用于诊断、治疗和预防罕见病的药品被称为孤儿药。根据世界卫生组织(WHO)的定义,患病人数占总人口0.65‰~1‰的疾病即可被定义为罕见病。罕见病特点有:50%的罕见病患者是儿童,其中30%的儿童患者活不过5岁。94%以上的罕见病没有药物。目前FDA批准的治疗药物不超过500种。80%以上的罕见病都是由基因突变引起的。对罕见病患者来说就是救命药,罕见病研发,就是与时间赛跑。
溶酶体广泛存在于动物和原生动物细胞中,有40多种不同的水解酶,在摄入的外来物质的消化、细胞自身衰老细胞器的清除以及细胞的自溶过程中起着重要的作用。溶酶体贮积症(lysosomal storage disorders, LSDs)是一种遗传性代谢病,是由于溶酶体内的酶(主要是酸性水解酶)、激活蛋白、转运蛋白或溶酶体蛋白加工校正酶的缺乏,引起溶酶体功能缺陷,代谢物不能被有效地消化,因而在组织细胞中贮积所导致的疾病。溶酶体贮积症主要类型有:1)粘多糖贮积症(MPS),是由于溶酶体内参与糖胺聚糖分解代谢酶类的缺陷,造成糖胺聚糖降解不完全所引起的溶酶体贮积病。包括MPS I, II, III, IV, VI。2)糖原贮积症,由于溶酶体内糖原分解的酶缺陷所致,如Pompe病。3)神经鞘脂分解代谢缺陷:因溶酶体内神经鞘脂分解代谢相关酶的缺乏所致,如我们非常熟悉的戈谢病(Gaucher disease),法布里病(Fabry disease)。还有其他一些类型,比如胆固醇分解障碍、转运和运输障碍、多种溶酶体酶缺陷等。
酶替代疗法(Enzyme replacement therapy, ERT)是溶酶体贮积症患者的常用疗法,当体内缺失特定的酶时,通过静脉注射,向患者体内注射含有缺失酶的药剂,替代缺失的酶。它的优点是可针对不同类型的酶,具有高特异性。原本只能从生物体中提取酶,现在用重组技术可实现批量生产,酶与生物体具有高度同源性,安全性通常比较好,毒理试验结果比较干净。酶替代疗法最大的挑战是价格昂贵,需要像糖尿病人注射胰岛素一样,长期用药。通常需要特定的递送载体将活性酶递送到靶器官中,而具有活性的酶,在稳定性方面也具有一定的挑战。
国外已批准的酶替代疗法的药物,列表如下。我们重点对Myozyme, Elaprase, Vpriv三款已上市药物的药效、药代、毒理进行介绍,以便更好的理解酶替代疗法类药物非临床开发策略。
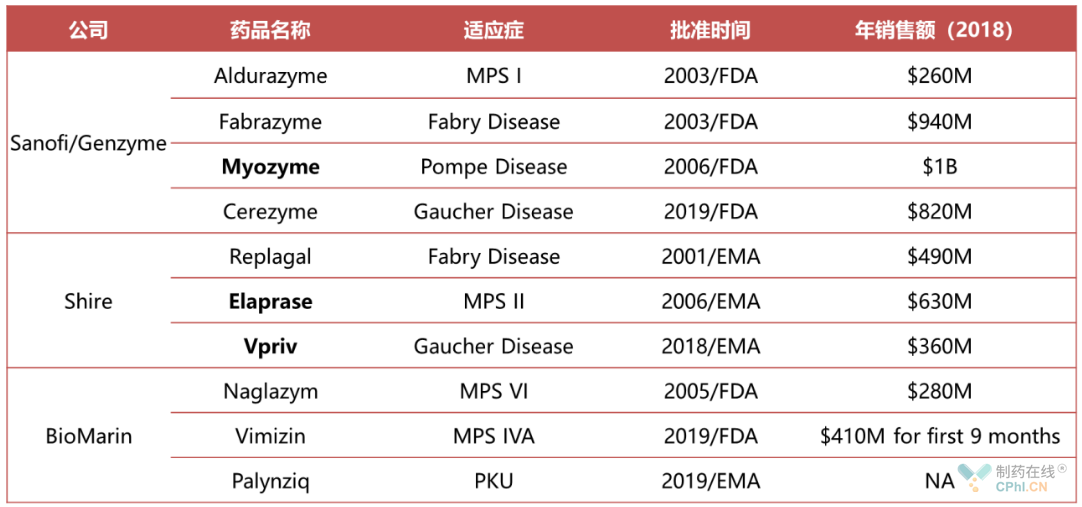
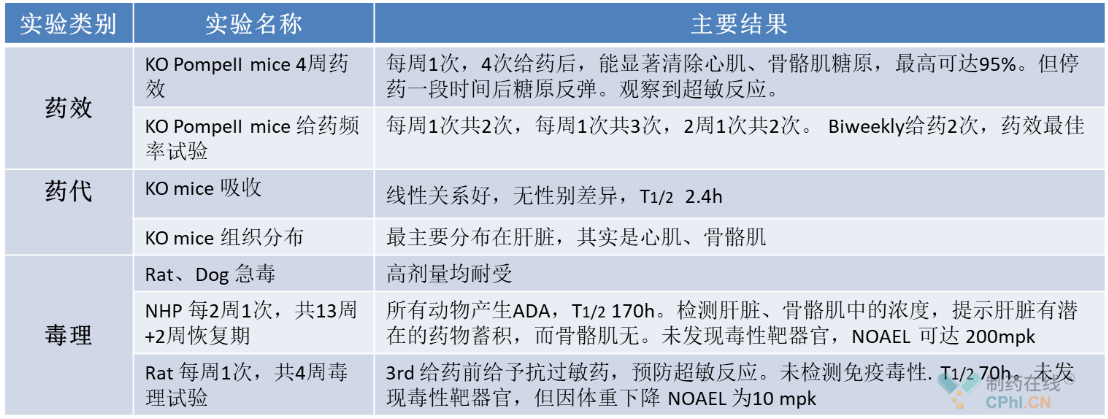
Myozyme于2006年获得FDA批准,适应症为庞培氏病,也叫糖原贮积症Ⅱ。临床给药方式/频率:IV Infusion,2周1次。分子量110kDa。Myozyme开展的药效、药代、毒理实验总结如下。
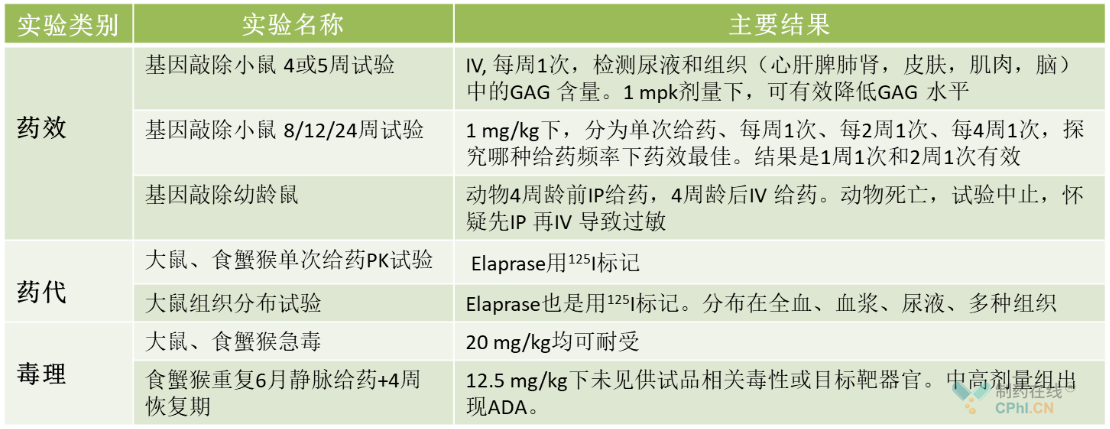
Elaprase于2006年获得FDA批准。适应症为亨特综合征(粘多糖贮积症II,MPS II),是MPS 中唯一一个X连锁隐性遗传疾病,多发于男性,该疾病特点是由于缺乏硫酸艾杜糖醛酸硫酸酯酶,黏多糖沉积于细胞内,导致发育落后、骨骼及面容呈轻度胡勒综合征。给药方式/频率:每周一次,静脉输注,0.5 mg/kg,分子量76kDa。Elaprase开展的药效、药代、毒理实验总结如下。
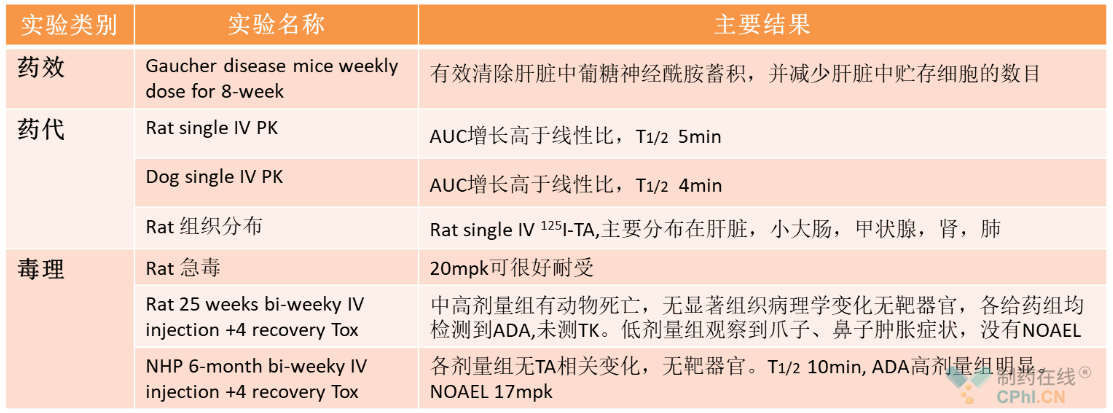
Vpriv 于2010年获得FDA批准。适应症为I型戈谢病,疾病特点:溶酶体酶β-葡萄糖脑苷脂酶缺乏,从而产生泡沫细胞。临床特征反映器官肿大。 临床给药方式/频率:2周1次,IV 60min,分子量63kDa。
根据已上市几款药物临床前分析,我们总结了酶替代疗法药物临床前安评策略。药效:通过转基因鼠,探索最 佳药效剂量、给药频率等。药代:吸收实验,需注意有些药物T1/2短,采血时间点前面要密集设置;组织分布,有些会使用同位素碘标记。毒理:急毒,最重要的是长毒试验,给药频率、次数≥临床,相关种属通常是大鼠和猴),免疫毒 性伴随考察,通常只做ADA, 注意是否有过敏反应。遗传毒、TCR、溶血等实验不需要考察。
根据EvaluatePharma发布的报告,2017年-2022年,预计孤儿药市场复合增长率为11.1%,远高于非孤儿药市场。到2022年,预计孤儿药的销售总额占全球药物销售额的21.4%,孤儿药研发有广阔的市场空间。孤儿药研发离不开政策的支持。以美国为例,美国在1983就颁布《罕见病用药法》,药物上市后,享有7年市场独占期,享受50%税金减免,纳入医疗保障制度,之后又推出了孤儿药审评的特殊待遇,使得孤儿药的社会认知度不断提高。近年来,中国关于罕见病各种政策,陆续出台。在此重点介绍2个政策。比如大家熟悉的2017年10月,发布的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,该政策提到,对于罕见病,加快审评审批,对于符合要求的,可以直接批准进口。2018年5月发布的《关于公布第一批罕见病目录的通知》:纳入121种罕见疾病,为罕见病药物的研发方向、临床诊治、医保准入提供重要依据。其它政策还有:如2019年发布的《关于印发罕见病诊疗指南的通知》,《关于罕见病药品增值税政策的通知》,2020年发布的《药品注册管理办法》,为罕见病研发提供了支持。目前,一些新技术应用于在孤儿药研发中,如核酸技术,2018年第一个siRNA 药物Onpattro获批上市后,适应症是罕见病。关于基因治疗,AAV(腺相关病毒)是主要手段。 其它技术,如基因编辑,酶分子定向进化,均从基因水平治疗罕见病。因为 80%以上的罕见病都是由基因突变引起的,相信基因治疗也是将来罕见病治疗的方向。
因为有爱,所以同行。新药研发不容易,罕见病新药研发更不容易。想起了鲁迅《呐喊》中的一句话:有时候仍不免呐喊几声,聊以慰藉在寂寞里奔驰的猛士,使他不惮于前驱。也希望罕见病研发人员和罕见病患者,不惮于前驱。让“罕见病”不“罕治”是全球性的挑战,让我们一起努力!
参考文献:
[1]Pharmacology Review(s)/of Myozyme (Alglucosidase Alfa) [EB/OL]. (2006-04-28). https://www. accessdata.fda.gov/drugsatfda_docs/nda/2006/125141s0000_Myozyme_PharmR.pdf.
[2]Pharmacology Review(s)/of Elaprase (Indursulfase) Injection [EB/OL]. (2006-07-24). https://www. accessdata. fda.gov/drugsatfda_docs/nda/2006/125151s0000_Elaprase_PharmR.pdf.
[3]Pharmacology Review(s)/of Vpriv (Velaglucerase alfa) Injection [EB/OL]. (2010-02-26). https://www. accessdata.fda.gov/drugsatfda_docs/nda/2010/022575s000pharmr.pdf.
作者简介:磐盛,美国PMP认证(项目管理专业人士资格认证)。目前在国内医药外包行业龙头上市公司从事临床前项目管理工作,工作内容主要涉及药效、药代、毒理、注册申报的项目管理。通过端到端的全程项目管理,赋能全球客户,为客户提供一体化新药研发及全球申报解决方案,助力更多药物获批临床。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57