6月26日,在今年的美国糖尿病学会(ADA)年会上,礼来公布了其在研新药Retatrutide在肥胖和非酒精性脂肪性肝炎(NASH)治疗中的最新临床试验数据。
Retatrutide是一种葡萄糖依赖性胰岛素性多肽(GIP)、胰高血糖素样肽1(GLP-1)和胰高血糖素(GCG)多重受体激动剂。在此次公布的随机、双盲II期临床试验中,入组338例受试者:
在减重领域,与安慰剂相比,所有剂量(1mg、4mg、8mg、12mg)的Retatrutide治疗均显示出具有临床意义的体重减轻,且对女性的减重效果更佳。每周注射Retatrutide(12 mg),48周后受试者平均体重减轻24.2%,这是迄今为止药物减肥能达到的最好效果。每周注射Retatrutide(12 mg),所有受试者可实现减重>5%;近一半受试者可实现减重≥25%;1/4的受试者可实现减重≥30%。每周注射剂量为8 mg时,48周后所有受试者实现减重>5%。
安全性方面,Retatrutide 治疗组中最常见的不良事件是胃肠道不良事件,严重程度一般为轻至中度,通常发生在剂量递增期间。Retatrutide在肥胖治疗中的疗效和耐受性良好。
在NASH治疗领域,Retatrutide在98例NASH亚群有效性和安全性探索数据显示:所有剂量组的Retatrutide均展现出了强大的肝 脏脂肪减少效果,且NASH相关的生物标志物也有显著改善。在Retatrutide的8mg和12mg治疗剂量下,受试者平均相对肝 脏减脂率>80%;实现减脂率≥70%的患者占比超过80%;且48周时超过85%的患者肝 脏脂肪变性消失。
Retatrutide的这一数据,让大部分治疗NASH的药物感到了严重威胁。事实上,NASH已成为GLP-1下一个竞争焦点。
GLP-1的下一片疆土——NASH
非酒精性脂肪性肝病(NAFLD)是指酒精和其他明确的损肝因素之外所导致的肝细胞内脂肪过度沉积引发的代谢应激性肝 脏损伤。NASH是NAFLD的严重形式,根据流行病学数据,15%~25%的NAFLD患者最终会发展为NASH。NASH可能继续发展成进行性纤维化,并且与肝癌的发生风险直接相关。
目前,除了印度批准的一款PPARα激动剂saroglitazar外,NASH几乎无药可治。NASH已成为全球最迫切的临床未满足需求之一,市场空间巨大。根据弗若斯特沙利文预测,到2025年治疗NASH药物的市场容量将超过100亿美元,其中2016-2025年复合增长率可达20.19%。
随着对GLP-1靶点研究的深入,研究者发现GLP-1与肝 脏细胞受体结合后能降低肝 脏脂肪变性、肝细胞损伤和葡萄糖输出,在 NASH 中能降低肝细胞炎性反应和纤维化。那么,GLP-1类药物在NASH治疗领域取得了哪些进展呢?
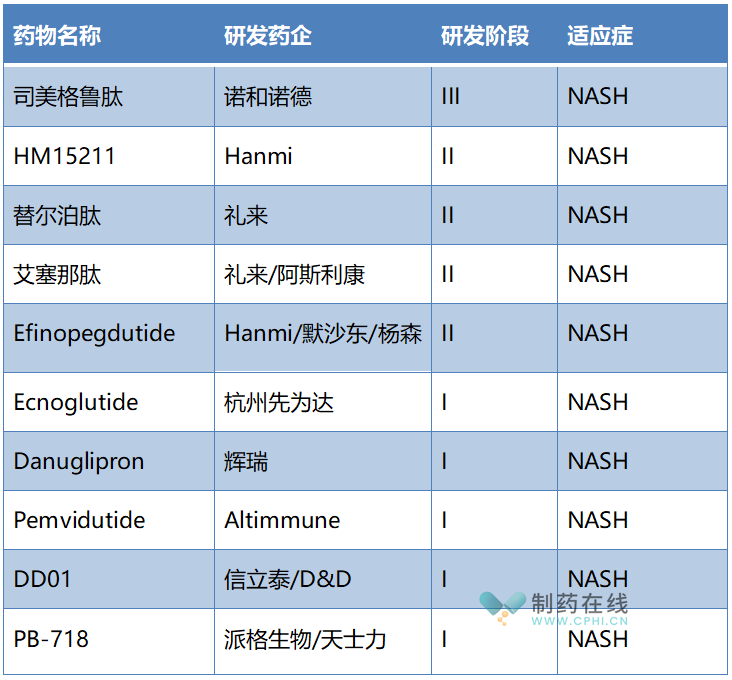
NASH治疗领域在研GLP-1类药物(公开资料)
司美格鲁肽
根据诺和诺德公告,司美格鲁肽在治疗NASH的II期临床中结果积极,在接受最高剂量司美格鲁肽治疗组的患者中,66.7%患者的NASH症状得到消除;在改善患者肝纤维化方面,在接受最高剂量司美格鲁肽治疗的患者中,有5.8%患者肝纤维化出现进展(安慰剂组为21.4%)。
HM15211
HM15211是Hanmi(韩美制药)基于其专有的长效蛋白/多肽发现技术平台开发的一款GLP-1/GCG/GIP-Fc融合蛋白,在大鼠体内,其半衰期长达82.8~85.7小时。临床前研究显示,HM15211可以重组肝脂质代谢基因表达,改善肝 脏炎症和肝纤维化。目前,Hanmi正在开展其用于NASH治疗的II期临床试验。
Efinopegdutide
Efinopegdutide是一种GLP-1R/GCGR激动剂,由Hanmi研发。2020年8月,默沙东以1000万美元预付款从Hanmi获得Efinopegdutide全球范围内除韩国外用于NASH的独家权益。
在Efinopegdutide用于治疗NASH的IIA期临床研究中,145例患者随机接受Efinopegdutide(每周10毫克)或司美格鲁肽(每周1毫克)的治疗。试验结果显示,24周后,Efinopegdutide组的肝 脏脂肪水平减少72.7%(95% CI:66.8,78.7),活性对照组为42.3%(95% CI:36.5,48.1)。Efinopegdutide目前正在进行临床II期研究,用于治疗NASH。
Pemvidutide
Pemvidutide是一款GLP-1R/GCGR双重受体激动剂,正在开发用于治疗肥胖和NASH。2022年9月,Altimmune宣布了Pemvidutide在NAFLD患者中的Ib期研究结果:在第12周时,各剂量Pemvidutide组均达到了肝 脏脂肪含量(LFC)的主要终点,其中,1.8mg Pemvidutide组受试者的LFC较基线降低了68.5%。
DD01
DD01为韩国D&D公司开发的一款长效GLP-1R/GCGR双重激动剂,拟开发适应症为II型糖尿病、肥胖、NASH等疾病。2021年9月,信立泰与D&D达成合作,获得DD01相关知识产权、技术信息于中国大陆地区的独家许可权。
目前,DD01正在美国开展以患有NASH、肥胖型2型糖尿病患者为受试者的I期临床试验。目前尚未在国内申报临床。
PB-718
PB-718是派格生物自主开发的一款GLP-1R/GCGR双重激活剂。它能够同时激活GLP-1及GCG受体,通过平衡两种受体的激活程度,产生协同作用,实现优于单一作用机制的减重及改善脂肪代谢的效果。目前,PB-718正在美国开展针对NASH的I期临床研究。
GLP-1就像一座富矿,可以作用于人体中广泛存在的受体,发挥降糖减肥、护心益脑等诸多功效。在GLP-1减重赛道火热的当下,新的战火迅速延伸到下一个百亿市场:NASH。新领域的揭幕往往带给后来者换道超车的机会,未来市场将如何演变,我们拭目以待。
主要参考资料:
1、Jastreboff AM. et al. “Triple–Hormone-Receptor Agonist Retatrutide for Obesity — A Phase 2 Trial” (2023) N Engl J Med. DOI: 10.1056/NEJMoa2301972;
2、Potent body weight loss, and therapeutic efficacy in a NASH animal model by a novel long-acting GLP-1/GIP/Glucagon tri-agonist (HM15211). EASD 2017;
3、Merck Gets FDA Fast Track for Efinopegdutide, Previews NASH Data Versus Novo’s Semaglutide(biospace);
4、http://data.eastmoney.com/notices/detail/002294/AN202109221517872702.html.



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57