笔者近来读了一篇题目为《【质量体系严重偏离GMP】两药企被处罚!》的文章,看到读者留言想知道药企缺陷如何分级。笔者今天试着就药企缺陷如何分级进行分享。
2021年5月24日,国家药品监督管理局发布了《药品检查管理办法(试行)》。该办法将GMP缺陷分为"严重缺陷"、"主要缺陷"和"一般缺陷",其风险等级是依次降低的。下图是笔者就检查过程发现的缺陷风险等级的确定制定的流程。
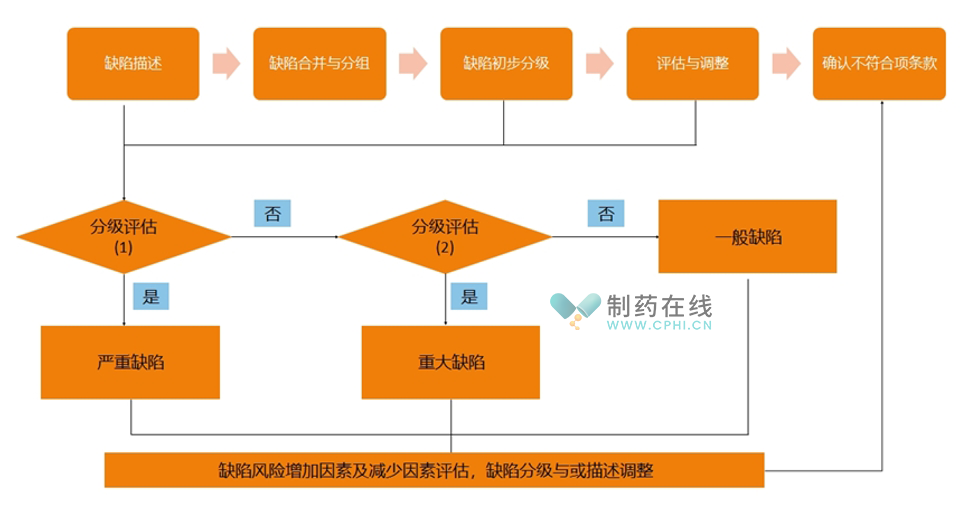
首先、缺陷的描述。GMP检查缺陷的描述应客观、准确、清晰。一般用5W2H进行描述,即何人何时在何地发现了因为特定原因引发的特定事情;该事情是如何发生的且数量多少。
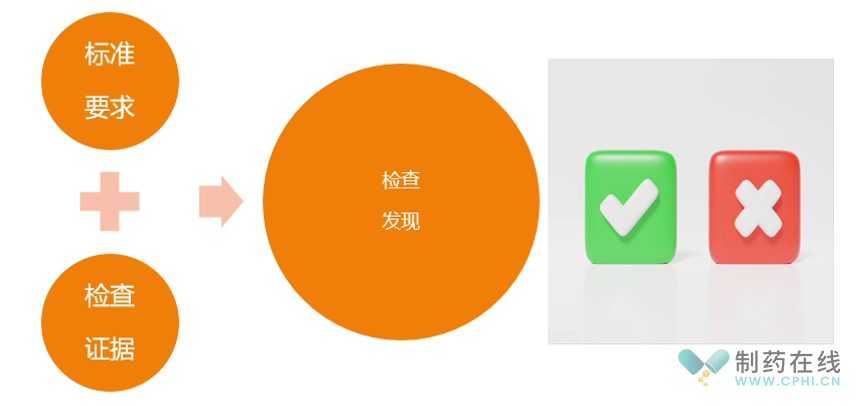
药品检查缺陷描述的要求,包括标准要求、检查证据和缺陷3个部分。同时需要明确区分该问题是程序规定本身的缺陷,还是未遵循程序规定产生的缺陷。
当有1项以上的缺陷涉及质量体系同一项基础性工作,通常应将此类缺陷进行合并和分组,并作为1个缺陷项进行缺陷分级。在实际检查中,通常最终完成缺陷合并、分组和分级后确认不符合条款。
其次、缺陷分级。
缺陷分级可以分为缺陷初步分级、评估与调整两个环节。
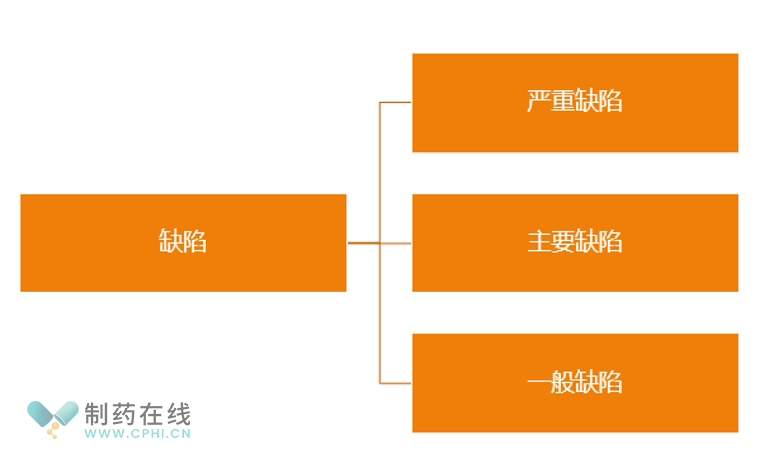
第一、缺陷的初步分级。缺陷初步分级是基于不同级别缺陷的定义对首次缺陷项进行的划分。缺陷通常分为"严重缺陷"、"主要缺陷"和"一般缺陷"。
1、严重缺陷。严重偏离给产品质量带来严重风险一般包括:污染风险,交叉污染风险,关键设备、关键性人员、质量体系的重大风险,即此项缺陷单独就可能对使用者造成危害。具体包括可能对使用者健康造成危害;故意篡改、歪曲、伪造数据的行为;与GMP 要求有严重偏离,对产品质量带来严重风险;多项关联主要缺陷总体表明某一系统不能有效运行的。
2、主要缺陷。经评估认为不属于严重缺陷,则进行主要缺陷的评估。主要缺陷一般包括严重缺陷以外的,可能导致产品不符合质量标准的缺陷、不能确保GMP 控制措施的有效实施的缺陷、影响产品质量属性或关键操作与参数或工艺设备的缺陷、关键人员履职不足导致放行符合上市许可产品等较大问题的缺陷。具体包括与GMP 要求有较大偏离,对产品质量带来较大风险;产品不能按要求放行或质量受权人不能有效履行放行职责;多项关联一般缺陷表明某一系统不完善。
3、一般缺陷。若评估认为不属于主要缺陷,则评级为一般缺陷。
第二、缺陷评估与调整。缺陷初步分级后,需要结合缺陷风险增加因素和缺陷风险减少因素开展进一步的评估。
1、风险增加。风险增加因素包括:重复出现的缺陷;缺陷的组合和合并;产品风险,对于一些高风险产品,某些一般缺陷或主要缺陷需要升级为主要缺陷或严重缺陷。
2、风险减少。风险减少因素包括产品风险因素和其他风险降低因素两类。对于一些低风险产品,某些主要缺陷或严重缺陷需要降为一般缺陷或主要缺陷。其他风险因素降低因素通常只有在已经建立了可以降低相关缺陷风险的辅助或相关系统时考虑。
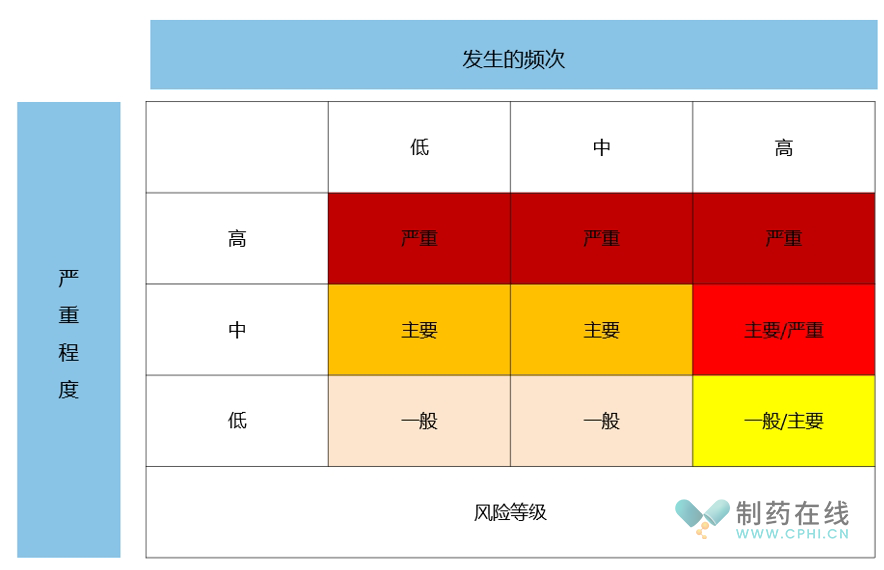
3、风险等级的确定。这包括确定缺陷风险的严重程度、确定缺陷发生的频次和确定缺陷的风险级别三部分。
确定缺陷风险的严重程度。根据严重缺陷和主要缺陷的评定标准,严重缺陷的严重程度为"高";主要缺陷的严重程度为"中";一般缺陷的严重程度为"低"。
确定缺陷发生的频次。根据检查发现,同一事项的缺陷小于等于3 条的为"低";同一事项的缺陷在3~5 条的为"中";同一事项的缺陷5 条以上为"高"。
确定缺陷的风险级别。根据缺陷风险的严重程度,以及同一事项缺陷发生的频次,对缺陷风险等级进行调整。如果同一事项的缺陷发现超过5次,即合并后将缺陷等级升高一级。
最后,确认不符合项条款。基于缺陷分级的进一步的评估后,每项缺陷的内容已基本确定,最后需要对应完善每条缺陷的法规标准依据。
作者简介:老陈,质量管理专家,从事食品与制药行业质量管理和质量控制相关工作近二十年,历任QA主管、质量部长、质量经理和生产厂长等职。在国内著名的跨国明胶企业负责质量和食品安全管理体系管理工作。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57