2024年2月8日,Alector Therapeutics公司和GSK宣布,美国FDA已授予在研抗体疗法latozinemab突破性疗法认定。这款潜在"first-in-class"人源化单克隆抗体旨在抑制名为sortilin的受体蛋白,从而提高颗粒蛋白前体(PGRN)的水平,目前正用于治疗带有编码PGRN的GRN基因突变的额颞叶痴呆(FTD)患者。
这一突破性疗法认定是基于名为INFRONT-2的2期临床试验结果。试验数据显示,latozinemab将患者血浆和脑脊液中PGRN水平恢复到年龄相当的健康志愿者的水平。同时,初步评估数据显示,与历史对照相比,latozinemab可能减缓患者的疾病进展。
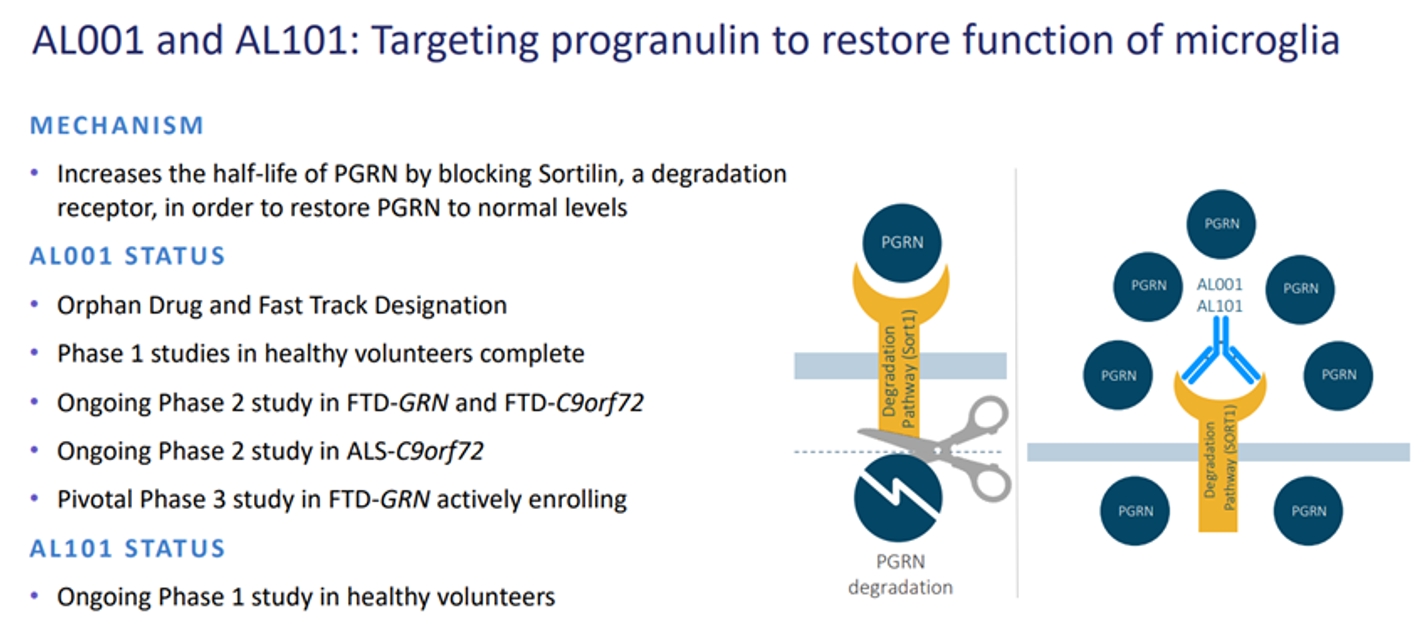
2022年阿尔茨海默氏症和帕金森病会议上公布了AL001治疗具有 C9orf72 突变的FTD的12 个月INFRONT-2 II期临床结果(60 mg/kg q4w for 96 weeks)。公布的试验结果显示,AL001表现出良好的安全性和耐受性,并且迅速提高血浆和脑脊液(CSF)中的PGRN蛋白水平。接受AL001的患者,与匹配的历史对照组相比,临床症状进展速度减缓54%。
图片来源:Alector Therapeutics官网
Latozinemab(AL001)是一种针对PGRN的单克隆抗体。PGRN是大脑内免疫反应的关键调节因子,与多种神经退行性疾病(包括FTD、阿尔茨海默病和帕金森病)相关。Latozinemab的作用机制涉及抑制sortilin,这是介导PGRN降解的受体,目的是提高患者的PGRN水平。它已经获得FDA授予的孤儿药资格、快速通道资格和突破性疗法认定。2021年7月,Alector公司与葛兰素史克(GSK)达成数额可达23亿美元的研发合作,其中包括联合开发AL001。GSK通过与Alector的一项交易重返脑部药物研究领域。
关于额颞叶痴呆(FTD)
额颞叶痴呆(Frontotemporal dementia,FTD)是早发性(中年)痴呆的常见原因之一,会导致患者行为、语言和执行功能的损害,并且在65岁以下的患者中,发生率与阿尔茨海默病相似。FTD表现为一种快速进展的临床综合征,疾病的早期阶段会出现个人和社会行为的变化,包括抑制力丧失、冷漠、回避社交、把任何看得到的东西塞进嘴里和强迫行为。这些症状严重致残,并可能被误诊为心理或情感问题;在老年人中,被误认为是回避或怪癖。FTD逐渐发展为不能动,言语和表达能力的丧失。FTD症状常隐匿发作,患者通常在45-65岁、平均58岁出现临床症状,平均预期寿命为症状出现后7-10年。FTD的疾病进展快于阿尔兹海默病,增加了该病的严重程度和患者未满足的医疗需求。FTD的疾病进展快于阿尔兹海默病,增加了该病的严重程度和患者未满足的医疗需求。
在大约5%到10%的FTD病患者中,是由GRN基因突变引起,导致progranulin蛋白缺乏。PGRN是一种复杂且高度保守的蛋白质,被认为在细胞生物学、发育和炎症中具有多重作用。新出现的证据表明,PGRN对FTD和其他神经退行性疾病的致病作用与溶酶体功能的关键作用有关。因此是新的免疫神经病学疗法开发中很具吸引力的基因验证靶点之一。
FTD基因疗法方兴未艾
目前尚无批准用于治疗FTD的药物,除了此次获得FDA突破性认定的抗体疗法latozinemab外,还有多款针对FTD的基因疗法已经进入临床试验阶段并展现出了巨大的应用潜力,下面笔者将对这几款基因疗法进行简要的介绍和分析。
AVB-101是由AviadoBio研发的专为带有Progranulin(GRN)基因突变的FTD患者而设计的腺相关病毒(AAV)基因疗法。AVB-101已被设计为一种潜在的一次性疗法,通过微创立体定向神经外科手术,将AAV9载体直接输送到大脑中的丘脑部位,传递GRN基因的功能副本以恢复颗粒蛋白前体的正常表达,从而阻止疾病的发展。AVB-101通过丘脑内给药,利用大脑的神经网络提高载体的生物分布,将治疗限制在最需要的脑部,实现基因的最大化广泛表达,同时减少所需剂量和潜在的全身暴露。目前AVB-101已经启动了其研究性基因疗法AVB-101的1/2期ASPIRE-FTD临床研究,旨在评估AVB-101在FTD GRN患者中的安全性和初步疗效。
除了AviadoBio,由基因治疗领域先驱、AAV大牛James Wilson创办的Passage Bio公司也布局了治疗FTD的AAV基因疗法。Passage Bio的基因治疗候选产品PBFT02是一种针对FTD-GRN的新型基因疗法,可以将编码GRN的修饰DNA传递到患者的细胞中。载体将通过单次注射直接传递到脑脊液(CSF)。这种载体和递送方法的目标是向CNS提供高于正常水平的PGRN,以克服GRN基因突变携带者中的PGRN的缺乏。Passage Bio也已将其基因治疗候选药物推进到1/2期临床试验。
此外,由Prevail Therapeutics开发的AAV9基因疗法PR006同样值得关注。Prevail正在进行PR006治疗FTD-GRN患者的1/2期研究,此前PR006被授予治疗FTD的孤儿药称号和用于FTG-GRN的快速通道指定。
参考来源
1. 各企业官网
2. Alector Corporate Presentation. Retrieved February 7, 2024, from https://investors.alector.com/static-files/70f1e5de-e44d-43a7-9500-8af6a1ea80a5



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57