国内仿制药研发批准动态
01
新注册分类品种首家批准上市情况
根据药渡数据调研,本次统计周期(2024.04.27-05.03)新增2个新注册分类首家过评受理号,涉及1个注射液,1个混悬液。与上次统计周期相比,本次增加2个新注册分类首家过评品种。
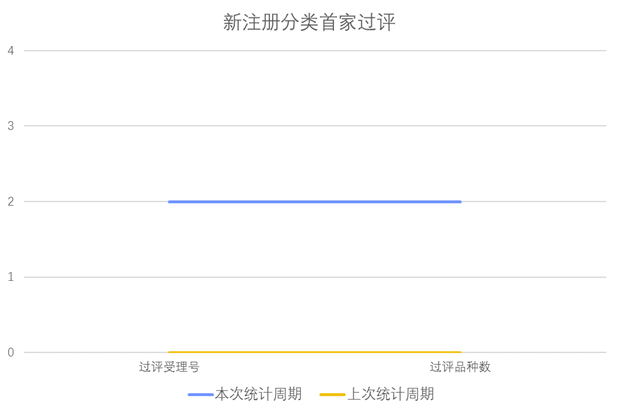
新注册分类品种首家过评情况
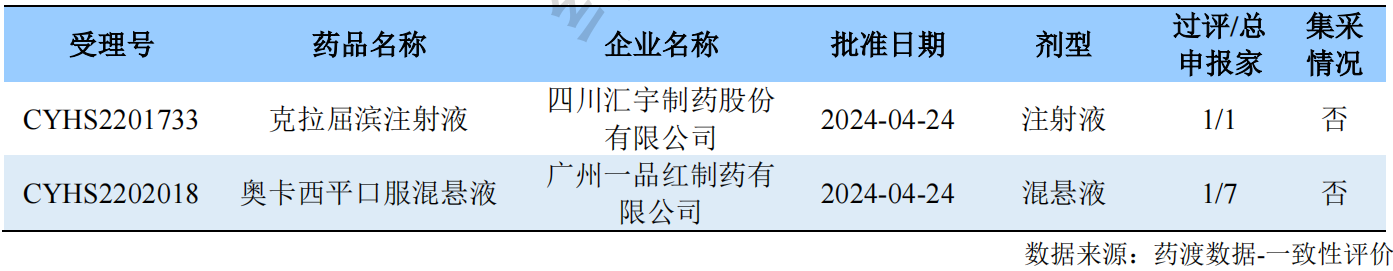
02
一致性评价品种首家批准上市情况
根据药渡数据调研,本次统计周期(2024.04.27-05.03)无新增一致性评价首家过评受理号。与上次统计周期相比,本次减少3个一致性评价首家过评品种。
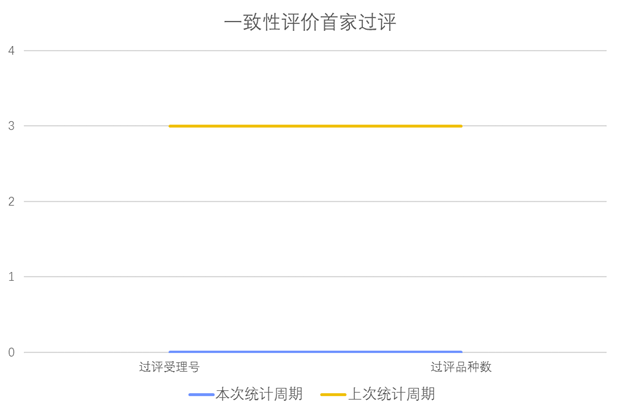
03
新注册分类品种批准上市情况
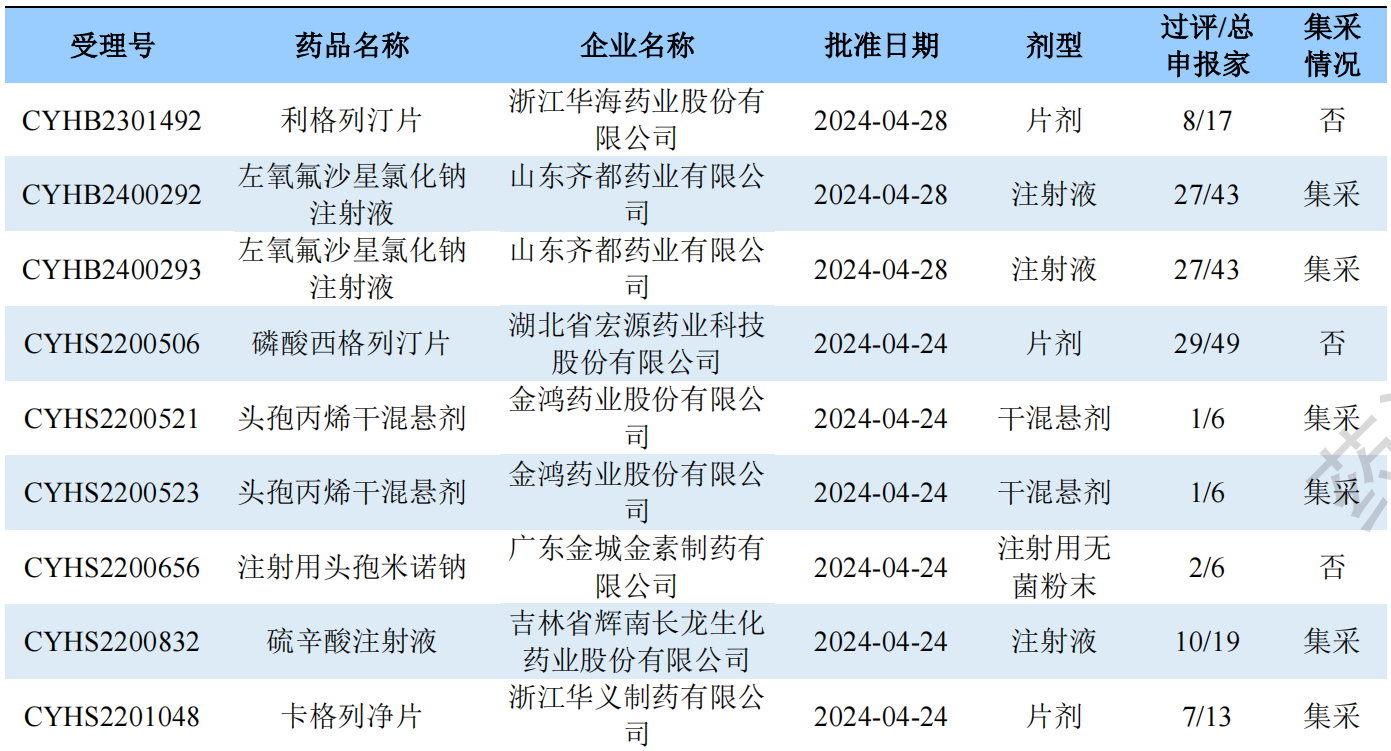
根据药渡数据调研,本次统计周期(2024.04.27-05.03)新注册分类新增43个过评受理号,涉及39个品种,包含4个滴眼剂,1个干混悬液,1个混悬液,2个胶囊剂,2个口服溶液剂,9个片剂,3个吸入溶液剂,17个注射剂。与上次统计周期相比,本次新注册分类过评品种与上周持平。
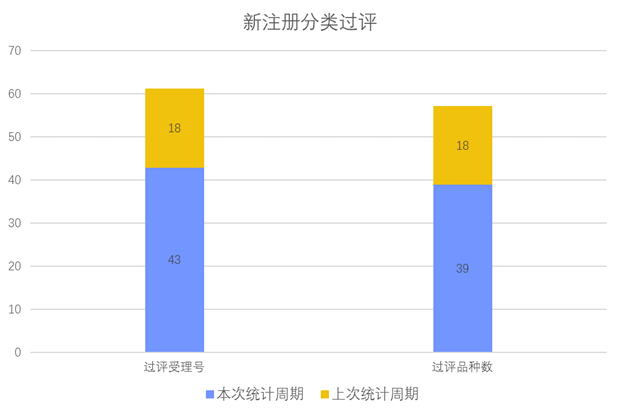
新注册分类品种过评情况(部分)
喷他佐辛注射液
喷他佐辛是由丸石制药开发的阿片受体激动剂,临床上用于各种慢性剧痛,如癌性疼痛、创伤性疼痛、手术后疼痛等,也可作为外科手术麻醉的辅助用药,用于手术前或麻醉前给药,属于第二类精神药品。
喷他佐辛注射液最早于1970年3月24日获PMDA批准在日本上市,1998年华润双鹤药业的首仿药物经NMPA批准在国内上市销售。
根据药渡数据-仿制药库调研,目前喷他佐辛注射液原研尚未进入国内,国内共有3家企业拥有喷他佐辛注射液的生产批文。其中,安徽恒星制药于去年11月24日视同过评,成功拿下该品种的“首家过评”称号;此次过评的福安药业庆余堂制药为该品种的第2家过评企业。
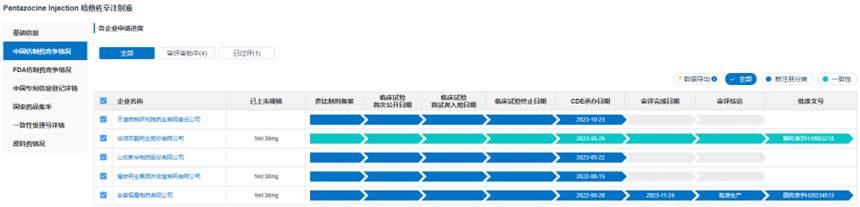
药渡数据-中国注册库信息显示,喷他佐辛注射液注册格局为“1+4”,过评格局为“0+2”。“首仿”企业华润双鹤药业的一致性评价申请目前正在审评审批中。

此外,另有4家企业递交了喷他佐辛注射液的新3类报产申请,除了首家过评的安徽恒星制药和此次视同过评的福安药业庆余堂制药,其他2家企业的报产申请尚在审评审批中。

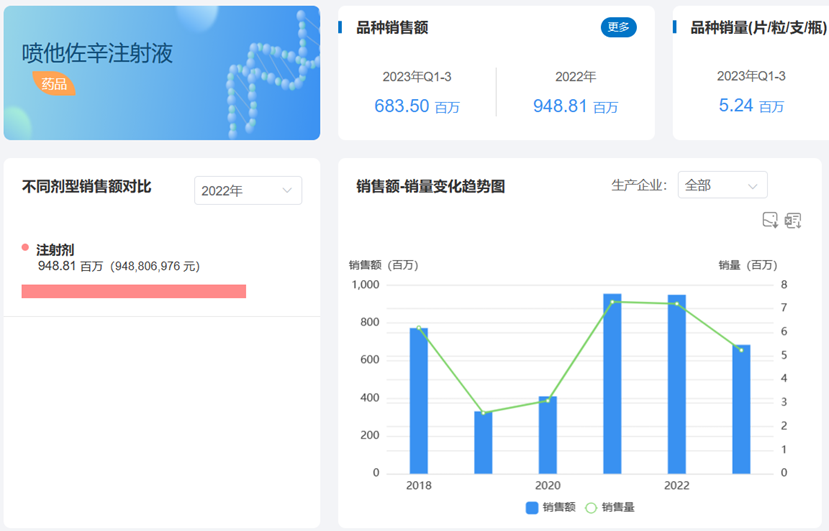
药渡数据-中国销量库统计数据显示,喷他佐辛注射液近年来销售情况喜人,2022年度销售额接近9.5亿元,2023年前三季度销售额高达6.85亿元,全部市场份额由华润双鹤药业独家享有。随着越来越多的企业通过一致性评价审评,在不久的将来,华润双鹤药业一家独大的局面将被终结。未来市场格局如何变幻,药渡将持续关注。
04
一致性评价品种批准上市情况
根据药渡数据调研,本次统计周期(2024.04.27-05.03)一致性评价新增1个过评受理号,涉及1个品种,包括1个注射剂。与上次统计周期相比,本次减少15个一致性评价过评品种。
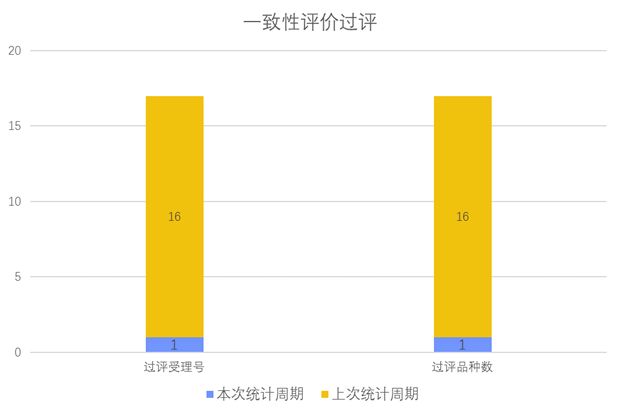
一致性评价品种过评情况

05
仿制药品种批准临床情况
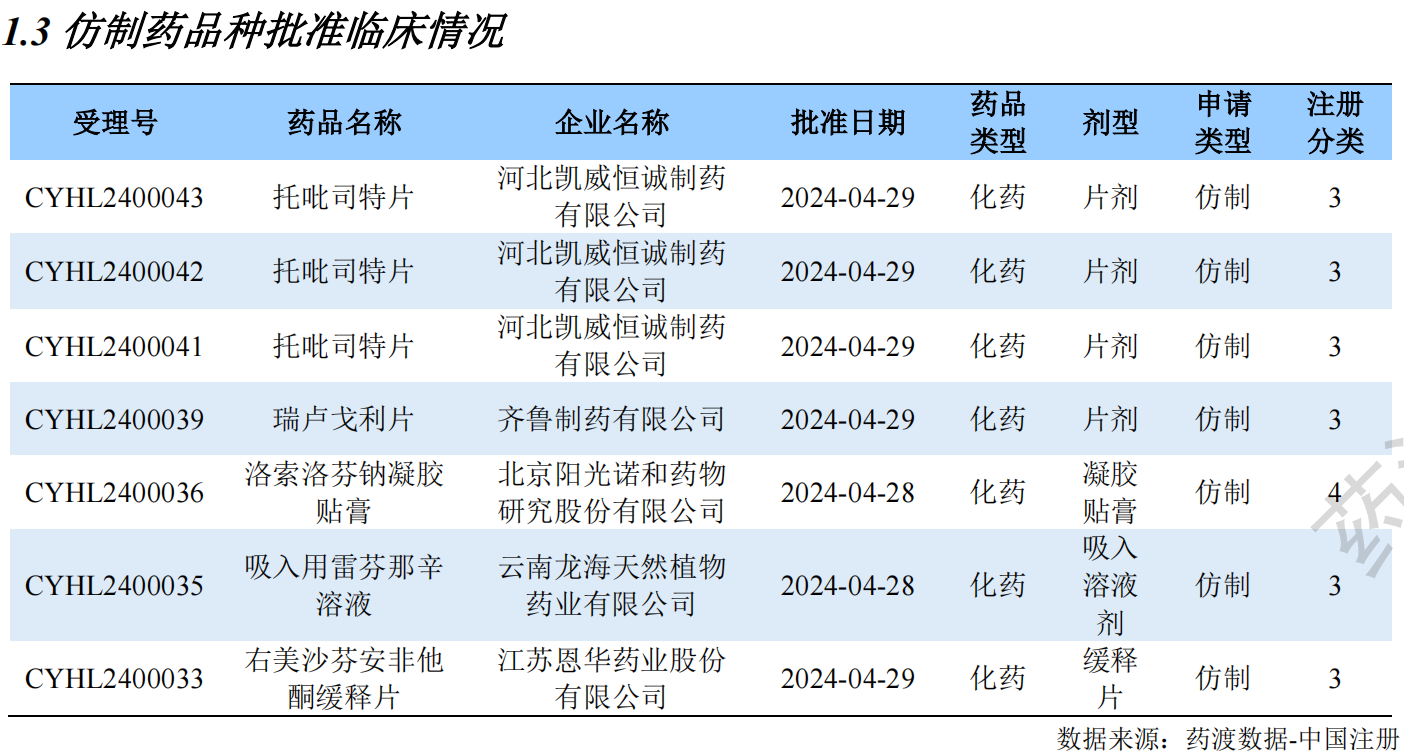
国内仿制药研发申报动态
01
新注册分类品种申报上市情况
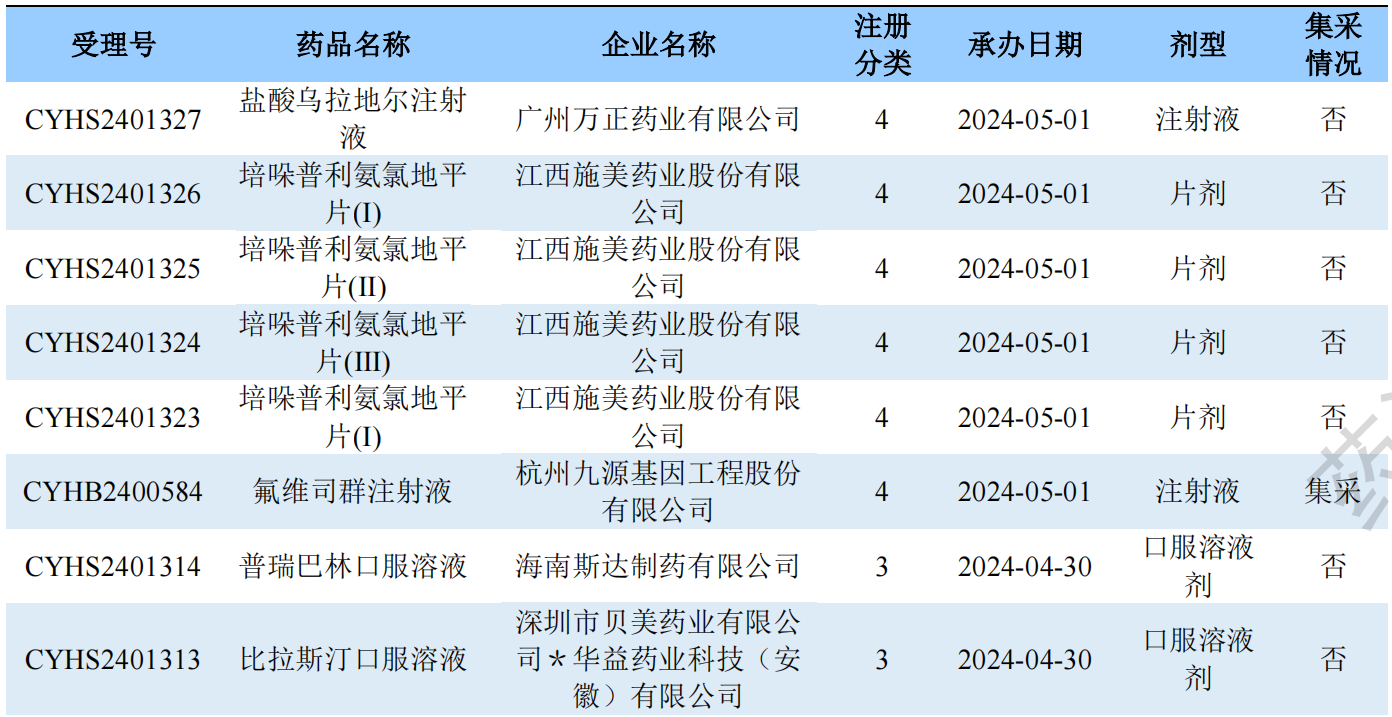
根据药渡数据调研,本次统计周期(2024.04.27-05.03)新注册分类数据新增49个新报受理号,涉及41个品种,包括1个滴剂,5个滴眼剂, 1个胶囊剂, 2个颗粒剂,4个口服溶液剂,12个片剂, 2个散剂,1个糖浆剂, 1个吸入溶液剂,12个注射剂。与上次统计周期相比,本次新注册分类申报品种与上周持平。
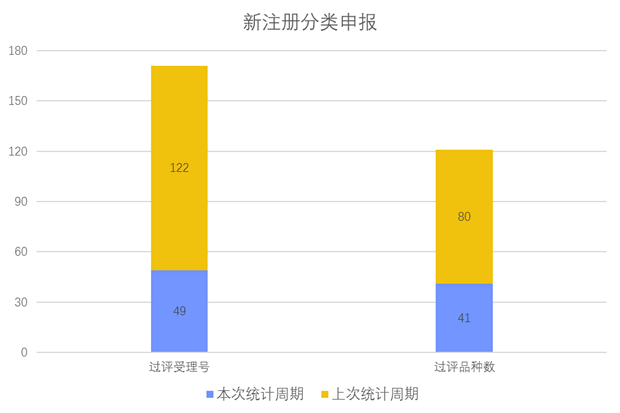
新注册分类品种申报受理情况(部分)
02
一致性评价品种申报上市情况
根据药渡数据调研,本次统计周期(2024.04.27-05.03)一致性评价数据新增6个新报受理号,涉及4个品种,包括1个胶囊剂,3个注射剂。与上次统计周期相比,本次增加2个一致性评价申报品种。
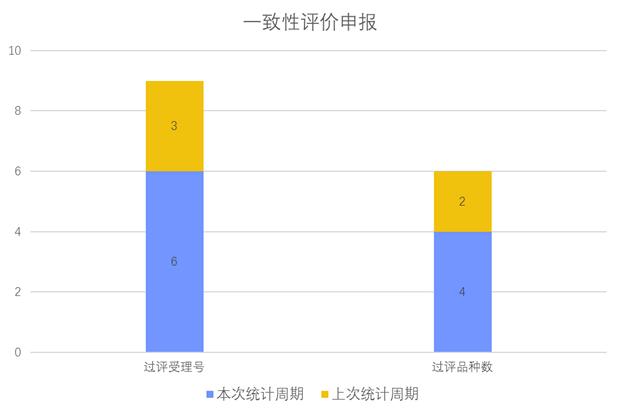
一致性评价申报受理情况
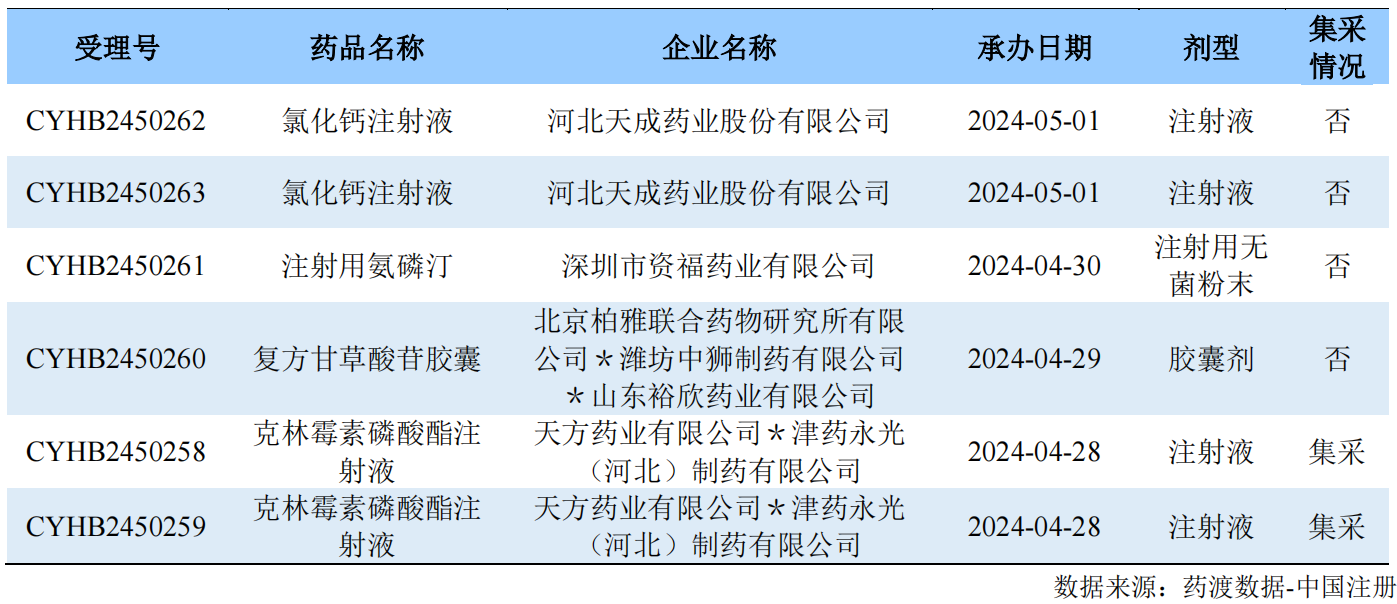
03
仿制药补充申请情况
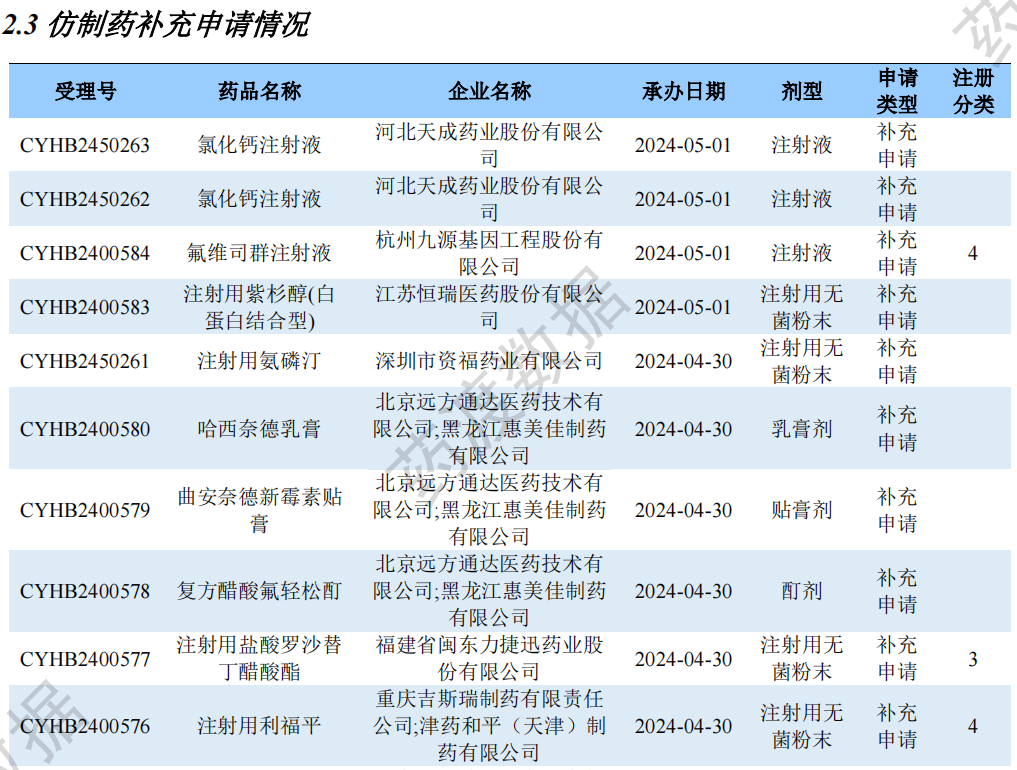
04
仿制药申报上市专利声明信息汇总
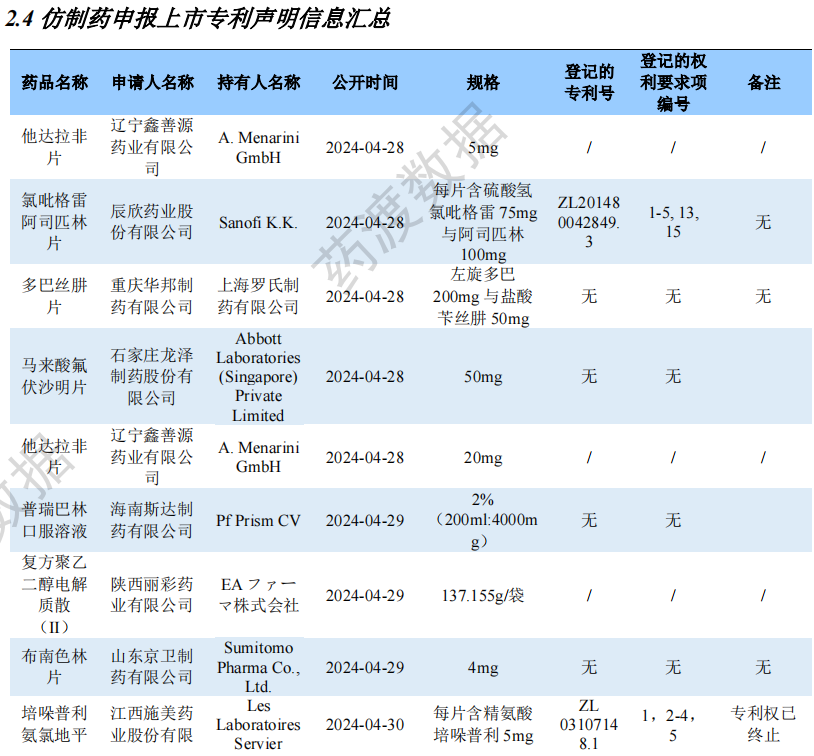
国内仿制药研发领域热点聚焦
01
国内仿制药研发领域政策法规相关动态
本周无仿制药研发领域相关政策法规发布。
02
国内仿制药研发领域热点新闻
金鸿药业:关于获得药品注册证书的公告
2024 年4月30日,金鸿药业股份有限公司发布公告称,本公司于近日收到国家药品监督管理局核准签发的关于头孢丙烯干混悬剂两个规格的《药品注册证书》。现将相关情况公告如下:
一、 药品基本情况
药品名称:头孢丙烯干混悬剂
剂型:口服混悬剂
规格:(1)1.875g (2)0.25g
注册分类:化学药品 3 类
药品批准文号:国药准字 H20243605
国药准字 H20243606
二、 对公司的影响及风险提示
公司高度重视药品研发,严格控制药品研发、生产及销售各环节的质量及安全。本次获得头孢丙烯干混悬剂的药品注册证书,将进一步丰富公司产品线,提高公司市场竞争力,对公司未来的经营业绩产生积极影响。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57