世界是个草台班子。
2024年7月17日,美国FDA公布了一则召回启事。一款0.25毫克规格氯硝西泮口服崩解片,因外包装标识规格错误,而发起召回。
图源:FDA
本身是0.25毫克规格的药品,在装药的泡罩条上,也标识的是正确的规格。但外包装上,则标识规格为0.125毫克。如果按照外包装的标量用药,会导致剂量翻倍。
作为一个用于治疗各种癫痫的药物,小儿常用量是根据体重来计算的,成年人每日用量不得超过20毫克。超量用药可能会导致严重的镇静、头晕、共济失调以及意识模糊,甚至呼吸抑制。尤其是肺部有疾病的患者用药,可能危及生命。

图源:FDA
从质量放行这个角度讲,很难说得通这个事件,因为这需要多个环节同时出问题,才会引发这种结局。泡罩条上的标识规格正确,说明本身就是按0.25毫克规格生产。那么对应的成品包装阶段,就要领用该规格的标签,仓库未必知道对应的规格,但领料的生产部必定知道要用的规格,竟然领错了。
当然如果是领用的空白标签,先装盒在贴签的同时打印规格和批号,那打印出来的前面几张,也应该核对相关信息,并把标签张贴在批生产记录本上。这个过程,至少要有一个负责复核的,竟然也没拦住进入下一流程。
到了成品质检这一步,质量部本身要把成品的各个指标都测一遍。包括规格含量,再对应着标识量以及请验单复核,理论上批生产记录的规格同请验单一致,都是0.25毫克,外包装不一致,这一步也应该能拦住。那么请验的到底是什么规格?竟然放行了。
到了成品入库这步,你除非就是写0.125毫克规格,否则也会被仓库拦住。然后也没拦住,不得不让人怀疑,这个产品在批生产记录、请验单、质检报告、入库单上到底是哪个环节错了?才导致后续都错了。还是说规格不断的跳跃变化,才导致未能察觉到?
当然,该公司产品肯定是也有0.125毫克规格的氯硝西泮口崩片,才会这样上错花轿。多数混淆的产生,都是由于名字或者标签本底的高度接近,导致防呆效果很差。其实标签的设计是个技术活,一方面要合规,另一方面要有公司特色,还要考虑到防混淆。
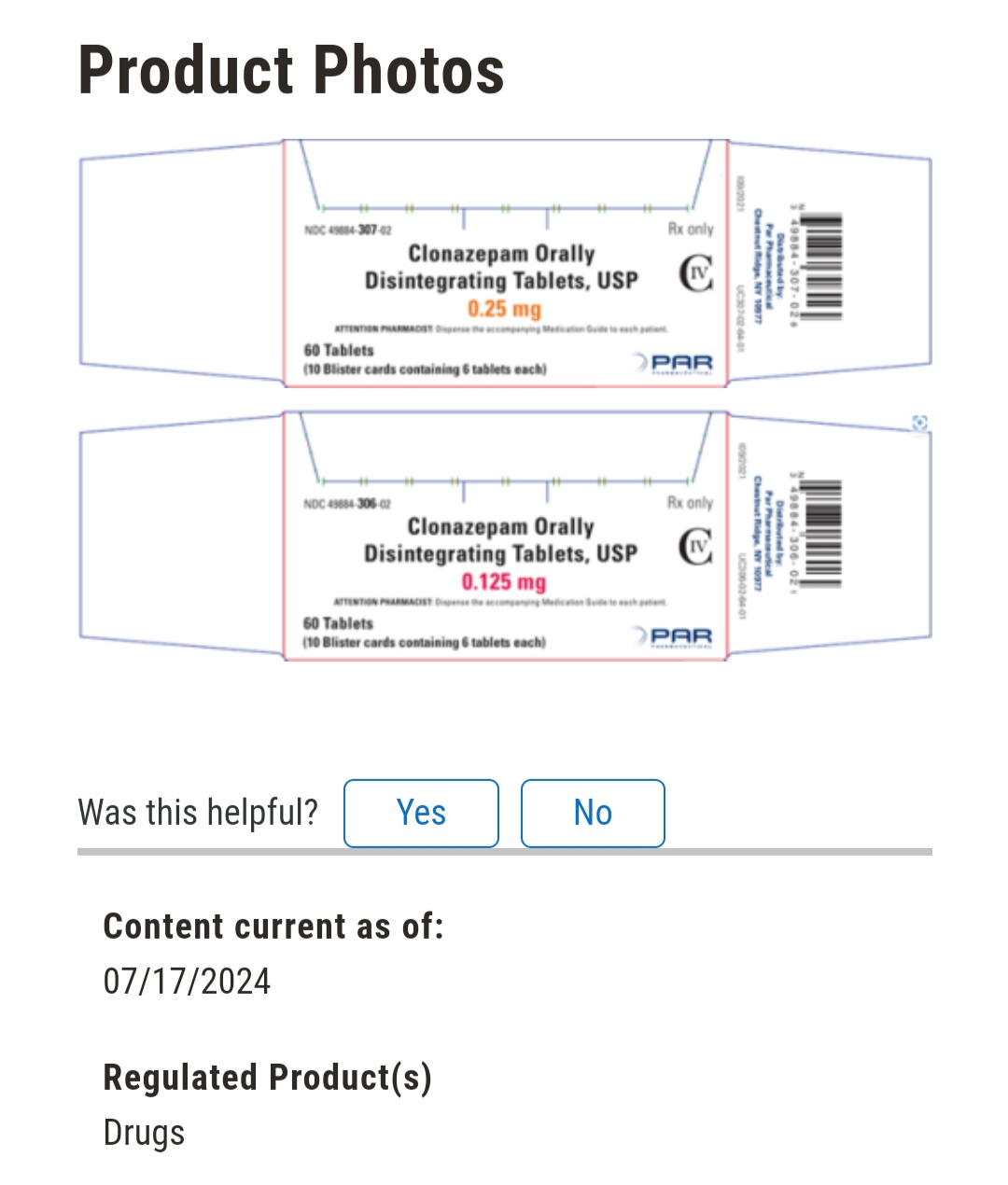
图源:FDA
很多公司能考虑到前面两条,第三条防混淆被第二条“公司特色”给抹杀了。但凡0.25和0.125规格的标签本底有很明显的差距,比如一个红一个蓝,那就很难不被有经验的包装工发现问题。
现在多个工序都没挡住混淆的出现,同时出现问题。可见整个质量体系,运行的并不通畅,世界真是个草台班子。
现在问题来了,这些召回的药品,是直接报废还是二次包装?
如果二次包装,那如何保证在外这段时间的储存是否恰当?那如何记录返工?生产日期要不要变更?反正成品检测是逃不过的。
后面的偏差调查咋写?本应提前发现的问题,咋就成了漏网之鱼?
偏差纠正是简单的一句加强培训?还是把责任推给生产或者质量?见得最多就是加强培训,把培训当成了救火英雄。
能不能直接变更产品标签本底颜色,做到从根源上做区分?这样做虽然说前期投入大,但能最大程度的做到防呆。相比于召回引发的问题,这其实反而是最经济最简单的。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57