漏液能叫漏液?不,那叫有微生物污染风险
8月8日,FDA公布了一则召回通知。一款1000毫升规格的生理盐水大输液,因为容器中存在颗粒物以及漏液的可能性,被召回。
图源:FDA
有些事,看到的现象,不一定是全貌,甚至同一现象,不同的描述也有不同的侧重点。就渗漏液体而言,一个无菌包装发生渗漏,则肯定会有外界空气进入包装的注射液。而除了生产灌装的区域,其他场所的空气大概率不是无菌的,因此空气的进入,会伴随着微生物以及外界尘埃等物质混入。当漏气,也就意味着无菌保障已经被破坏,至于原先有无颗粒异物,已经不是重点关注点。
当然,提存在颗粒物以及漏液,更大的可能是有些包装只是存在颗粒物,有些包装只是漏液,有些包装属于既有颗粒物又有漏液。至于最多是不是完好无损的合格品,已经不重要了,因为无法冒险使用。而且对于无菌大输液而言,价值不高,也无需冒太大的风险去试错。
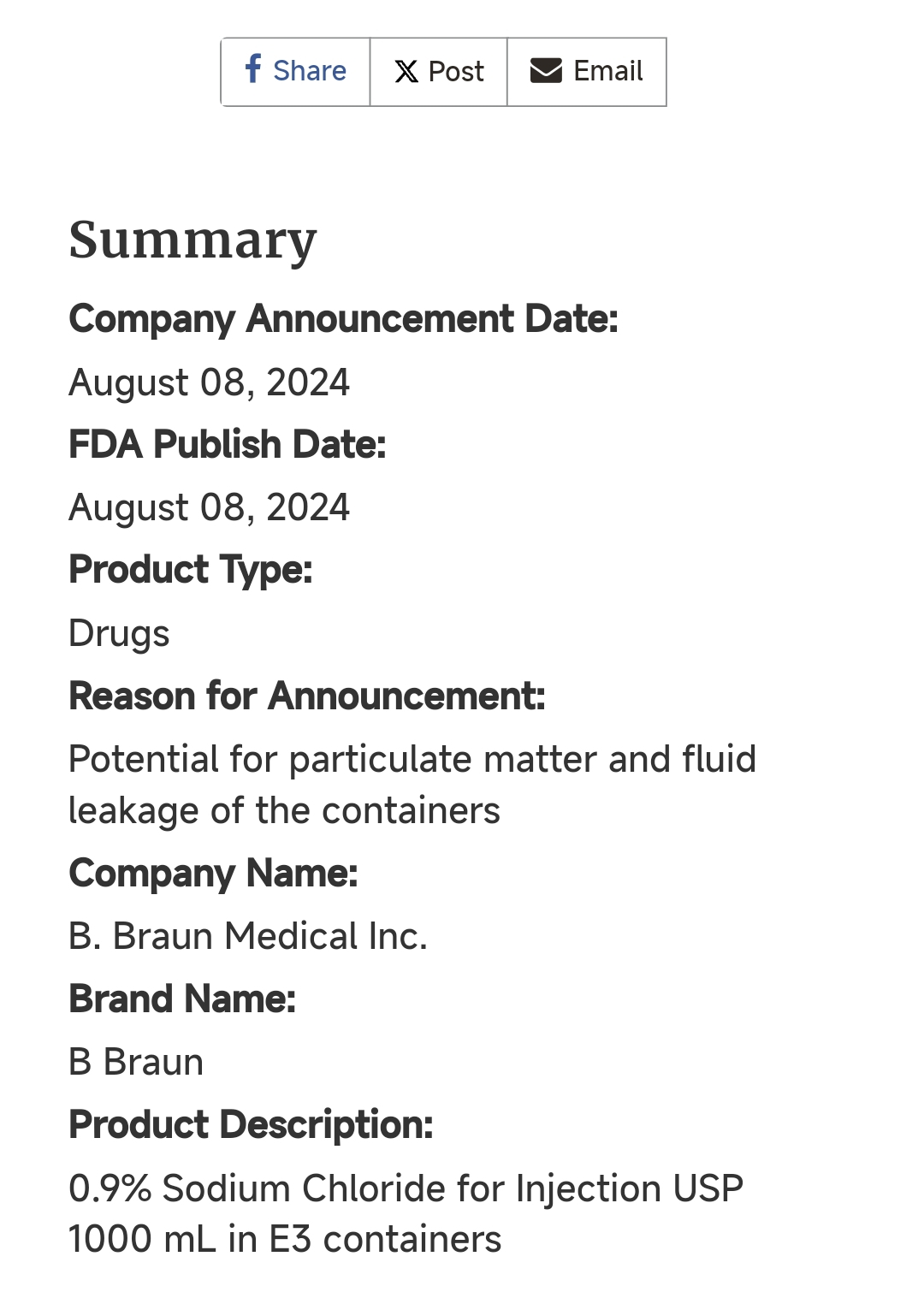
图源:FDA
在生产灌装区域,除了要求做沉降菌浮游菌等检测空气中微生物含量的项目外,还有尘埃粒子检测,看的是空气中尘埃粒子的数量,这个能反映出高效过滤器的功能。还有一点就是尘埃上可能附有微生物芽孢等等,所以尘埃粒子也关乎到无菌水平。
注射液常用的容器有玻璃安瓿瓶、玻璃瓶、塑料安瓿瓶、塑料瓶(袋子)等等,要做密封性方法确认。而且考虑到要观察有无异物等因素,这些包装往往是透明的,有避光要求的除外。就大输液而言,像这种1000毫升规格的,多是塑料袋包装,因为玻璃制品包装越大,越容易因为磕碰而出现质量问题。而塑料袋包装会引入另一个问题,可能会因为挤压以及接触到尖锐物品而产生破损。至于是不是那种随着注射液还配备注射用针头针管的,也不好说,我之前就遇到过,护士把针插入注射液做好封闭后,竟然有液滴不断的从针孔流出,最后及时反馈,换了一袋注射液。
1000毫升的生理盐水,往往是用于提供电解质和水,也可以用于血液透析程序的启动溶液,用于启动和终止输液,以及用作药物的稀释溶剂。即使不存在无菌风险,颗粒无也可能造成栓塞,最终形成中风或者其他器官的梗塞,从而影响整体功能损伤。颗粒的来源,可能是灌装环境空气、包装引入等等,为了规避这个风险,有些输液管还会配有过滤装置,能过滤直径5微米以及更小的颗粒,有效减少异物脱落进入人体的风险。这种更适用于儿童、老年、肿瘤、心血管等长期输液的病患。当然避免产生颗粒才是最重要的,注射液的颗粒物风险不能过度依赖后端的输液器过滤。当责任后移,往往会导致前端的问题越来越大。因为会觉得后端有兜底保险,从而放松警惕,总觉得后面严重了,再集中处理,对于达到警戒线的问题也放任发展。
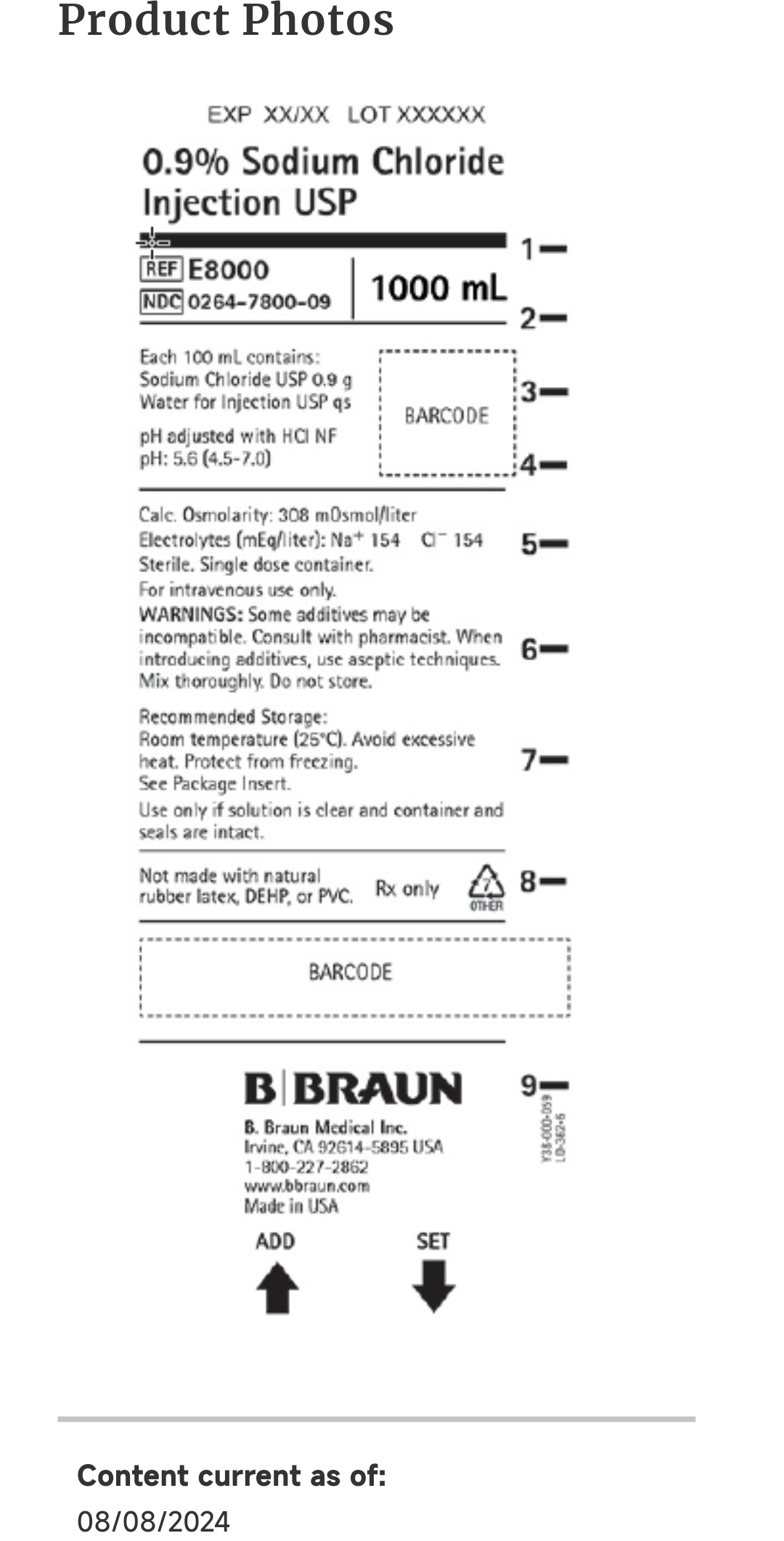
图源:FDA
看到召回通知,要注意看是企业自行发起召回,还是因为外界投诉不良反应而召回,这对应着不同的理念以及问题严重程度。很多企业的召回是从留样检发现问题,是先于医疗使用端的,这一般表明企业留样检测有较好的运转。有些是被投诉反馈才发起召回,这样的就需要注意自身的留样检,有无起到作用。很多时候,检测留样是很繁琐的,就像有些药企可能三个月都没有生产,生产工都轮流调休了,而质量部却还是月月不落地有留样检测需求,忙得很充实。如果为了减少工作量,留样检只是走个形式,那可能就真的是拿病患的风险来给自己做警示了。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57