近日,苏州赞荣医药自主研发的ZN-A-1041肠溶胶囊获得了国家药品监督管理局药品审评中心(CDE)的突破性疗法认定。ZN-A-1041的突破性在于其独特的联合治疗方案,即与卡培他滨和曲妥珠单抗联合使用,针对那些已经接受过含曲妥珠单抗治疗但仍出现病情进展的HER2阳性晚期脑转移乳腺癌患者。这一患者群体面临着极大的治疗挑战,传统疗法往往难以有效控制病情,而ZN-A-1041的加入为他们提供了新的治疗选择和希望。罗氏以总额6.8亿元购买了该药的全球权益的授权。
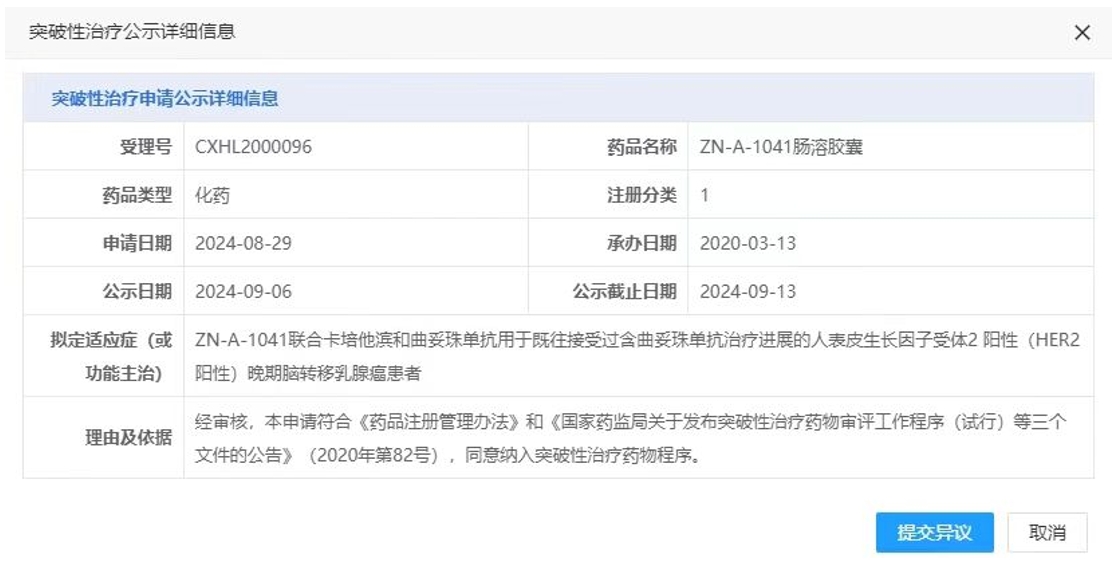
图片出自:参一
ZN-A-1041:BIC小分子的独特魅力
ZN-A-1041是一款由赞荣医药自主研发的口服小分子HER2酪氨酸激酶抑制剂(TKI),它不仅具有高度的选择性,能够精准靶向HER2受体,还展现出卓越的血脑屏障通透性。这一特性在当前的抗癌药物中极为罕见,使得ZN-A-1041能够有效地穿越血脑屏障,针对脑转移病灶进行治疗,从而填补了当前市场的空白。此外,ZN-A-1041在临床试验中还表现出良好的安全性和耐受性,即使在联合治疗中也能保持稳定的疗效,这为其在临床上的广泛应用奠定了坚实的基础。
在分子设计层面,ZN-A-1041通过精妙的化学结构调整,实现了对HER2的高选择性抑制,同时避免了对野生型EGFR等无关受体的影响,从而减少了不良反应的发生。这种"精准打击"的策略不仅提高了治疗效果,还改善了患者的生活质量。此外,ZN-A-1041还具备出色的药物代谢动力学特性,确保了药物在体内的稳定释放和有效浓度,为持续治疗提供了有力保障。
ZN-A-1041的I期临床试验还纳入了多种类型的肿瘤患者,包括伴或不伴脑转移的乳腺癌患者以及胃癌患者等。这一广泛的适应症研究不仅验证了ZN-A-1041的广谱治疗潜力,也为其在未来的药物开发和商业化道路上提供了更多的可能性。
ZN-A-1041的疗效
ZN-A-1041在临床试验中展现出的疗效令人振奋。在2023年ASCO年会上公布的早期临床数据显示,ZN-A-1041在治疗HER2阳性乳腺癌脑转移患者方面取得了显著成果。在单药治疗组中,对于既往未接受TKI治疗的HER2阳性肿瘤患者,总客观缓解率(ORR)和颅内客观缓解率(iORR)均达到了50%,最长治疗时间更是达到了15个月。而在联合卡培他滨和曲妥珠单抗的联合治疗组中,对于完成至少两次肿瘤评估的脑转移乳腺癌(BCBM)患者,总ORR提升至78.9%,iORR达到73.7%,疾病控制率(DCR)更是实现了惊人的100%。这一数据不仅证明了ZN-A-1041在治疗HER2阳性乳腺癌脑转移方面的巨大潜力,也为其未来的广泛应用提供了有力支持。
值得一提的是,ZN-A-1041的I期临床试验还纳入了多种类型的肿瘤患者,包括伴或不伴脑转移的乳腺癌患者以及胃癌患者等。这一广泛的适应症研究不仅验证了ZN-A-1041的广谱治疗潜力,也为其在未来的药物开发和商业化道路上提供了更多的可能性。
结语
罗氏斥资6.8亿美元购入ZN-A-1041的全球权益,是其在HER2阳性肿瘤治疗领域的重要布局。ZN-A-1041作为一款潜在的BIC小分子药物,凭借其高度的血脑屏障通透性和卓越的临床数据,展现了其在治疗HER2阳性乳腺癌脑转移方面的巨大潜力。此外,罗氏与赞荣医药的此次合作,不仅彰显了双方对创新药物研发的共同追求与坚定信念,也为全球肿瘤治疗领域注入了新的活力。罗氏作为全球领先的制药巨头,其丰富的市场资源、强大的研发能力和广泛的销售网络,将为ZN-A-1041的后续研发、临床试验及市场推广提供强有力的支持。
参考文献
1. 中国国家药监局药品评审中心官网
2. 罗氏制药宣布收购赞荣医药ZN-A-1041全球权益https://www.roche.com/media/releases/med-cor-2023-05-09
3. ZN-A-1041:一款潜在的BIC小分子HER2抑制剂在HER2阳性乳腺癌脑转移治疗中的早期临床研究



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57