2017年12月29日,CFDA在年末送出了元旦大礼包,国内首批通过仿制药质量和疗效一致性评价的品种名单新鲜出炉,共涉及12个仿制药品种的17个规格,7家制药生产企业。
除了华海药业以大赢家的姿态再度成为焦点之外,首批名单中还有一项特别的信息,即厄贝沙坦片是唯一一个拥有两家生产厂家通过批准的产品,也是首批通过一致性评价的品种中获批规格最多的仿制药。
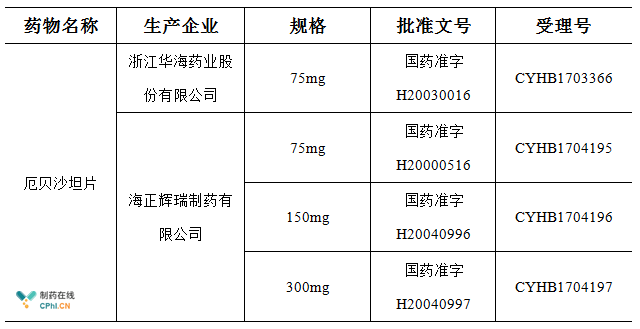
专利已过期的原研产品依然主导国内市场
厄贝沙坦属于血管紧张素Ⅱ受体抑制剂,主要用于原发性高血压、合并高血压的Ⅱ型糖尿病肾病治疗。厄贝沙坦片的原研药为赛诺菲旗下的安博维,这款产品于1997年获得FDA批准,已上市品种的规格包括75mg、150mg以及300mg,其中300mg规格的产品曾被FDA列为橙皮书中的参比制剂。
2016年,国内厄贝沙坦制剂的销售额超过33亿元,大约占了沙坦类药品市场规模的1/4。从历史数据来看,在国内厄贝沙坦片市场中,原研药专利已经过期的赛诺菲依然是国内市场中这一细分领域的领军企业,原研产品占有的市场份额一直超过77%。
PDB销售数据显示,2017年1月至9月国内市场厄贝沙坦片的销售额大约为18.48亿元。查阅CFDA官方网站的公示信息,国内厄贝沙坦片的现有药品批准文号共有12个,涉及到9家制药生产企业。根据艾美达数据库的统计,2017年前三季度厄贝沙坦片全国样本医院销售额的TOP6制药生产企业见下图,恒瑞医药是继赛诺菲之后的第一大国内制药生产企业,华海药业和海正辉瑞分列第5名和第6名。
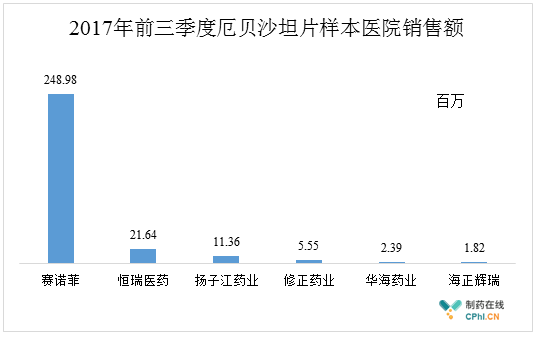
国产仿制药进口替代 潜力大
在这款固体口服制剂产品的一致性评价完成之前,华海药业和海正辉瑞均已经通过制剂国际化路径使得旗下的厄贝沙坦片在美国成功上市。其中,华海药业规格为75mg的产品于2012年9月在美国获批上市,海正辉瑞75mg、150mg以及300mg三个规格的产品于2016年6月在美国获批上市。
相似地,这两家制药生产企业的厄贝沙坦片均属于海外ANDA转报国内的路径,从类型判断,境内共线生产并在欧美日上市的品种是获批一致性评价的潜力优势品种。此次,二者同时通过了首批仿制药质量和疗效的一致性评价,国内制药企业海外ANDA回归国内除优先审评审批之外的又一种利好开始显现。
回到初始,CFDA旨在通过仿制药质量和疗效的一致性评价使我国国产药品与外资原研药在质量上一致、在临床上可以相互替代。简言之,一致性评价的初衷之一就是实现仿制药对进口原研药的替代。
这里粗略地以上述TOP 6制药企业在国内厄贝沙坦片样本医药的销售数据估算,原研药企赛诺菲的市场占比超过85%,占比的本土制药企业恒瑞医药为7.42%,不及原研产品的1/10,此次拿下一致性评价的华海药业和海正辉瑞合计的占比为1.44%。
从这种简单的市场份额对比中,我们可以粗略看到国内厄贝沙坦片市场中未来国产仿制药替代进口原研产品的潜力。另外,单单从此次通过一致性评价的品种结构来看,华海药业获批的产品规格为75mg,海正辉瑞获批的规格包括75mg、150mg以及300mg,海正辉瑞的获批产品不仅与原研产品的规格一致,而且在满足市场的需求方面似乎具有更大的潜力。
先发优势争夺战 还有谁要来玩
值得注意的是,厄贝沙坦片并不属于289基药目录品种。按照仿制药质量和疗效一致性评价工作安排,对于289基药目录品种以外的化学药品仿制药口服固体制剂,企业自行组织开展一致性评价工作,这就是说2018年底并非厄贝沙坦片这款口服固体制剂一致性评价时间的大限。
综合目前国内利好一致性评价品种的政策,通过一致性评价的仿制药品种将享受到至少以下四个方面的政策激励:
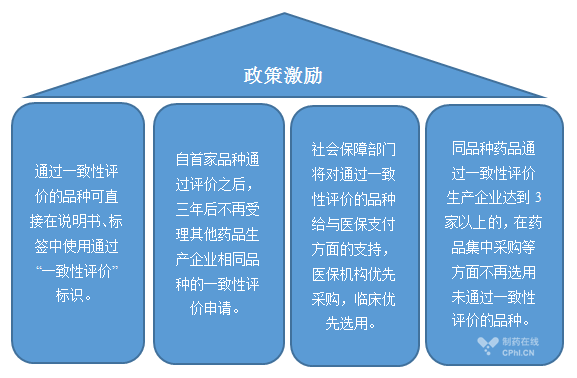
有业内人士解读,集中采购是一致性评价的主要政策驱动点,但是这并非是决定未来销售增长的核心竞争力,无论进口替代与否。一致性评价的通过的确为制药生产企业提供了先发优势,此次首批通过的仿制药品种也颇具明星产品的范儿。
不过,从某种程度而言,这可能也意味着下一轮的实力比拼才刚刚开始,最终销售业绩的增长还是得依赖于各自的神通,尤其是对于销量极度依赖医院终端的品种而言,后续各省的中标情况以及制药生产企业对于医院终端的覆盖和推广能力可能在很大程度上决定了产品的未来业绩。
然而,不论各方的实力究竟如何,厄贝沙坦片这一仿制药品种"三年"的受理期限倒计时已经开始,下一位冲刺一致性评价的后来者又将会是谁呢?
作者简介:小药丸,制药行业从业者,自媒体时代的文字搬运工,专注于制药圈内的阴晴冷暖。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57