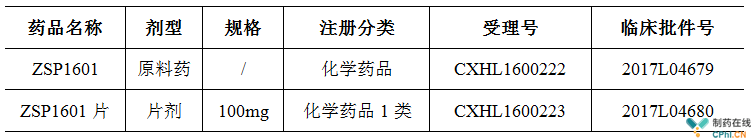
本周,广东众生药业股份有限公司发布公告,公示ZSP1601的Ⅰ期临床试验启动,首例受试者已经入组。ZSP1601是用于非酒精性脂肪性肝炎(NASH)治疗的1类化学小分子创新药,也是国内首个进入临床阶段的在研非酒精性脂肪性肝炎治疗新药。
2017年10月,众生药业旗下的ZSP1601原料药及片剂收到了CFDA核发的《药物临床试验批件》。随后经过了临床试验方案、专家论证及伦理审查环节,此次Ⅰ期临床试验的启动是继获批临床之后的又一个标志性的新阶段。
中国首个1类NASH治疗在研新药 中美两地同步公示临床
从全球范围来看,目前权威的药物监管机构如FDA和EMA尚未批准任何一款可用于NASH治疗的药品,这一领域还属于空白。
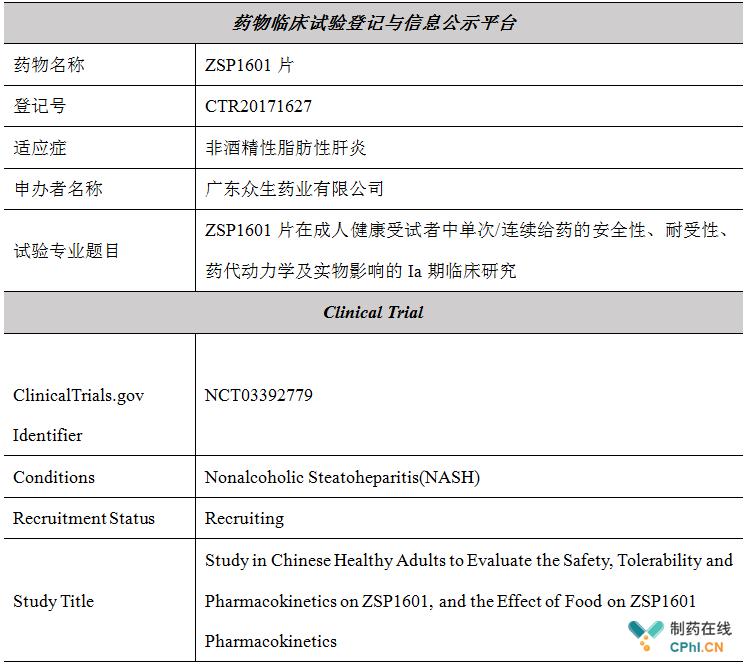
ZSP1601是国内首个获批临床的用于NASH治疗的小分子化学创新药物,由众生药业与药明康德合作共同开发。临床前研究结果显示,ZSP1601抗炎及抗肝纤维化作用显著,尤其在抗肝纤维化方面的强效作用表现出色,这种潜在的疗效优势是NASH新药领域最重要的关注点。作为具有全新作用机制的的1类在研化学新药,ZSP1601具备了成为First-In-Class级别药物的潜力。
此次,ZSP1601临床试验启动并按照相关法规要求在中国和美国两地同步进行临床试验的登记和信息公示。
全球Ⅲ期临床NASH在研新药概览
根据德意志银行分析师的预测,2025年全球NASH治疗药物的市场将达到350~400亿美元的规模。这一肝病治疗细分市场的未来预期被普遍看好,属于潜在的价值高地,吸引了包括众多制药公司的参与,这其中既包括了诸如吉利德、诺和诺德等国际制药巨头,又包括了像Akarna这样的小而美的制药公司,基于NASH创新药物开发的项目次第展开。据不完全统计,目前处于Ⅱ期临床试验阶段的试验数量总数超过了20项。
在众多的开发项目中,最有希望率先获批拿下NASH适应症的在研新药当属处于Ⅲ期临床试验的在研品种,见下表。
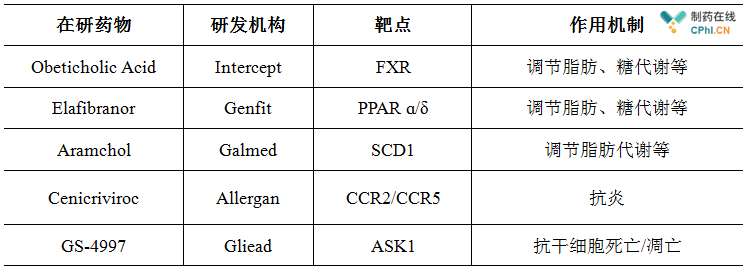
其中,Intercept公司旗下的Obeticholic Acid于2016年5月通过了FDA的批准,用于原发性胆汁性胆管炎的治疗。目前,Intercept公司针对Obeticholic Acid用于NASH治疗的临床试验正在进行中。在下表中处于Ⅲ期临床试验的品种中,进展最快的似乎是Genfit公司旗下的在研新药Elafibranor,该药物是化学合成的PPAR ɑ/δ双重激动剂。据悉,业内人士乐观估计这款在研药物将于2019年获批上市。无疑,Elafibranor将成为Intercept公司Obeticholic Acid用于NASH治疗的强有力竞争者之一。
作者简介:小药丸,制药行业从业者,自媒体时代的文字搬运工,专注于制药圈内的阴晴冷暖。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57