2019年2月22日,信达生物制药(以下简称“信达生物”)主办的抗肿瘤新药达伯舒®(信迪利单抗注射液)上市新闻发布会在京顺利举行。同时,由希思科临床肿瘤学研究基金会和信达生物共同发起的“希思科—信达肿瘤免疫治疗研究基金”也正式启动。
信迪利单抗由信达生物和礼来制药合作开发,是首个国内上市的针对经典型霍奇金淋巴瘤(cHL)的国产PD-1单抗,其研发和生产质量均达到国际标准。基于ORIENT-1研究,信迪利单抗已经于2018年12月24日正式获得国家药品监督管理局的批准,用于至少经过二线系统化疗的复发或难治性cHL的治疗。该研究结果获得国内外专家的认可,并刊登为国际著名期刊《柳叶刀•血液学》杂志封面文章。
试验设计
ORIENT-1研究是一项2期多中心单臂(即没有对照,所用受试者都使用试验药物)临床试验,共有18家来自中国的医学中心参与,入组患者为年龄≥18岁,接受过≥2线治疗的复发难治性cHL患者。静脉给予信迪利单抗200mg,每3周一次,直至疾病进展、死亡、出现不可接受**或撤出研究,主要研究终点是客观缓解率。
试验结果
自2017年4月19日至2017年11月1日,共招募96例患者,其中4例患者的诊断未经病理中心确认,故未纳入分析,10例患者停用治疗,中位随访10.5个月。纳入分析的92例患者中,74例患者(80.4%)获得了客观反应,90例患者疾病控制(97.8%),完全缓解31例(34%),部分缓解43例(47%),疾病稳定16例(17%)。(具体如下图所示)
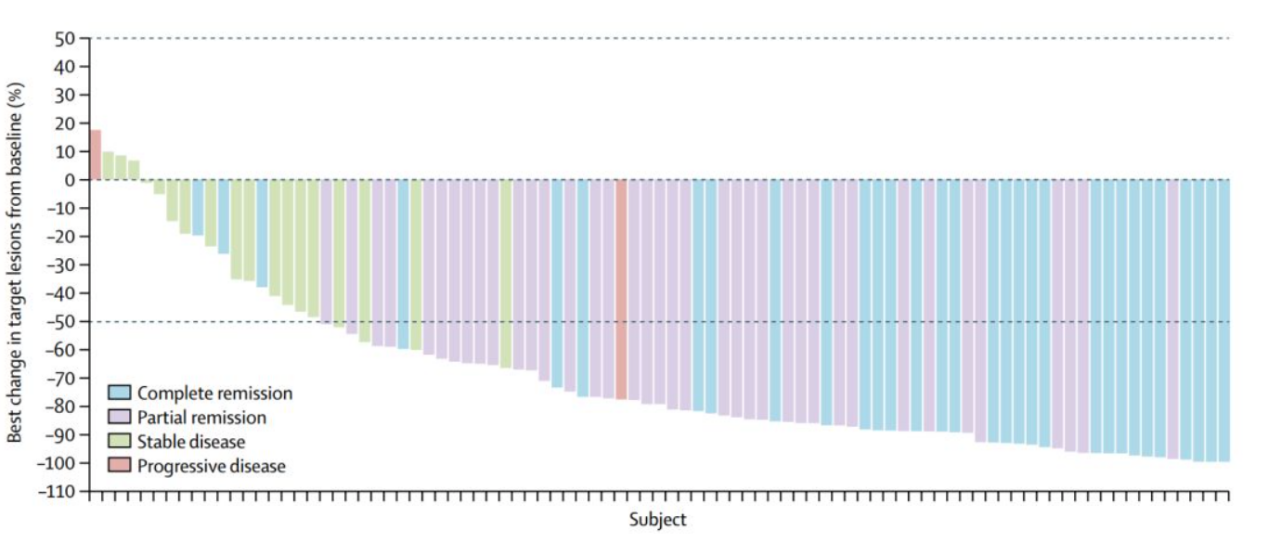
肿瘤大小变化比例
副反应分析
89/96例(93%)出现治疗相关副反应(表2),其中17例(18%)发生3或4级治疗相关不良事件,最常见的不良反应是发热,研究中没有患者死亡。ORIENT-1研究结果充分显示了信迪利单抗治疗复发难治cHL的疗效,同时也证实了该药良好的安全性和耐受性,研究中只有3例患者因为不良反应而停止治疗,多数不良反应为轻度可控,无不良反应导致的死亡。
什么是经典型霍奇金淋巴瘤?
淋巴瘤是我国常见的恶性肿瘤之一,发病率约为6.68/10万人,居各类癌症发病率的第八位,并且近几年呈增长趋势,已成为我国公共卫生不容忽视的重要问题。其中经典型霍奇金淋巴瘤是一种B细胞恶性淋巴瘤,发病人群分布相对集中,多发生于20-40岁的中青年人。2014年经典型霍奇金淋巴瘤发病率0.4/10万人,并以5%的年增长率增长。尽管联合化疗与放疗的初始治疗使经典型霍奇金淋巴瘤治愈率较高,但一线治疗后仍有15%-20%的患者为复发或难治性经典型霍奇金淋巴瘤,造血干细胞移植治疗失败后的病人平均存活期只有1~2年左右。中国复发难治cHL患者的治疗需求一直未能得到满足。信迪利单抗预计三月底正式在国内开售,将填补这一空白。
定价
信达生物首席商务官刘敏先生表示,信迪利单抗的定价会低于市面同类进口药物。同时,医保谈判开启,信达生物将积极推动信迪利单抗进入医保目录,造福更多肿瘤患者。
目前,信迪利单抗的其他20多项临床试验也正在进行之中,包括一线非鳞非小细胞肺癌、一线肺鳞癌、二线肺鳞癌、EGFRTKI治疗失败的EGFR突变阳性的非小细胞肺癌、一线胃癌、一线肝癌、一线食管癌、二线食管癌等。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57