近日,全球权威医学期刊柳叶刀相继公布了两款腺病毒载体新冠**的II期临床研究结果,相关**在受试者中产生了较好的免疫反应,均无严重不良反应出现,新冠**的开发再次迎来了好消息。
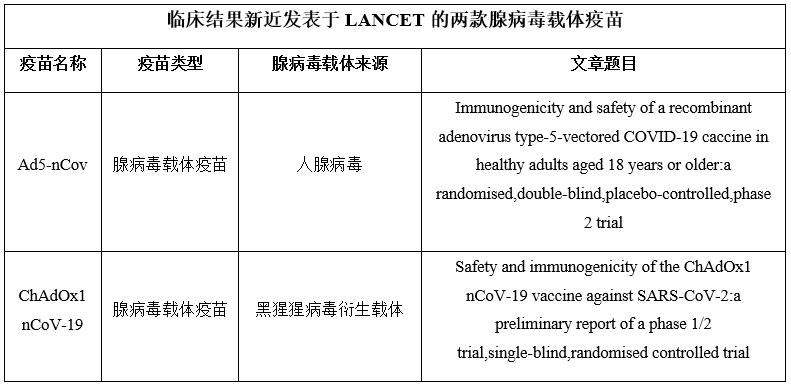
资料来源:公开资料整理
临床试验设计
康希诺Ad5-nCov
康希诺Ad5-nCov的临床研究是一项单中心随机,双盲,安慰剂对照II期临床研究。该试验在武汉共招募了508名受试者,均为健康成年人。
基于单剂高剂量优于两剂低剂量的假设,同时为了避免Ⅰ期临床中的发热等不良反应,试验设置了1×1011个病毒颗粒/ mL的低剂量组(253人)、5×1010个病毒颗粒/ mL的高剂量组(129人)及安慰剂组(126人)。试验终点为病毒受体结合区(RBD)抗体滴度和第28 天的中和抗体反应,及接种后 14 天内安全性,旨在验证 Ad5-nCov **的免疫原性和安全性。
牛津大学ChAdOx1 nCoV-19
牛津大学ChAdOx1 nCoV-19的临床研究为一项单盲,随机对照Ⅰ/Ⅱ期临床研究,共招募了1077名18-55岁的健康受试者。
试验将表达SARS-CoV-2 S蛋白的ChAdOx1 nCoV-19与脑膜炎球菌结合**进行比较,将受试者随机分配为5x1010vp ChAdOx1 nCoV-19组(543人)和一次肌注MenACWY组(534人),设置的主要有效性终点为病毒学症状,安全性终点为接种后 28 天严重不良反应率,旨在评价 ChAdOx1 nCoV-19 **的免疫原性和安全性。
临床试验结果
康希诺Ad5-nCov
康希诺Ad5-nCov临床试验结果显示:高、低剂量试验组血清阳转率 96%和 97%,其中中和抗体血清转阳率为 59%和 47%;第 28 天 RBD 抗体滴度峰值分别为 656.5 及571.0,针对活病毒的中和抗体反应显著,其滴度的平均值分别为 19.5和18.3;实验组患者均无严重不良反应发生。
牛津大学ChAdOx1 nCoV-19
牛津大学ChAdOx1 nCoV-19临床试验结果显示:在**首次接种28天后,抗体反应达到峰值,接种第二剂**后抗体浓度增加。MNA80 中和抗体检测阳性率91%,PRNT50 中和抗体检测阳性率 100%,所有受试者都产生了中和抗体,抗体的浓度与康复者及感染者血浆抗体浓度相近。
两款腺病毒载体的差异
根据WHO公布的数据,截止2020年7月14日,全球共计163个新冠**处于研发当中,其中处于临床中、临床前的在研产品分别为23个、140个,包括DNA**、mRNA**、重组病毒载体**核酸**共计78个,占比约 48%,在数量上位居第一。
自20世纪80年代以来,临床研究已经建立了以多种病毒作为载体的**。其中,腺病毒(Ad)载体是最常用的病毒载体之一,目前已被识别的人类腺病毒共分为七个属种的57种病毒。
研究发现,腺病毒载体**能够诱导人体产生有效的细胞免疫和体液免疫,其免疫原性的强弱取决于所使用腺病毒的血清型,复制缺陷Ad5是应用最为广泛的腺病毒载体之一。
然而,在人类中广泛存在对该病毒的免疫,可以抑制病毒载体转染细胞的效率和目标抗原基因的表达,且**接种的可重复性较差,阻碍其临床应用。康希诺Ad5-nCov的临床试验结果显示,受试者对其**中使用的病毒产生了抗体,推测这些患者曾经接触过这种病毒并预先建立了防御,这种防御性的免疫力可能意味着指令无法顺利进入靶细胞,影响**效果。
通过开发非人类起源的腺病毒载体能够解决这一问题,如牛津大学开发的黑猩猩病毒衍生载体。此次ChAdOx1 nCoV-19的临床研究结果显示,98位参与检测的受试者中,仅有一人存在针对该病毒载体的较高免疫力。
不过,上述两项腺病毒载体**研究的测试指标并不相同,暂时难以进行较为准确的比较。从Ⅱ期临床结果的整体看来,这两种候选**数据积极,都证明了**能够在安全性的前提下有效刺激人体产生针对冠状病毒关键蛋白的抗体。基于目前Ⅱ期试验结果,这两款**都将推进 Ⅲ 期临床研究。
作者简介:小药丸,制药行业从业者,自媒体时代的文字搬运工,专注于制药圈内的阴晴冷暖。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57