
目前,全球新冠疫情的防控形势依然严峻,部分地区仍然持续恶化。截至11月中旬,全球累计新冠感染人数已接近1700万人,死亡人数已超过138万人。在尚无有效治疗药物可大规模应用的大背景之下,作为预防型手段的**将是阻断疫情传播扩散的有力武器。
据不完全统计,目前全球已申报临床的新冠**数量已超过200种,其中的10个品种进入了临床Ⅲ期阶段。
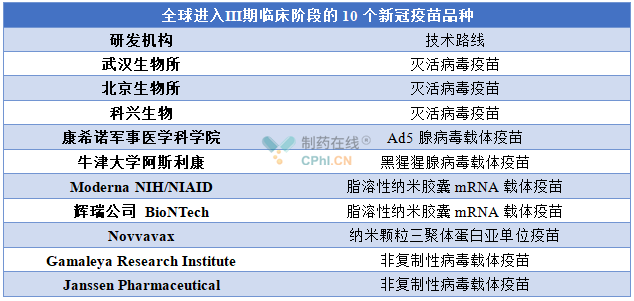
资料来源:公开资料整理
新型技术平台新冠**的比较
从**类型来看,上述进入Ⅲ期临床的**除了灭活病毒**之外,腺病毒载体**、mRNA载体**及非复制性病毒载体**等新型技术**的表现着实亮眼。
不同类型**在抗原选择及免疫应答等诸多方面都存在着显著性的差异:
传统的病毒减毒**和病毒灭活**的抗原是完整的病原体,免疫原性较弱,需要多次接种,通常引起体液免疫,不引起细胞免疫;优点是这两类**已经广泛使用了多年,工艺成熟、制备技术相对较简单。
病毒载体**通过非致病性微生物表达病原物抗原,模拟病原体的感染过程,诱导免疫反应,可以诱导更为均衡的免疫应答,且载体本身可发挥佐剂效应;当前已经有人类腺病毒、痘病毒、麻疹病毒等应用到**研发中,目前在研的病毒载体**品类广泛,针对埃博拉病毒的腺病毒载体和rVSV载体**已经获批,新冠品种中包含多种病毒载体平台;但已感染过微生物的人群对这类**具有免疫力,效果会打折。
mRNA**不仅能够全面的诱导体液免疫与细胞免疫应答,并且RNA本身可以作为激活DC细胞TLR样受体的配体以达到刺激Ⅰ型干扰素分泌及其下游基因的响应,进而抑制病毒复制、增强抗病毒的效果;不过mRNA的稳定性差,递送系统的开发成为了mRNA**技术的关键。
非复制性病毒载体**可有效诱导体液免疫和细胞免疫,但对载体的纯度和活性要求高。
新技术**成功应用的实例
截至目前,上述新技术**的其中一些已经取得了实质性的进展。
BioNTech/辉瑞mRNA技术路径新冠品种BNT162b2成为首个披露临床Ⅲ期初步数据的品种,数据显示完成接种后7天保护率超过90%。回顾之前BNT162b2披露的美国、德国两地Ⅰ/Ⅱ期临床的数据,均呈现出了良好的中和抗体反应和细胞免疫应答。辉瑞预计在2020年供应产能5000万剂,在2021全年供应产能13亿剂。继BioNTech/辉瑞mRNA技术路径新冠品种BNT162b2打头阵之后,Moderna的mRNA-1273临床数据表现积极,能够同时兼顾细胞免疫与体液免疫,25μg、100μg两组在S1和S2肽环境刺激下都引起CD4+ T细胞应答,100μg剂量组在第二次接种后检查到低水平的CD8+ T细胞应答。
除了新冠**领域之外,2017年在mRNA寨卡**中首次亮相的LNP系统因其稳定的递送效果成为当前国际上多数mRNA技术相关企业的共同选择。
病毒载体**已有成功获批上市的案例。2019年11月,默沙东病毒载体**rVSV-ZEBOV 获得EMA的有条件批准上市,同年12月又获美国FDA批准上市,商品名为ERVEBO,用于18岁及以上人群的主动免疫,以预防由扎伊尔型埃博拉病毒引起的埃博拉病毒病。在我国,由军事医学和康希诺共同研发的5型腺病毒载体埃博拉病毒病**Ad5-EBOV,于2017年10月作为1类预防用生物制品获得了中国新药申请批准,已申请作为应急使用及国家储备,是我国第一款获批的埃博拉**。
在此次抗击新冠疫情的**开发热潮中,康希诺Ad5-nCovAd5-nCoV 采用基因工程方法构建,以复制缺陷型人5型腺病毒为载体,可表达新型冠状病毒 S 抗原。临床试验结果显示:高、低剂量试验组血清阳转率96%和 97%,其中中和抗体血清转阳率为 59%和 47%;第 28 天 RBD 抗体滴度峰值分别为 656.5 及571.0,针对活病毒的中和抗体反应显著,其滴度的平均值分别为 19.5和18.3;实验组患者均无严重不良反应发生。
尚未得到验证的非复制性病毒载体**
非复制性病毒载体**通过人工合成的非病毒载体材料介导基因的转移,通常将含有编码的蛋白基因序列的质粒载体,经肌肉注射导入体内,通过宿主细胞表达抗原蛋白,进而诱导体液免疫和细胞免疫。
这类**的制备过程相对简单,易于大规模生产,在产业化方面具有明显的优势;然而,这类**有潜在的致癌风险,目前仍未得到市场验证。
新型技术**的共有特点
无论是腺病毒载体**、mRNA载体**,还是非复制性病毒载体** ,这三类新型技术**目前均具有相对成熟的技术平台作为支撑,基于平台技术,通过不同抗原核酸序列的搭载可以实现**品种的快速拓展;同时,这类**使用的抗原物质即核酸制备简单快速,**的生产周期短,产量也易于放大;除此之外,这些新型技术**可模拟病原体感染过程,在免疫应答诱发方面更均衡全面。
作者简介:小药丸,制药行业从业者,自媒体时代的文字搬运工,专注于制药圈内的阴晴冷暖。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57